主要区别
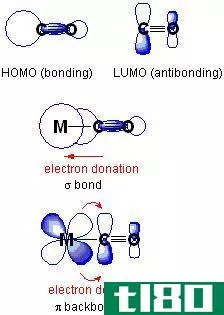
当两个原子相互作用时,它们在它们之间形成一种化学键,通过这种键把它们结合在一起。所以,在化学领域,一种用来把物体绑在一起的东西叫做化学键。化学键分为离子键、共价键、极性键和氢键。在这里,我们将讨论sigma键和pi键,它们是共价键的类型。Sigma键(σ键)是原子轨道之间头部重叠形成的最强的化学键(共价键),而pi键(π键)是与Sigma键(σ键)相比较弱的化学键(共价键)。当一个轨道的两个波瓣与第二个轨道的两个波瓣重叠时形成。
比较图
什么是西格玛键(sigma bond)?
Sigma bond也被写成σbond,因为符号σ是用于Sigma的希腊字母。σ键(σ键)是原子共价键的一种。它是两个原子之间形成的最强的共价键。它是由原子轨道的头部沿原子核间轴相互重叠而形成的。所形成化合物的相对性与某些σ键(σ键)成反比,而化合物的稳定性与σ键(σ键)的数目成正比。这个键决定了分子的形状,核间轴上的重叠使分子绕着它的轴旋转,这使它具有旋转对称性。σ键(σ键)可以由轨道和p轨道组成。有趣的是,单键只包含一个σ键(σ键),而像双键和三键这样的多键也只包含一个σ键(σ键)。西格玛键(σ键)的例子有氨(NH3)和苯环等。
什么是π键(pi bond)?
π键也被写成π键,因为π是用来表示π的希腊字母。π键(π键)是原子中的一种共价键。与sigma键(σ键)相比,它是一种较弱的共价键。π键是原子轨道横向重叠形成的。其次,由于π键(π键)比其它键弱,因此存在部分重叠。所形成化合物的相对性与一些π键(π键)成正比,而化合物的稳定性与π键(π键)的数目成反比。这个较短的键决定了分子的长度。轨道重叠垂直于原子的核间轴,原子不允许旋转,这意味着这种键具有非旋转对称性。π键(π键)只由p轨道形成。有趣的是,一个单键只包含一个π键(π键),而像双键这样的多个键有两个π键(π键),而三键有三个π键(π键)。π键(π键)的例子是二羰基(C2)和二硼烷(B2H2)。
西格玛键(sigma bond) vs. π键(pi bond)
- Sigma键(σ键)是两个原子之间形成的最强的共价键,而pi键(π键)是与Sigma键(σ键)相比较弱的共价键类型。
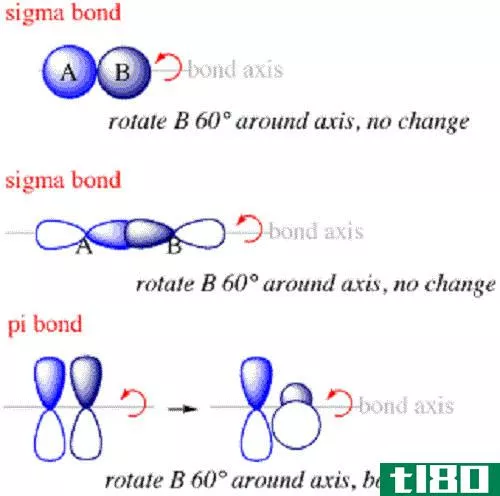
- Sigma键(σbond)是原子轨道头部沿原子核间轴相互重叠形成的,而Pi键(π键)是原子轨道重叠形成的。
- σ键(σ键)决定了分子的形状,而π键(π键)决定了分子的长度。
- σ键(σ键)可以绕核间轴旋转,而π键(π键)不能绕核间轴旋转。
- 在σ键(σ键)中,所形成化合物的相对性与某些σ键(σ键)成反比,而化合物的稳定性与σ键(σ键)的数目成正比。相反,在π键(π键)中,形成的化合物的相对性与一些π键(π键)成正比,而化合物的稳定性与π键(π键)的数目成反比。
- 在sigma键(σ键)的情况下,一个单键只包含一个sigma键(σ键),然后像双键和三键这样的多个键也只包含一个sigma键(σ键)。另一方面,在π键(π键)的情况下,一个单键只包含一个π键(π键),而像双键这样的多个键有两个π键(π键),而三键有三个π键(π键)。