主要区别
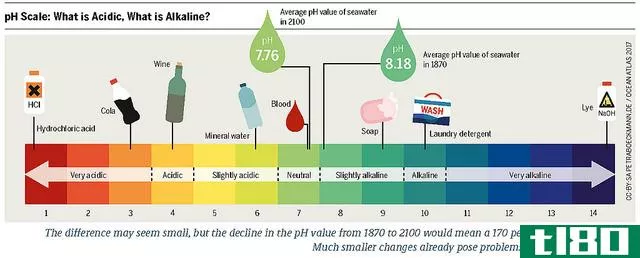
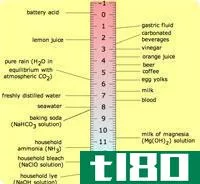
酸和碱是被称为相互对立的化学化合物。它们是各种属性,以及可以区分它们的定义。酸被称为是质子供体的化合物,当它们混合在水溶液中时,会提高H+离子的浓度,而碱是作为质子受体的化合物,当它们混合在水溶液中时,会增加OH-离子的浓度。除此之外,由于酸是一种化合物,当溶液溶解于水(即pH值小于7.0)时,它比纯水具有更高的氢离子活性。与此相反,碱是一种化合物,当溶液溶解在水中(即pH值高于7.0)时,它使溶液的氢离子活性低于纯水。
比较图
什么是酸的(acid)?
酸是一种pH值低于7的化合物,它具有提供质子和接受电子对的能力,当它混合或溶解在水溶液中时,它会增加H+离子的浓度。酸是化学中不可分割的化合物之一,许多著名化学家对酸的定义很多。上面给出的定义是一个简洁的定义,涵盖了酸的各种性质。除此之外,这里还有一些著名的酸的定义。根据阿伦尼乌斯的说法,酸是任何一种化合物,当溶解在水中时,其溶液中的氢离子活度比在纯水中更大。根据Br***tead-Lowry的说法,酸是一种能提供质子的物质。根据Lewis的说法,酸是一种能从供体化合物中接受电子对的化合物或离子物种。酸类的pH值比7强,但酸值比酸值低。它们通常有酸味,例如醋酸(CH3COOH)、硫酸和(H2SO4)盐酸(HCl)。酸使蓝色石蕊纸变红,而碱使红色石蕊纸变蓝。
什么是基础(base)?
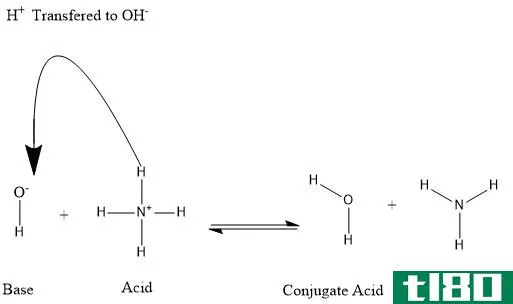
碱是一种pH值高于7的化合物,它能够接受质子并提供电子对,当它混合或溶解在水溶液中时,它会增加OH-离子的浓度。根据阿伦尼斯的说法,碱是一种可以接受氢离子的水性物质。根据Br***tead-Lowry的说法,碱是任何接受质子的物质。根据刘易斯的说法,碱是一种能给电子受体提供一对电子的物质。如上所述,碱是指pH值高于7的化合物,此处应始终提及,pH值越高,碱基越强。盐是以溶解为基础的另一种化合物,是酸和碱发生化学反应而形成的。酸碱之间的反应过程称为中和,它产生水而不是盐的形成。底座变成红色石蕊纸蓝色。碱一般有肥皂味,常见的碱有:氢氧化钠(NaOH)、氢氧化钙(Ca(OH)2)、NH3等。
酸的(acid) vs. 基础(base)
- 酸被称为是质子供体的化合物,当它们混合在水溶液中时,会提高H+离子的浓度,而碱是作为质子受体的化合物,当它们混合在水溶液中时,会增加OH-离子的浓度。
- 酸是一种化合物,当溶液溶解在pH值小于7.0的水中时,它使溶液比纯水具有更高的氢离子活性。与此相反,碱是一种化合物,当溶液溶解在水中(即pH值高于7.0)时,它使溶液的氢离子活性低于纯水。
- 酸使蓝色石蕊纸变红,而碱使红色石蕊纸变蓝。
- 酸通常有酸味,而碱一般有肥皂味。