价壳层与倒数第二层壳层的主要区别在于,价壳层是原子最外层的含电子壳层,而倒数第二层壳层是最外层含电子壳层的内层壳层。
价壳层和倒数第二层壳层这两个术语主要在普通化学中用来确定一个特定原子的电子组成。价壳层和倒数第二层包含一个或多个电子。
目录
1. 概述和主要区别
2. 什么是价壳层
3. 什么是倒数第二个贝壳
4. 并列比较-价壳层与倒数第二层的表格形式
5. 摘要
什么是价壳层(a valence shell)?
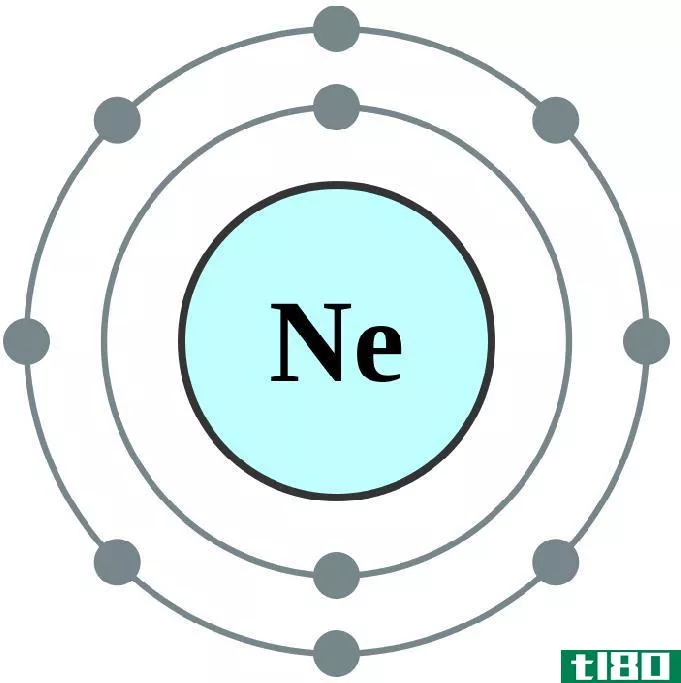
价壳层是原子最外层的电子壳。这个壳层中的电子称为价电子。这些电子对原子核的吸引力最小。这是因为价电子与原子的其他电子相比,位于远离核的很长的距离。
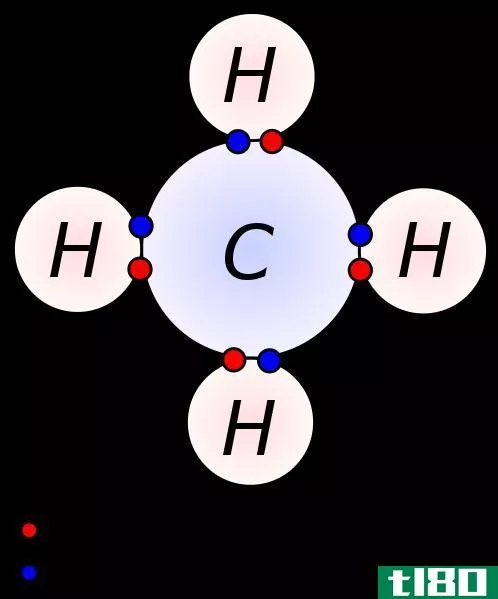
图01:参与键形成的价电子
价壳层中的电子负责原子的化学反应和化学键合。由于这些电子和原子核之间的吸引力较小,价电子可以很容易地被移除(比内轨道上的电子)。这对离子化合物和共价化合物的形成很重要。通过失去价电子,原子可以形成阳离子。将一个原子的价电子与另一个原子的价电子共用,就会形成共价键。
对于s块元素和p块元素,价壳层分别是s轨道和p轨道。但对于过渡元素,价电子也可以存在于内轨道中。这是由于子轨道之间的能量差。例如,锰的原子序数是25。钴的电子构型为[Ar]3d54s2。钴的价电子应该在4s轨道上。但Mn中有7个价电子。3d轨道上的电子也被认为是价电子,因为3d轨道位于4s轨道之外(3d的能量高于4s轨道)。
什么是倒数第二壳(penultimate shell)?
倒数第二层壳层是包含电子的壳层,位于最外层价壳层的内部。换言之,它是第二个最后一个充满电子的壳层或价壳层之前的壳层。因此,与价壳层相比,倒数第二层的电子更容易被原子核吸引。
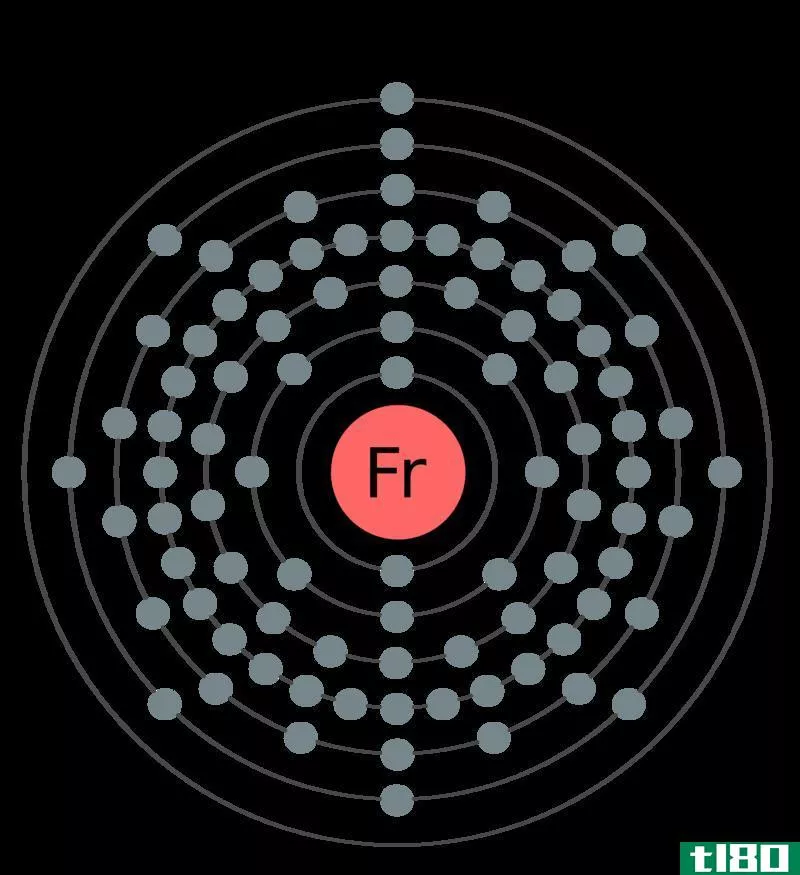
图02:在倒数第二层壳层中有八个电子的镧原子
此外,倒数第二壳层中的电子不参与化学键合和化合物形成过程,因为它们被价壳层电子覆盖。然而,在过渡金属中,倒数第二层壳层中的电子可以是金属原子的最外层电子,因为它们的子轨道能量不同。
价壳层(valence shell)和倒数第二壳(penultimate shell)的区别
价壳和倒数壳层的关键区别在于价壳是原子最外层的含电子壳。但是,倒数第二层壳层是最外层电子壳的内部。因此,倒数第二壳层比价壳更接近原子核。
此外,价壳层中的电子比倒数第二层的电子对原子核的吸引力更小。除此之外,价壳层中的电子参与化学键合和化合物的形成,而倒数第二层的电子则不参与化学反应。
下面的信息图表列出了价壳层和倒数第二层壳层之间的差异。
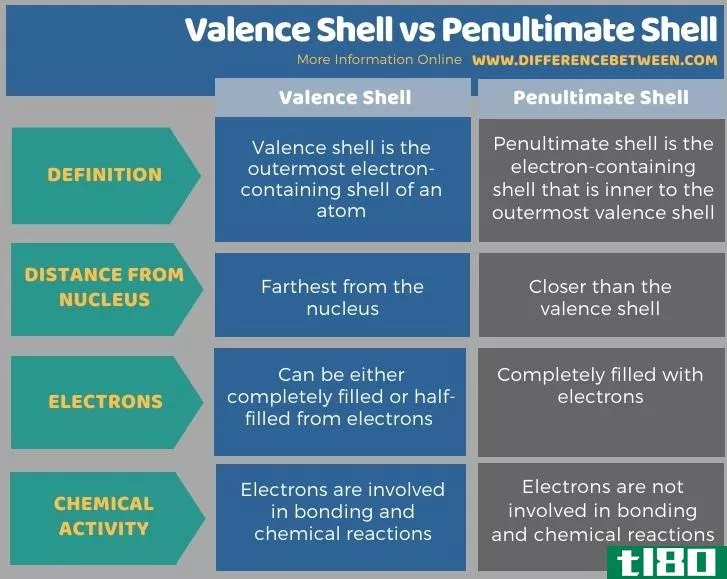
总结 - 价壳层(valence shell) vs. 倒数第二壳(penultimate shell)
价壳层和倒数壳层是普通化学中非常重要的两个化学术语。价壳层与倒数第二层壳层的主要区别在于,价壳层是原子最外层的含电子壳层,而倒数第二层壳层是原子最外层含电子壳层的内层壳层。
引用
1赫尔曼斯汀,安妮·玛丽。“化学中的价电子定义”,《图恩TCO》,2020年2月11日,
2“价电子”,《维基百科》,维基媒体基金会,2020年2月6日,