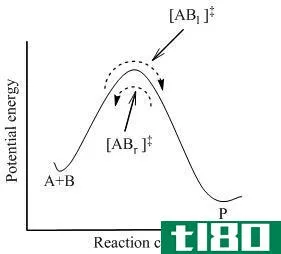
化学中的活化能定义
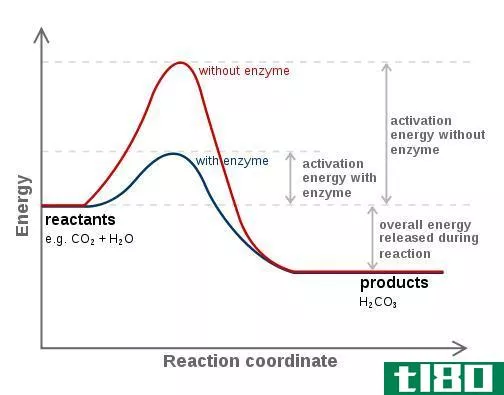
活化能是启动反应所需的最小能量。它是反应物和产物势能最小值之间势能垒的高度。活化能用Ea表示,通常单位为千焦耳/摩尔(kJ/mol)或千卡/摩尔(kcal/mol)。“活化能”一词是由瑞典科学家斯万特·阿伦尼乌斯(Svante Arrhenius)于1889年提出的。阿累尼乌斯方程将活化能与化学反应进行的速率联系起来:

k=Ae Ea/(RT)
其中k是反应速率系数,A是反应的频率因子,e是无理数(约等于2.718),Ea是活化能,R是通用气体常数,T是绝对温度(开尔文)。
从阿累尼乌斯方程可以看出,反应速率随温度而变化。通常,这意味着化学反应在较高温度下进行得更快。然而,也有一些“负活化能”的情况,其中反应速率随温度降低。
为什么需要活化能?
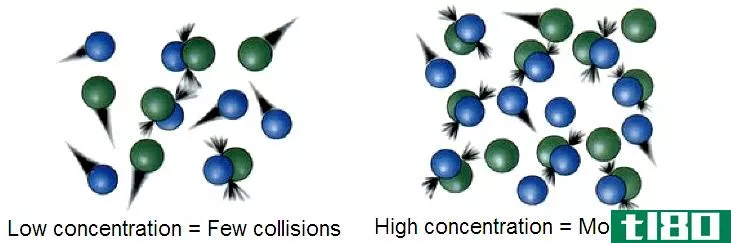
如果你把两种化学物质混合在一起,反应物分子之间自然只会发生少量的碰撞,从而生成产物。如果分子的动能很低,这一点尤其正确。因此,在很大一部分反应物转化为产物之前,必须克服体系的自由能。活化能提供了反应所需的额外推力。即使是放热反应也需要活化能才能开始。例如,一堆木头不会自行燃烧。点燃的火柴可以提供启动燃烧的活化能。一旦化学反应开始,反应释放的热量提供活化能,将更多反应物转化为产物。
有时,化学反应在不增加任何额外能量的情况下进行。在这种情况下,反应的活化能通常由环境温度的热量提供。热增加了反应物分子的运动,提高了它们相互碰撞的几率,并增加了碰撞力。这种结合使反应物之间的键更有可能断裂,从而形成产物。
催化剂与活化能
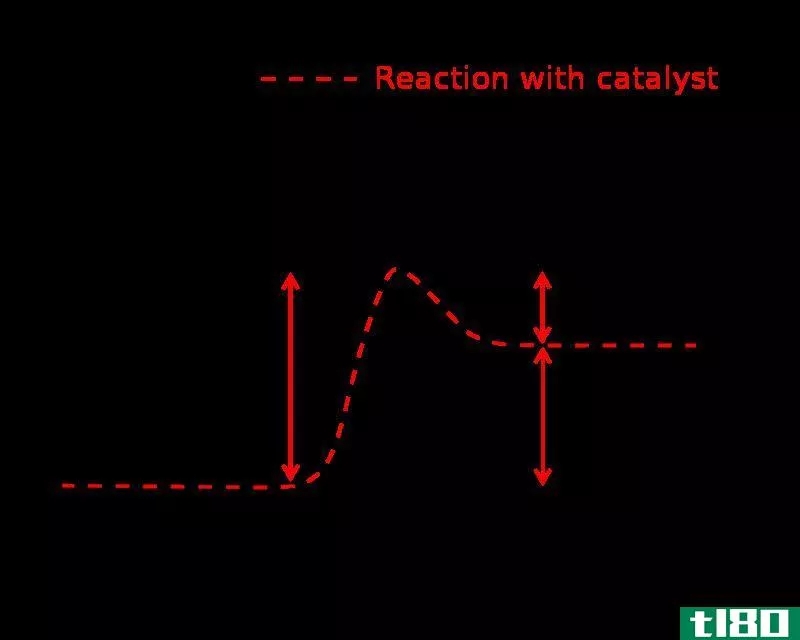
降低化学反应活化能的物质称为催化剂。基本上,催化剂通过改变反应的过渡状态起作用。催化剂不会被化学反应消耗,也不会改变反应的平衡常数。
活化能与吉布斯能的关系
活化能是Arrhenius方程中的一项,用于计算克服从反应物到产物的过渡状态所需的能量。Eyring方程是描述反应速率的另一个关系式,除了使用活化能之外,它还包括过渡态的吉布斯能。反应的焓和熵中过渡态因子的吉布斯能。活化能和吉布斯能是相关的,但不能互换。
- 发表于 2021-09-29 05:16
- 阅读 ( 392 )
- 分类:数学
你可能感兴趣的文章
催化的(catalytic)和化学计量试剂(stoichiometric reagents)的区别
催化试剂和化学计量试剂的关键区别在于,在反应过程中不消耗催化试剂,而在反应过程中消耗化学计量试剂。 催化试剂和化学计量试剂是特定化学反应中的两类反应物。催化试剂优于化学计量试剂。这是因为特定化学反应...
- 发布于 2020-09-28 18:29
- 阅读 ( 554 )
动能(kinetic energy)和活化能(activation energy)的区别
...ch less than the speed of light. 什么是活化能(activation energy)? 化学反应的活化能是为了从反应中得到产物而必须克服的能量屏障。换句话说,它是反应物转化为产物所需的最小能量。为了开始化学反应,总是需要提供活化能。 We denot...
- 发布于 2020-10-15 00:52
- 阅读 ( 727 )
碰撞理论(collision theory)和过渡态理论(transition state theory)的区别
...态理论 碰撞理论和过渡态理论是在分子水平上解释不同化学反应速率的两种理论。碰撞理论描述了气相化学反应中气体分子的碰撞。过渡态理论通过假设过渡态中间化合物的形成来解释反应速率。碰撞理论与过渡态理论的主要...
- 发布于 2020-10-16 12:41
- 阅读 ( 694 )
酶的(enzymatic)和非酶反应(nonenzymatic reaction)的区别
...酶反应的关键区别在于生物催化剂(酶)催化酶反应,而化学催化剂催化一些非酶反应,而其他非酶反应则不需要任何催化剂来催化。因此,酶反应本质上只是生物反应,而非酶反应可以是生物反应,也可以是化学反应。 酶是...
- 发布于 2020-10-17 18:28
- 阅读 ( 211 )
活化能(activation energy)和阈值能量(threshold energy)的区别
...足够的能量,我们可以用它来做一些我们想要的工作;在化学中,这个功可以是化学反应,也可以是核反应。我们用两种不同的能量形式来定义化学反应能。 目录 1. 概述和主要区别 2. 什么是活化能 3. 什么是临界能量 4. 并列比...
- 发布于 2020-10-17 18:57
- 阅读 ( 359 )
激活复合物理论(activated complex theory)和碰撞理论(collision theory)的区别
...撞理论则不太可靠。 活化络合物理论和碰撞理论是描述化学反应热力学的两个重要概念。这些理论可以用来预测化学反应的反应速率。活化络合物理论又称过渡态理论。然而,激活复合物理论被认为比碰撞理论更精确。 目录 1. ...
- 发布于 2020-10-25 22:55
- 阅读 ( 513 )
活化络合物(activated complex)和过渡状态(transition state)的区别
...物时,它们可能经历不同的修饰和能量变化。反应物中的化学键正在断裂,新的键正在形成,生成的产物与反应物完全不同。这种化学修饰被称为化学反应。有许多变量控制着反应。反应要发生,就需要能量。反应物分子在整个...
- 发布于 2020-10-27 04:37
- 阅读 ( 922 )
阿伦尼乌斯(arrhenius)和艾林方程(eyring equation)的区别
...于统计力学论证的。 阿伦尼乌斯方程和艾林方程是物理化学中两个重要的方程。当我们假设活化焓和活化熵为常数时,Eyring方程类似于经验Arrhenius方程。 目录 1.概述和主要区别 2. 什么是阿伦尼乌斯方程 3. 什么是艾林方程 4. ...
- 发布于 2021-03-04 18:53
- 阅读 ( 2143 )
养成良好习惯的“化学反应”
化学中有一个概念叫做活化能。活化能是化学反应发生所需的最小能量。假设你拿着一根火柴,轻轻地把它碰在火柴盒侧面的敲击条上。什么也不会发生,因为不存在激发化学反应和引发火灾所需的能量。这篇文章最初出现在詹...
- 发布于 2021-05-17 05:05
- 阅读 ( 214 )
催化剂(catalyst)和酶(enzyme)的区别
...催化剂。催化剂和酶的主要区别在于催化剂是一种能提高化学反应速率的物质,而酶是一种能提高生化反应速率的球状蛋白质。无机催化剂包括矿物离子或小分子。相反,酶是具有三维结构的复杂大分子。酶是特殊的,在温和的...
- 发布于 2021-06-29 11:13
- 阅读 ( 555 )