钠原子与钠离子
元素周期表中的元素除了惰性气体外是不稳定的。因此,要想获得与其他惰性元素反应稳定的稀有元素。同样地,钠也必须得到一个电子来实现惰性气体氖的电子组态。所有非金属与钠反应生成钠离子。钠原子和钠离子由于一个电子的变化而具有不同的物理化学性质。
钠原子
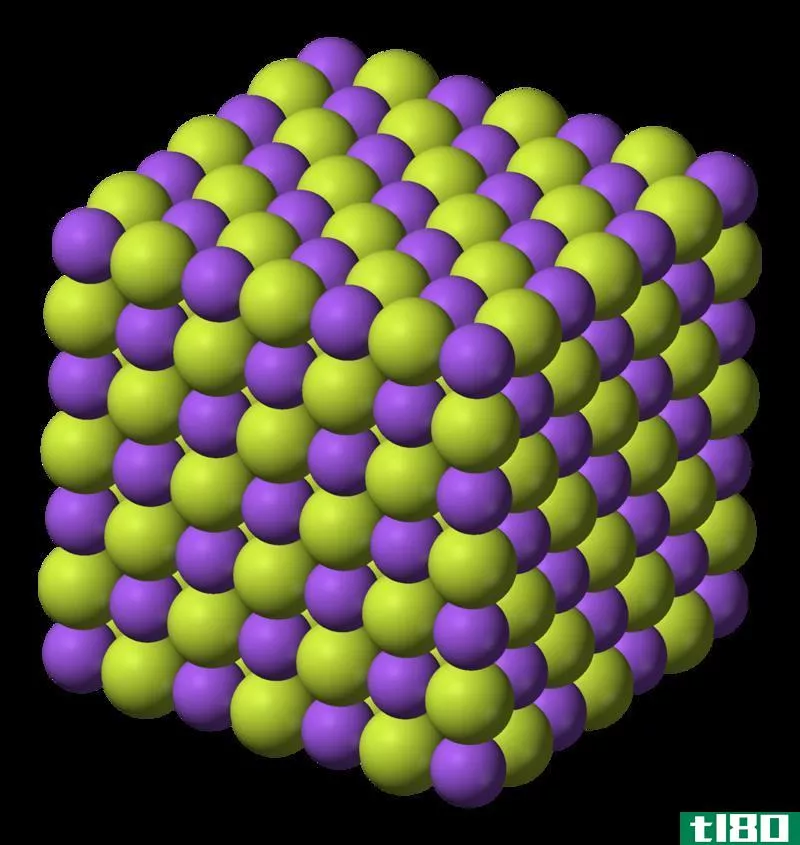
钠是原子序数为11的第1族元素。钠具有1类金属的特性。它的原子量是22.989。它的电子构型是1s2 2s2 2p6 3s1。钠是第三周期的第一个元素,所以电子已经开始填充到轨道3中。钠以银色固体存在。但是当钠暴露在空气中时,它与氧气反应非常迅速,从而使氧化膜呈现暗淡的颜色。钠足够软,可以用刀切割,一旦切割,银色的颜色就会因为氧化层的形成而消失。钠的密度比水低,所以它在剧烈反应的同时漂浮在水中。钠在空气中燃烧时发出明亮的黄色火焰。钠的沸点是883℃,熔点是97.72℃,钠有许多同位素。其中以Na-23最为丰富,相对丰度在99%左右。钠是生命系统中维持渗透平衡、神经冲动传递等必不可少的元素。钠还可用于合成其他各种化学品、有机化合物、肥皂和钠蒸气灯。
钠离子
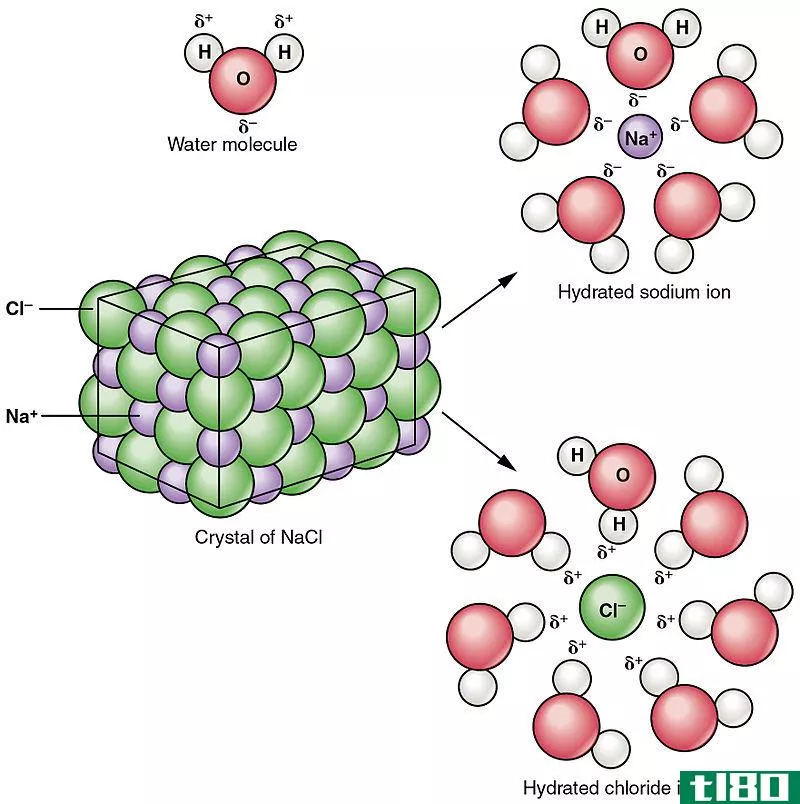
当钠原子释放其价电子给另一个原子时,它形成一个单价(+1)阳离子。它的电子配置为1s2 2s2 2p6,与氖的电子配置类似。从中移除电子很困难;因此,电离能非常高(4562 kJ·mol−1)。钠的电负性非常低(根据鲍林的标度,它大约为0.93),它可以通过向一个更高的负电原子(如卤素)提供一个电子来形成阳离子。因此,钠常生成离子化合物。
| 钠原子和钠离子的区别是什么?•钠离子通过从钠原子发出一个电子而获得稳定的电子构型。因此,钠离子比钠离子少一个电子。换句话说,钠原子的价壳层/最后一层只有一个电子。但是在钠离子中,最后一层有8个电子。•钠离子带+1电荷,而钠原子是中性的。•钠原子非常活泼,因此,在自然界中不会发现是游离的。它以钠离子的形式存在于化合物中。•由于释放了一个电子,钠离子半径与原子半径不同。•钠离子被吸引到带负电荷的电极上,但钠原子没有。•与钠离子+1离子的电离能相比,钠原子的第一电离能非常低 |