原子轨道与混合轨道
在薛定谔、海森堡和保罗·迪亚克提出的新理论中,人们以一种新的方式来理解分子中的键合。量子力学随着他们的发现而出现。他们发现电子具有粒子和波的特性。基于此,薛定谔发展了方程来发现电子的波动性质,并提出了波动方程和波函数。波函数(Ψ)对应于电子的不同状态。
原子轨道
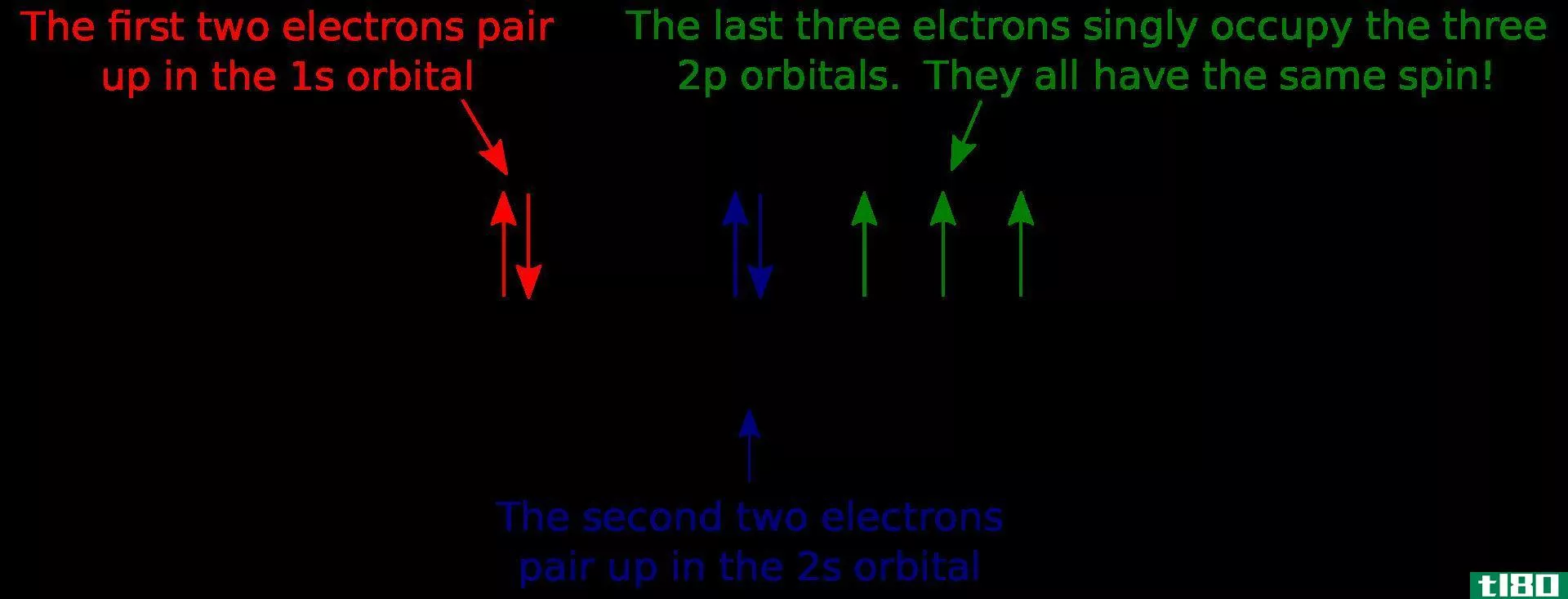
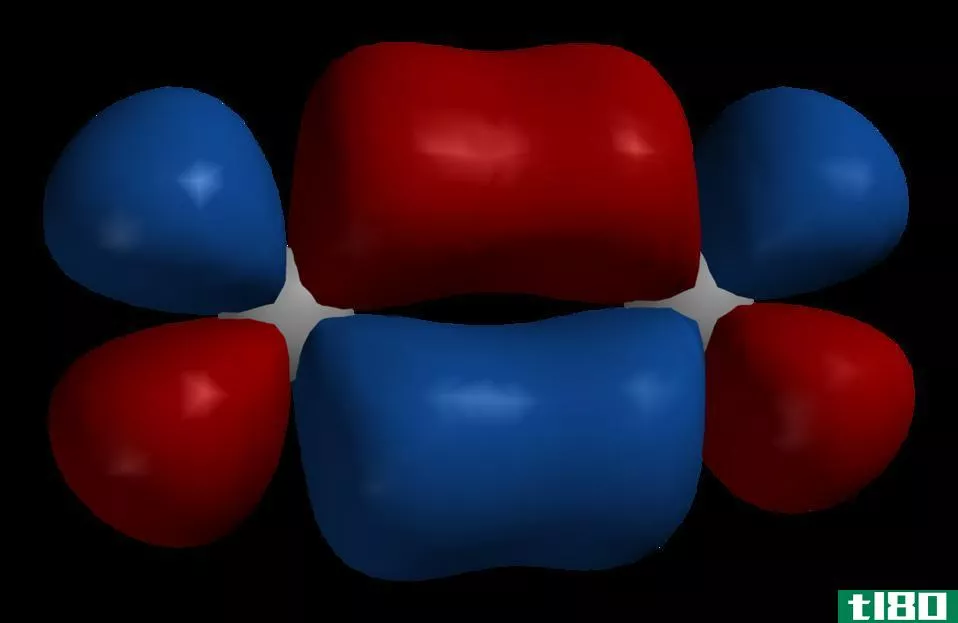
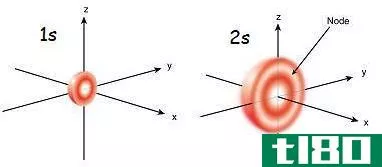
薛定谔提出这一理论后,马克斯·伯恩指出了波函数(Ψ2)平方的物理意义。根据Born的说法,Ψ2表示在特定位置找到电子的概率。所以,如果ψ2值较大,那么在这个空间中找到电子的概率就更高。因此,在空间中,电子的概率密度很大。相反,如果Ψ2很低,那么那里的电子概率密度就低。ψ2在x,y,z轴上的曲线图显示了这些概率,它们呈现s,p,d和f轨道的形状。这些被称为原子轨道。原子轨道可以定义为,在一个原子中找到电子的概率很大的空间区域。原子轨道以量子数为特征,每个原子轨道可以容纳两个自旋相反的电子。例如,当我们写电子组态时,我们写为1s2,2s2,2p6,3s2。1,2,3….n整数值是量子数。轨道名称后面的上标数字表示该轨道中的电子数。s轨道是球形的,而且很小。P轨道为哑铃形,有两个瓣。一个瓣是正的,另一个瓣是负的。两个叶瓣互相接触的地方称为节点。有3个p轨道,如x,y和z,它们排列在空间中,因此它们的轴相互垂直。有5个d轨道和7个f轨道,形状不同。总而言之,下面是一个轨道上可以存在的电子总数。
s-2轨道电子
P轨道-6个电子
d轨道-10个电子
f轨道-14个电子
混合轨道
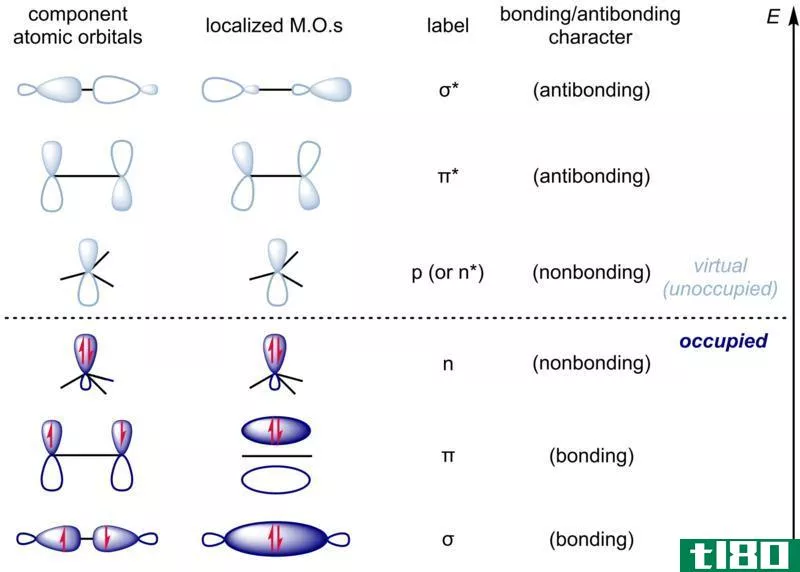
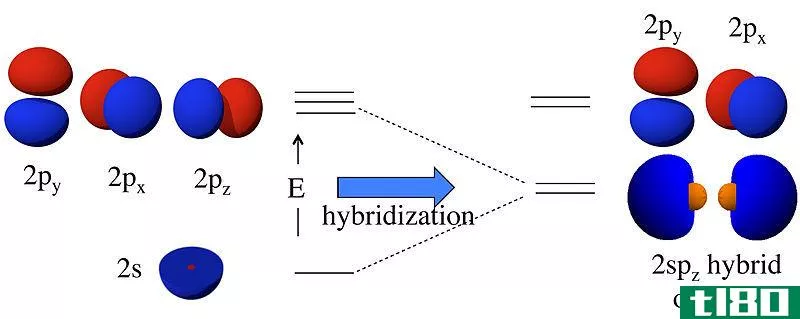
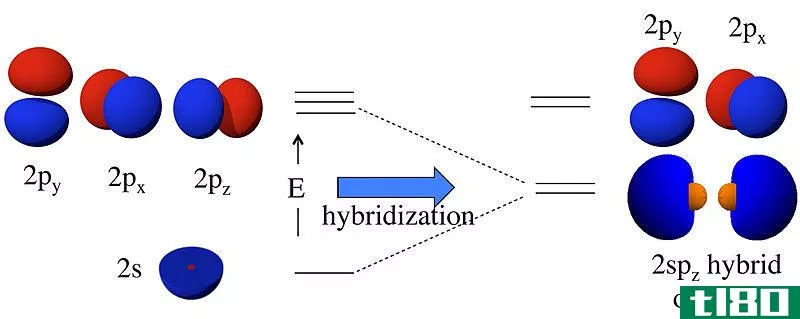
杂化是两个非等效原子轨道的混合。杂交的结果是杂交轨道。由s,p,d轨道混合而成的杂化轨道有很多种。最常见的杂化轨道是sp3,sp2和sp。例如,在CH4中,C有6个电子,电子组态为1s2 2s2 2p2,处于基态。当激发时,2s能级中的一个电子移动到2p能级,产生三个3个电子。然后2s电子和三个2p电子混合在一起,形成四个等效的sp3杂化轨道。同样,在sp2杂交中形成三个杂交轨道,在sp杂交中形成两个杂交轨道。产生的杂化轨道数目等于杂化轨道的总和。
| 原子轨道和杂化轨道有什么区别?•杂化轨道由原子轨道构成。•不同类型和数量的原子轨道参与形成混合轨道。•不同的原子轨道具有不同的电子形状和数量。但是所有杂化轨道都是等价的,并且具有相同的电子数。•杂化轨道通常参与共价sigma键的形成,而原子轨道参与sigma键和pi键的形成。 |