主要区别
原子轨道和分子轨道的主要区别在于,原子轨道包含受一个正原子核影响的电子,而分子轨道则包含受两个以上原子核影响的电子,这取决于分子中原子的数量。
原子轨道(atomic orbital) vs. 分子轨道(molecular orbital)
原子轨道被认为是原子中最有可能找到电子的区域。相反,分子轨道被认为是最有可能找到一个分子的电子的区域。原子周围的电子云负责产生原子轨道,而由相对相同能量组成的原子轨道的聚变则负责产生分子轨道。
原子轨道的类型如s、p、d或f决定了原子轨道的形状;另一方面,组成分子的原子轨道的形状决定了分子轨道的形状。薛定谔方程用于原子轨道,而在分子轨道中,通常使用原子轨道的线性组合。
原子轨道上的电子云受单个原子核的影响,而分子轨道上的电子云受两个或多个原子核的影响。原子轨道是单中心的,因为它位于单个原子核附近,而分子轨道被称为多中心轨道,因为它位于两个或多个不同的原子核附近。
分子轨道由两种分子轨道组成。原子轨道上的电子构型不影响原子的恒定性,而分子轨道上的电子构型则影响分子的稳定性。
比较图
什么是原子轨道(atomic orbital)?
这个区域是原子轨道,它包含了找到电子的最高可能性。原子电子位置的可能性可以用量子力学来解释。但是量子力学不能解释一个电子在一定时间内的特定能量。这种特殊的能量可以用海森堡的不确定原理来解释。
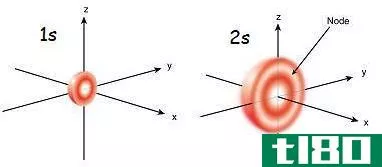
薛定谔方程的解被用来计算给定原子的电子密度。在一个原子轨道上最多可以有两个电子。原子轨道按子级分为s、p、d和f。这些子级的轨道有不同的形状。
次能级s轨道是球形的,最多包含两个电子,只有一个子能级。p轨道的形状是一个哑铃,包含多达六个电子。它有三个亚能量阶段。
d轨道和f轨道包含更多的复合形状,因为d轨道包含5个亚能级,并且由多达10个电子组成。而f轨道包含7个亚能级,最多有10到15个电子。轨道的能级方向是s<p<d<f。
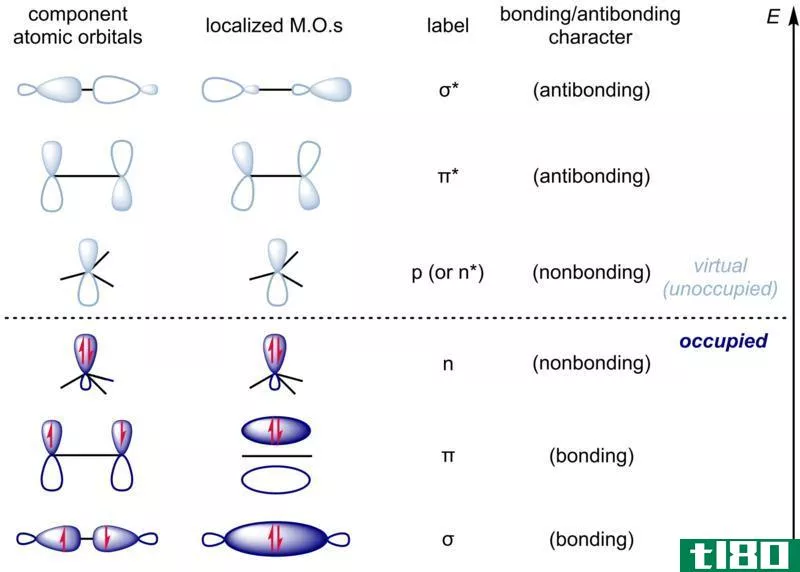
什么是分子轨道(molecular orbital)?
分子轨道理论解释了分子轨道的性质。分子轨道理论最早由F.Hund和R.S.Mulliken于1932年提出。
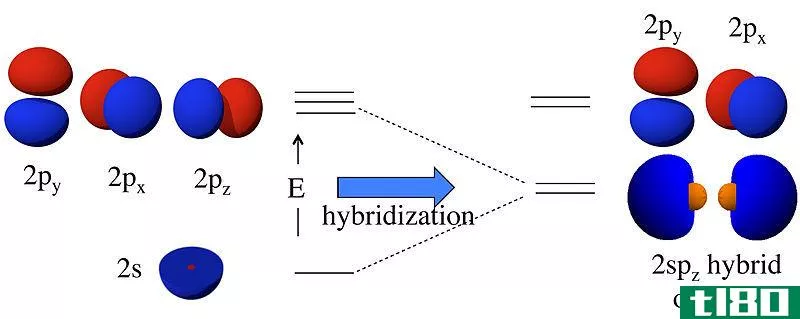
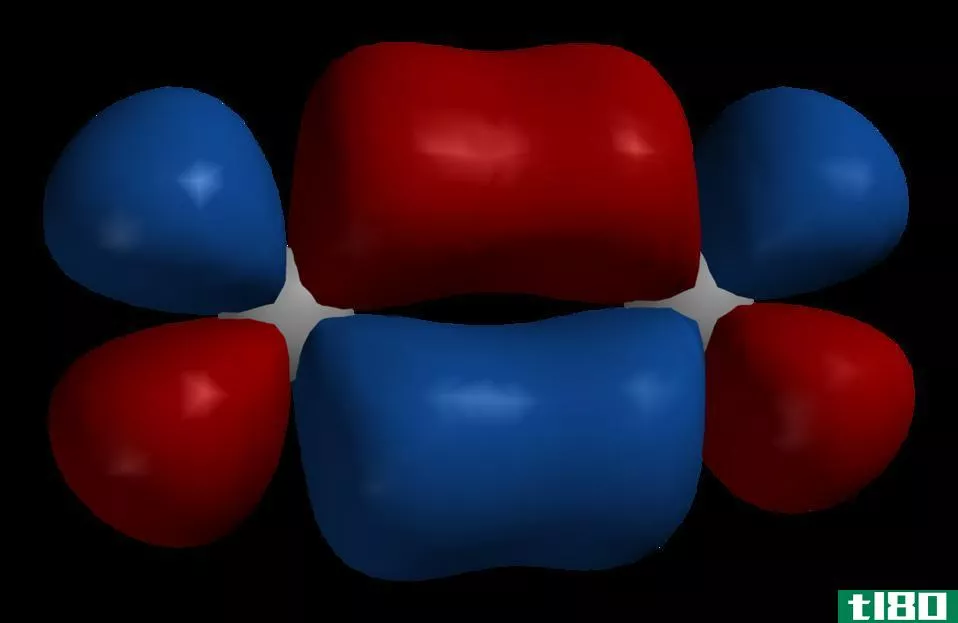
根据分子轨道理论,当原子连接在一起形成一个分子时,由于原子核的影响,重叠的原子轨道通常会失去形状。分子中出现的新轨道现在称为分子轨道。
由相对相同能量组成的原子轨道的聚变是产生分子轨道的原因。分子轨道不象原子轨道那样只属于一个分子中的一个原子,但它适合于构成分子的所有原子的原子核。所以,许多不同原子的原子核都是多中心的。
分子轨道的最终形状是复杂的,因为构成分子的原子轨道的形状通常决定了分子轨道的形状。根据Aufbau规则,分子轨道一般按低能轨道向高能轨道填充。
主要区别
- 原子轨道中的电子通常只受一个正原子核的影响;另一方面,分子轨道中的电子受两个或多个原子核的影响,而原子核的数目取决于分子中原子的数量。
- 原子轨道由简单的形状组成,如s、p、d和f决定原子轨道的形状;相反,分子轨道由复杂形状组成,因为构成分子的原子轨道的形状通常决定分子轨道的形状。
- 原子轨道存在于单个原子核周围,因此被称为单中心轨道,而分子轨道则存在于许多不同的原子核周围,因此被称为多中心轨道。
- 在原子轨道上,单个原子核通常影响电子云;相反,在分子轨道上,两个或两个以上的原子核影响电子云。
- 原子轨道上的电子密度可以用薛定谔方程来描述。相比之下,分子轨道中的电子密度通常可以用原子轨道的线性组合(LCAO)来描述。
结论
以上讨论得出结论:原子轨道的性质可以由原子的单个原子核决定。相比之下,分子轨道的性质可以通过原子轨道的融合来确定,而原子轨道的聚变构成了分子。