单原子和双原子的关键区别在于单原子物种有一个原子,而双原子物种有两个原子。
因此,单原子和双原子的区别主要在于物种中存在的原子。顾名思义,这两个术语都代表了原子结合的不同状态,其中“mono”表示“1”,“di”表示“2”。因此,简单地说,monatomic意味着一个“一个原子”,双原子意味着“两个原子”
目录
1. 主要区别和主要概述
2. 什么是单原子
3.什么是双原子
4. 并列比较-单原子与双原子的表格形式
5. 摘要
什么是单原子(monatomic)?
当单个原子独立存在时(这种情况很少发生),我们称之为单原子。也就是说,这些元素是纯单数形式。然而,唯一可能属于这一类别的实际例子是稀有气体,它们以原子的形式存在,因为它们的外壳上有一个完整的八位电子。因此,它们不希望为了更稳定而接受或捐赠更多的电子。因此,稀有气体是稳定的单原子形式。一些例子是:氦-氦,氖-氖,氩-氩,氙-氙,氪-氪,氡-氡。

图01:单原子意味着有单个原子
此外,还存在以离子形式存在的单个原子,特别是在溶液中,例如:Na+、Ca2+、K+等。这些离子上有固定电荷,意味着它们具有恒定的价态。但是,还有其他类型的离子,它们有许多价态,可以以多种离子形式存在,仍然是单原子的。一个很好的例子是铁;Fe2+和Fe3+。因此,不仅阳离子(带正电荷)而且阴离子(带负电)也以单原子形式存在;Cl-、F-、I-是以单原子形式存在的少数例子。这些离子物种本身并不稳定,自然会寻找对应物来形成化合物。
但是,如上所述,我们可以在其化合物水解的溶液中找到它们。离子物种的形成是由于单一原子在纯态中缺乏稳定性,无法获得稀有气体的电子组态。因此,这些原子要么接受电子,要么捐赠电子以获得稳定性。
什么是双原子(diatomic)?
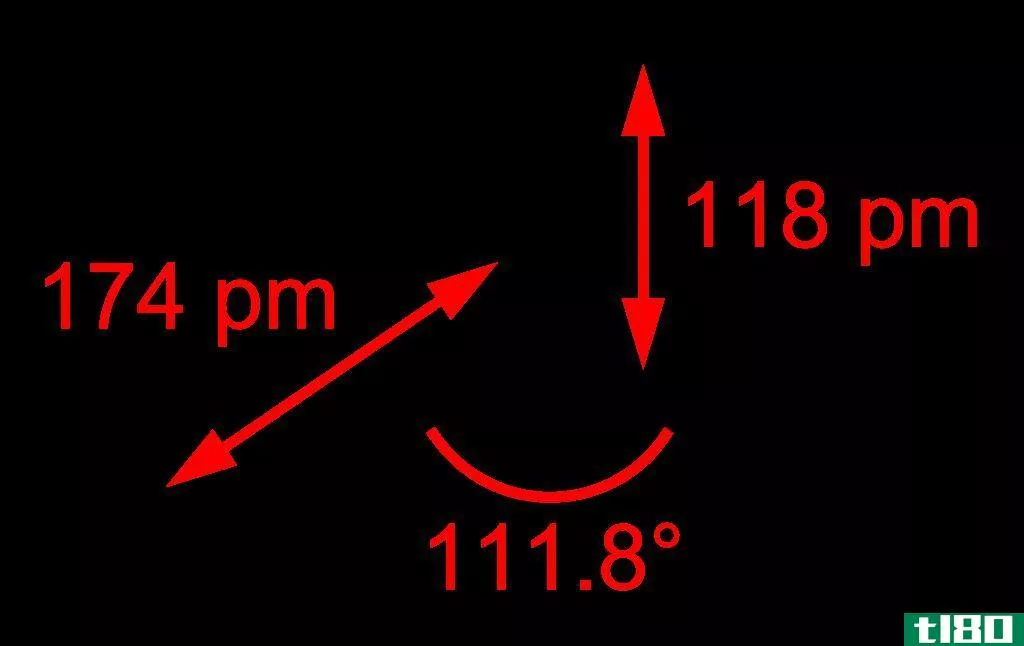
当两个原子相互结合时,我们称之为双原子。不同类型的原子可能会出现。当它们是两个相似的结合原子时,我们称之为“同核硅藻”,如果它们由不同类型的原子组成,我们称之为“异核硅藻”。一些同核硅藻的例子是O2、N2、H2等,而CO、NO、HCl等可以作为异核硅藻的例子。
图02:双原子意味着有两个原子
我们可以把硅藻看作化合物,因为它们形成了这些缔合物,以便通过彼此共享电子来获得更大的稳定性,从而使两个原子都获得惰性气体电子构型。它们可以通过原子轨道的重叠通过共价键结合,或者在它们之间形成离子键,这是阳离子(带正电)物种和阴离子(带负电)物种之间的吸引力。硅藻间共价键的例子包括CO,NO等,我们认为HCl是一种具有离子吸引特性的物种。然而,由于H+和Cl-之间的吸引力不是很强,这不是一个很好的例子,离子键是另一个定义的主题。
单原子(monatomic)和双原子(diatomic)的区别
术语“单原子”指的是一个原子的存在,而术语“双原子”是指存在两个相互关联的原子。因此,单原子和双原子的关键区别在于单原子物种有一个原子,而双原子物种有两个原子。此外,单原子和双原子的另一个区别是,除稀有气体外,单原子物种通常不稳定,而双原子物种通常是稳定的,因为两个原子之间存在化学键,形成了围绕每个原子的电子八位体。
下面的信息图以表格形式显示了单原子和双原子的区别。

总结 - 单原子(monatomic) vs. 双原子(diatomic)
单原子和双原子这两个术语描述了一种化学物质中存在的原子数。因此,单原子和双原子的关键区别在于单原子物种有一个原子,而双原子物种有两个原子。
引用
1“单原子气体”,维基百科,维基媒体基金会,2018年9月17日。此处提供