三角平面vs三角锥体
三角平面和三角金字塔是我们用来命名原子在空间中的三维排列的两种几何结构。还有其他类型的几何图形。线性,弯曲,四面体,八面体是一些常见的几何体。原子以这种方式排列,以使键-键排斥、键孤对排斥和孤对排斥最小化。具有相同原子数和电子孤对的分子倾向于容纳相同的几何结构。因此,我们可以通过考虑一些规则来确定分子的几何结构。VSEPR理论是一种利用价电子对数来预测分子几何结构的模型。实验上可以用各种光谱法和衍射法观察分子的几何结构。
三角平面
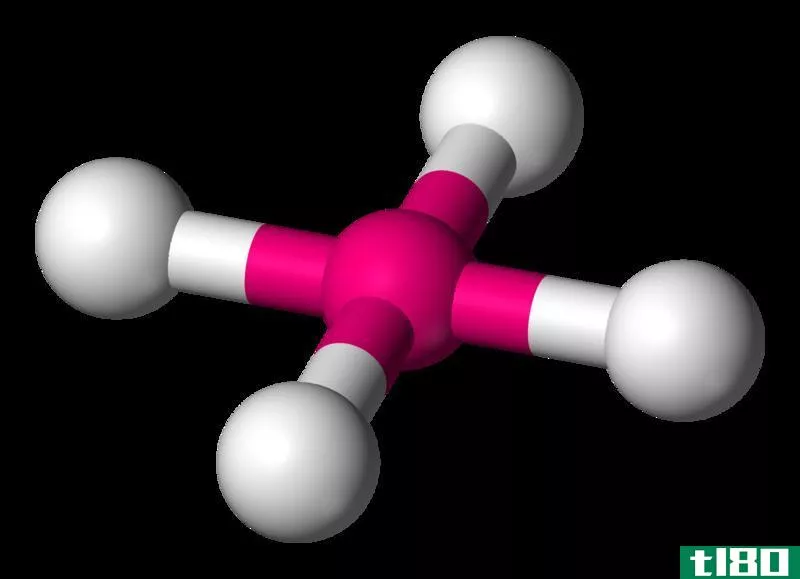
三角平面几何是由含有四个原子的分子表示的。有一个中心原子,其他三个原子(外围原子)以三角形的角与中心原子相连。中心原子中不存在孤立对,因此,在确定几何结构时只考虑中心原子周围基团的键-键排斥作用。所有的原子都在一个平面上,因此,这个几何体被称为“平面”。一个具有理想三角形平面几何结构的分子,其外围原子之间的夹角为120度。这样的分子会有相同类型的外围原子。三氟化硼(BF3)就是具有这种几何结构的理想分子的一个例子。此外,还有一些分子具有不同类型的外围原子。例如,可以采用COCl2。在这种分子中,根据原子的类型,角度可能与理想值略有不同。此外,碳酸盐和硫酸盐是两种无机阴离子,显示出这种几何形状。除了处于外围位置的原子,在三角平面几何中,中心原子周围可能有配体或其他复杂基团。C(NH2)3+是这种化合物的一个例子,其中三个NH2基团与一个中心碳原子结合。
三角锥体
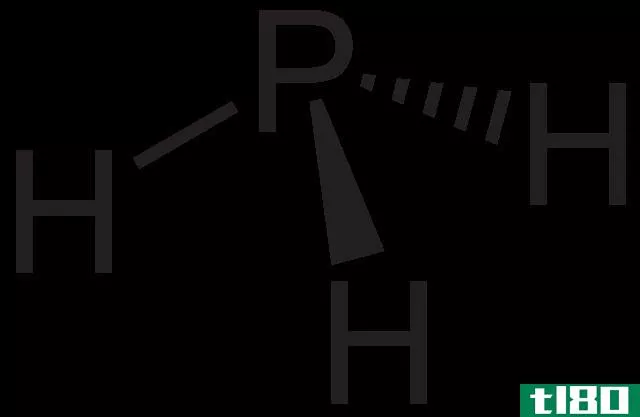
三角锥的几何结构也表现为分子有四个原子或配体。中心原子在顶点,另外三个原子或配体在一个基部,在三角形的三个角上。在中心原子中有一对孤电子。通过将三角平面几何可视化为四面体几何,很容易理解。在这种情况下,所有的三个键和孤对都在四面体形状的四个轴上。因此,当孤立对的位置被忽略时,剩下的键形成三角金字塔几何。由于孤子对键的斥力大于键-键的斥力,键合的三个原子和孤对之间的距离将尽可能远。原子之间的夹角将小于四面体的角度(109o)。典型的三角棱锥的角度大约是107o。氨,氯酸盐离子和亚硫酸盐离子是显示这种几何形状的一些例子。
| 三角平面和三角金字塔有什么区别?•在三角平面中,中心原子中没有孤对电子。但在三角锥中,中心原子有一对孤对。•三角平面中的键角约为120°,而三角锥体中的键角约为107°。•在三角平面中,所有原子都在一个平面上,但在三角锥体中,它们不在一个平面内。•在三角平面中,只有键-键排斥。但在三角锥体中有键-键和键-孤对排斥。 |