饱和溶液与不饱和溶液
饱和一词在化学的各个分支中有不同的定义。而在物理化学中,饱和的概念不同于有机化学中对饱和的看法。然而,saturation这个词来自拉丁语,字面意思是“填充”。因此,饱和的基本思想是填满总容量,而不饱和意味着还有更多的空间来填充整个容量。
什么是饱和溶液?
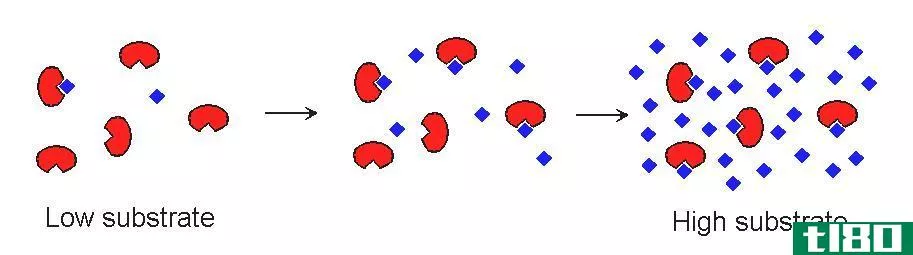
溶液是由溶质溶解在溶剂中制成的。由此产生的混合物就是我们所说的溶液。在任何给定的温度和压力下,溶解在特定溶剂中的溶质量是有限度的,以便溶质在溶液相中保持溶解。这个极限被称为饱和点。在试图溶解超过饱和点的更多溶质时,多余的溶质会在底部形成沉淀物,将自身分离成固相。这是为了保持溶液在给定温度和压力下所能保持的溶质极限。
因此,任何达到饱和点的溶液都称为“饱和溶液”。原则上,饱和溶液有两种类型:完全饱和和接近饱和。当它完全饱和时,由于溶质不能在溶剂中进一步溶解,我们通常会看到在底部形成沉淀。而当溶液接近饱和时,溶液中几乎含有饱和所需的准确数量的溶质;因此,一点点添加的溶质会在底部形成少量沉淀。因此,当溶液接近饱和时,即使我们认为它是饱和溶液,我们也不会在底部看到沉淀。一定量溶液的饱和点随温度和压力而变化。在较高的温度下,相同体积的溶剂能够在溶液相中容纳更多的溶质。因此,温度越高,饱和所需的溶质量就越大。相比之下,当压力增加时,很容易达到饱和。
当溶质溶解在溶剂中时,必须定期混合。这样做是为了避免局部过饱和(通过饱和点的少量溶剂)。因此,溶质必须均匀地分布在整个体积上,不应在同一个地方滴下。
什么是不饱和溶液?
不饱和溶液是具有溶解更多溶质的能力的溶液。这些溶液还没有超过饱和点,因此在底部永远不会有沉淀。如上所述,不饱和溶液和接近饱和溶液,从外观上看几乎相似,但通过快速步骤可以很容易地区分它们。也就是说,当一小部分溶质分子溶解时,接近饱和的溶液会迅速形成沉淀,而对于不饱和溶液,由于溶质在溶液相中有足够的空间容纳它们,所以在外观上没有差别,因为溶质会完全溶解。
一般来说,在较低温度下饱和的溶液,在较高的温度下会变得不饱和,因为温度的升高增加了溶液相中溶质的承载能力。
饱和溶液和不饱和溶液的区别是什么?
•饱和溶液不能在溶液相进一步溶解溶质,而不饱和溶液可以。
•通常,饱和溶液在底部带有沉淀物,但不饱和溶液不携带。