自由能与标准自由能
什么是自由能?
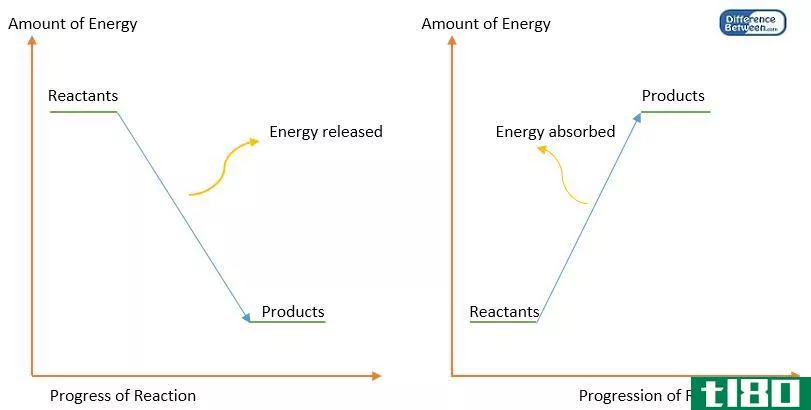
一个热力学系统所能做的功的量被称为自由能。自由能可以用两个术语来描述,亥姆霍兹自由能和吉布斯自由能。在化学中,当我们用“自由能”这个词时,意思是吉布斯自由能。在物理学中,自由能是指亥姆霍兹自由能。这两个术语如下所述。
热力学第二定律与熵有关,它说:“宇宙的熵在自发过程中增加。”熵与产生的热量有关,也就是能量退化的程度。但是,事实上,由一定量的热量q引起的额外无序程度取决于温度。如果它已经很热了,一点额外的热量不会造成更多的混乱,但是如果温度很低,同样的热量会导致无序的急剧增加。因此,写,
ds=dq/T
要分析变化的方向,我们必须考虑系统和周围环境的变化。下面的克劳修斯不等式说明了当热能在系统和周围环境之间传递时会发生什么。(考虑系统在温度T下与周围环境处于热平衡状态)
dS–dq/T≥0…………(1)
如果加热是在恒定的体积下进行的,我们可以把上面的方程(1)写如下。这个方程仅用状态函数表示自发反应发生的判据。
dS–dU/T≥0
这个方程可以重新排列得到下面的方程。
TdS≥dU(方程式2),因此,可以将其写为
dU–TdS≤0
上述表达式可以通过使用术语Helmholtz energy,A来简化,可以定义为,
A=U-TS
从上述方程中,我们可以导出一个自发反应的判据,即dA≤0。这说明,当dA≤0时,系统在恒定温度和体积下的变化是自发的。所以当它对应于亥姆霍兹能量的减少时,变化是自发的。因此,这些系统以自发的方式运动,给出较低的值。
吉布斯自由能与恒压下发生的变化有关。当热能在恒压下传递时,只有膨胀功;因此,我们将方程2修改为:。
TdS≥dH
该方程可重新排列,使dH TdS≤0。用吉布斯自由能G,这个方程可以写成,
G=H-TS
在恒定的温度和压力下,化学反应是自发的,在降低吉布斯自由能的方向上。因此,dG≤0
什么是标准自由能?
标准自由能是指标准条件下定义的自由能。标准条件为温度298K;压力,1 atm或101.3 kPa;以及1m浓度下的所有溶质。标准自由能表示为Go。
| 自由能和标准自由能有什么区别?•在化学中,自由能指吉布斯自由能。它与恒压下发生的变化有关。标准自由能是在标准条件下定义的自由能。•因此,标准自由能在298K温度和1 atm压力下给出,但自由能值会随温度和压力而变化。 |