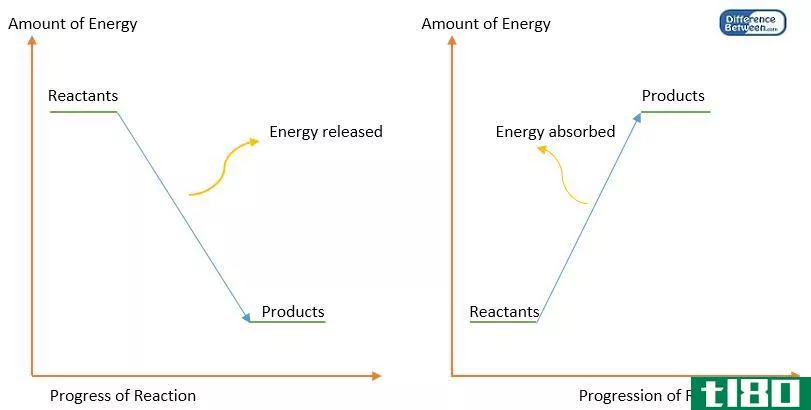
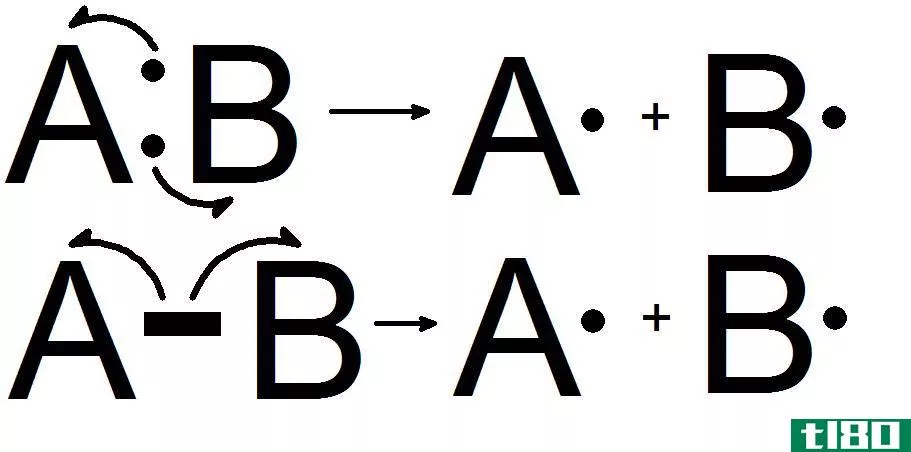关键区别-均裂和异溶键离解能
键离解能是化学键强度的量度。键可以以均裂方式或异溶方式解离。键离解能是指化学键经均裂而发生的标准焓变。均溶键离解能是通过溶血分解化学键所需的能量,而异溶键离解能是通过异构化裂解化学键所需的能量量。同一化合物的均裂键离解能值与异裂键离解能值不同。这是均裂键和异溶键离解能的关键区别。
目录
1. 概述和主要区别
2. 什么是均裂键离解能
3. 什么是异溶键离解能
4. 并列比较-均裂和异溶键解离能的表格形式
5. 摘要
什么是均裂键离解能(homolytic bond dissociation energy)?
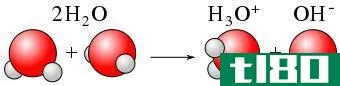
均溶键离解能是通过溶血分解化学键所需的能量。化学键的溶血是键的对称断裂,形成两个自由基,而不是两个离子。在这里,原子间的键电子被分成两半,由两个原子占据。例如,每一个不裂解的自由基都有一个不裂解的自由基。
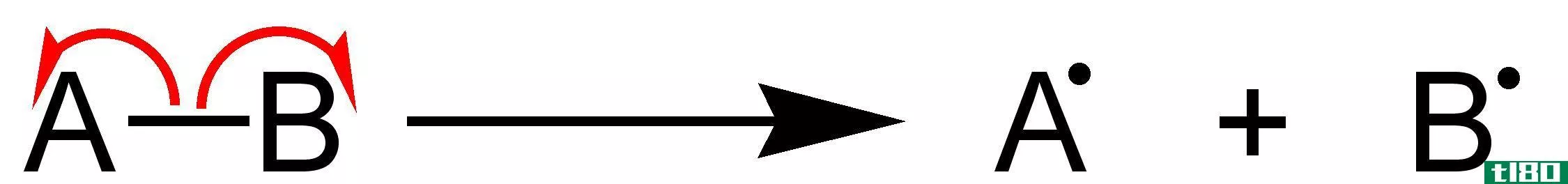
图1:均分解
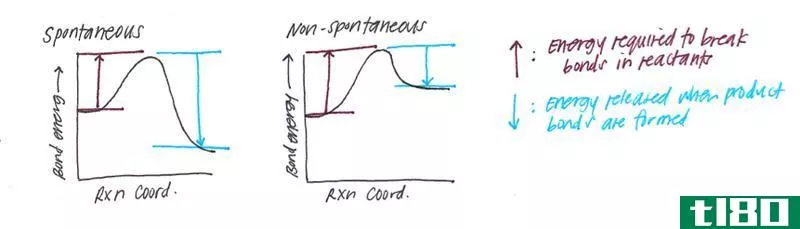
键离解能是指在标准条件下,通过溶血来裂解化学键所需的能量。均裂键离解能决定了化学键的强弱。如果均裂键离解能值较高,则说明需要提供大量能量来裂解该键;因此,它是一个强键。
什么是异溶键离解能(heterolytic bond dissociation energy)?
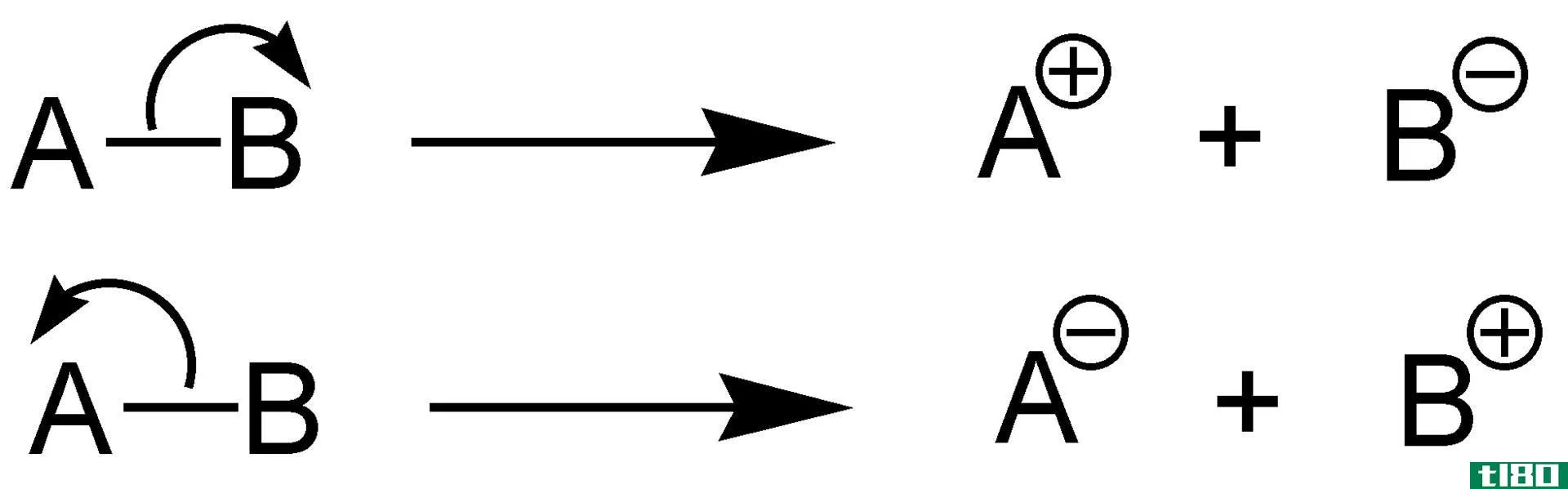
异构化键离解能是通过异构化裂解化学键所需的能量。异构化是化学键以不对称的方式断裂。异构化形成阳离子和阴离子。这是因为,在杂化反应中,键-电子对被电负原子(它被转换成负离子)占据,而另一个原子不带电子(它形成阳离子)。
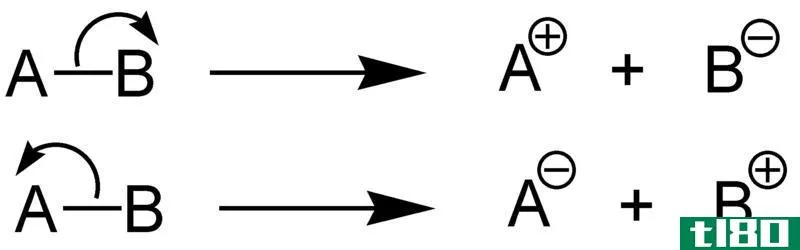
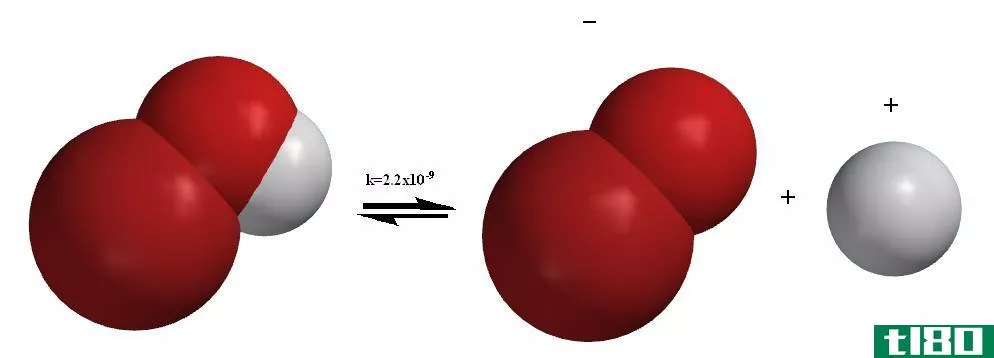
图2:化学键的异构化分解
当同一分子的均分解相比时,同一分子的异分解与均分解的值不同。这意味着化合物的均裂键离解能不同于同一分子的异溶键离解能。
例:让我们考虑氢分子中H-H键的断裂。
均裂键离解:H2→H●+H●(键离解能为104 kcal/mol)
异溶键离解:H2→H++H–(键离解能为66 kcal/mol)
均裂的(homolytic)和异溶键离解能(heterolytic bond dissociation energy)的区别
| 均裂与异裂键离解能 | |
| 均溶键离解能是通过溶血分解化学键所需的能量。 | 异构化键离解能是通过异构化裂解化学键所需的能量。 |
| 产品 | |
| 均裂键离解能与化学键断裂形成自由基有关。 | 异溶键离解能与化学键断裂形成阳离子和阴离子有关。 |
总结 - 均裂的(homolytic) vs. 异溶键离解能(heterolytic bond dissociation energy)
键解离能是指在标准条件下,通过均分解来裂解化学键所需的能量。键裂解有两种类型:均溶和异分解。均溶键裂解形成自由基,而杂化键裂解形成阳离子和阴离子。均溶键解离能与异溶键解离能的关键区别在于,同一化合物的均溶键解离能值与异溶键解离能值不同。
引用
1“键离解能量”,维基百科,维基媒体基金会,2018年2月28日,可在这里查阅。“异源分解(化学)。”维基百科,维基媒体基金会,2018年2月19日,可在这里查阅。“键离解能=均裂。”有机化学硕士RSS,可在这里找到。
2“异源分解(化学)。”维基百科,维基媒体基金会,2018年2月19日,
三。“键离解能=均裂。”有机化学硕士RSS,