反键轨道定义
反键轨道是在两个原子核之间区域外含有电子的分子轨道。

当两个原子彼此接近时,它们的电子轨道开始重叠。这种重叠在两个原子之间形成了一个分子键,具有自己的分子轨道形状。这些轨道与原子轨道一样遵循泡利不相容原理。一个轨道上的两个电子不可能有相同的量子态。如果原始原子中含有电子,其中一个键会违反规则,则该电子将填充高能反键轨道。
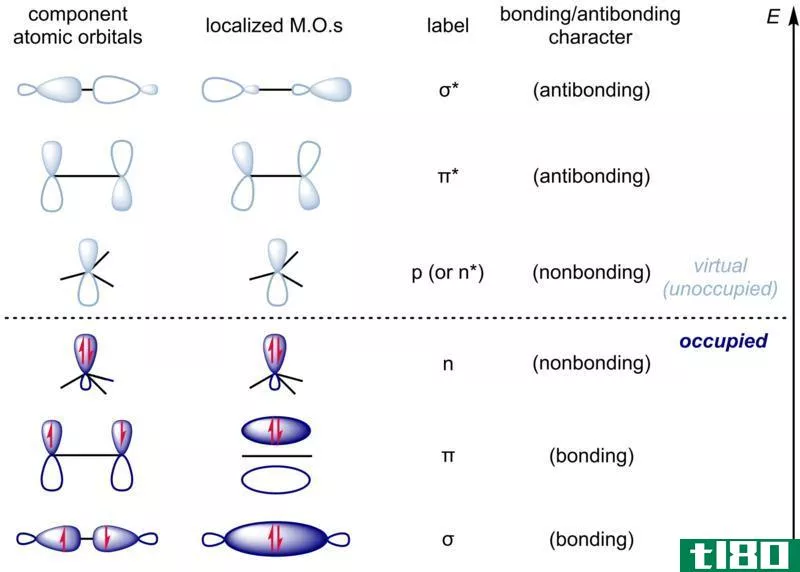
反键轨道在相关分子轨道类型旁边用星号表示。σ*是与σ轨道相关联的反键轨道,π*轨道是反键π轨道。当谈到这些轨道时,经常在轨道名称的末尾加上“星”一词:σ*=σ星。
例子
H2-是一种含有三个电子的双原子分子。其中一个电子位于反键轨道。
氢原子只有一个1s电子。1s轨道有两个电子的空间,一个自旋“向上”电子和一个自旋“向下”电子。如果一个氢原子包含一个额外的电子,形成一个H-离子,则1s轨道被填满。
如果一个氢原子和氢离子彼此接近,两个原子之间就会形成一个西格玛键。每个原子将贡献一个电子来填充低能σ键。额外的电子将填充更高的能量状态,以避免与其他两个电子相互作用。这个高能轨道叫做反键轨道。在这种情况下,轨道是σ*反键轨道。
来源
- 阿特金斯。;de Paula J.(2006年)。阿特金斯物理化学(第8版)。弗里曼。国际标准书号:0-7167-8759-8。
- 奥钦,M。;谢菲,H.H.(1967年)。反键轨道的重要性。霍顿·米夫林。ISBN:B0006BPT5O。
- 发表于 2021-09-15 16:44
- 阅读 ( 432 )
- 分类:化学
你可能感兴趣的文章
dπ-dπ键(dπ-dπ bond)和三角洲债券(delta bond)的区别
...成。 当考虑δ键的轨道对称性时,我们可以观察到它与π反键轨道的对称性不同。π反键轨道包含一个由核间轴组成的节面和另一个垂直于原子间轴的节面。 科学家罗伯特·穆利肯在1931年介绍了三角洲符号。他首先用化学化合物...
- 发布于 2020-09-16 00:02
- 阅读 ( 485 )
电子旋转(electronic rotational)和振动跃迁(vibrational transition)的区别
...一键的LUMO激发。同样地,π键轨道上的电子可以被激发到反键π轨道上。然而,分子的电子跃迁很大程度上取决于分析中使用的溶剂类型。 什么是旋转跃迁(rotational transition)? 分子的转动跃迁是指分子角动量的突变。这个定义是...
- 发布于 2020-09-19 13:27
- 阅读 ( 653 )
回粘超共轭(backbonding hyperconjugation)和共轭(conjugation)的区别
...。后结合是电子从一个原子上的原子轨道移动到配体上的反键π轨道,而超共轭是sigma键与π网络的相互作用,共轭是π轨道沿sigma键的重叠。 我们可以根据化合物中不同的化学键来讨论背键、超共轭和共轭。这三个术语都描述了...
- 发布于 2020-09-20 20:03
- 阅读 ( 413 )
背面粘合(back bonding)和配位键合(coordinate bonding)的区别
...关键区别在于,背键是指在一个原子的原子轨道和配体的反键轨道之间形成的化学键,而配位键是指在一个负电荷物种和一个缺电物种之间共享一对电子。 配位键通常出现在配位配合物中,中心金属原子被一组配体包围,配体...
- 发布于 2020-10-07 10:30
- 阅读 ( 677 )
多重性(multiplicity)和债券定单(bond order)的区别
...学键稳定性的指标。键序值越高,化学键越强。如果没有反键轨道,键序等于分子中两个原子间的键数。这是因为键序等于键电子数除以2(化学键每个键有两个电子)。计算特定分子中键级的方程如下: 键序=(成键电子数-反...
- 发布于 2020-10-13 16:56
- 阅读 ( 465 )
分子轨道理论(molecular orbital theory)和杂交理论(hybridization theory)的区别
...杂化理论的主要区别在于分子轨道理论描述了成键轨道和反键轨道的形成,而杂交理论描述了杂化轨道的形成。 有不同的理论发展来确定分子的电子结构和轨道结构。VSEPR理论、Lewis理论、价键理论、杂化理论和分子轨道理论是...
- 发布于 2020-10-15 22:50
- 阅读 ( 852 )
反键合(antibonding)和非键合(nonbonding)的区别
反键和非键的关键区别在于反键轨道增加了分子的能量,而非键轨道不会改变分子的能量。 反键和非键这两个术语都属于分子轨道理论。根据这个理论,这些轨道是由于其他轨道重叠而形成的混合轨道。 目录 1. 概述和主要...
- 发布于 2020-10-16 03:12
- 阅读 ( 1281 )
晶体场理论(crystal field theory)和配位场理论(ligand field theory)的区别
...网络相互作用产生了一组新的轨道,一个是键,另一个是反键。(一个*表示轨道是反键的。) 当没有净相互作用时,原子轨道和分子轨道不受影响,在金属-配体相互作用中,它们本质上是非键的。 键轨道和反键轨道具有sigma(...
- 发布于 2020-10-24 03:34
- 阅读 ( 764 )
分子轨道(molecular orbital)和原子轨道(atomic orbital)的区别
...分子轨道 此外,分子轨道有两种类型:成键分子轨道和反键分子轨道。成键分子轨道包含基态电子,而反键分子轨道不包含基态电子。此外,如果分子处于激发态,电子可能占据反键轨道。 什么是原子轨道(an atomic orbital)? 在...
- 发布于 2020-10-24 07:58
- 阅读 ( 574 )
结合(bonding)和反键分子轨道(antibonding molecular orbitals)的区别
成键与反键分子轨道 这两种分子轨道间的化学键可以用化学键和分子轨道键的不同来解释。键和反键分子轨道之间最显著的区别是它们相对于母原子轨道的能级。这种能级差异导致了两个分子轨道之间的其他差异。 成键和反...
- 发布于 2020-10-26 19:13
- 阅读 ( 659 )