科学中的p轨道定义
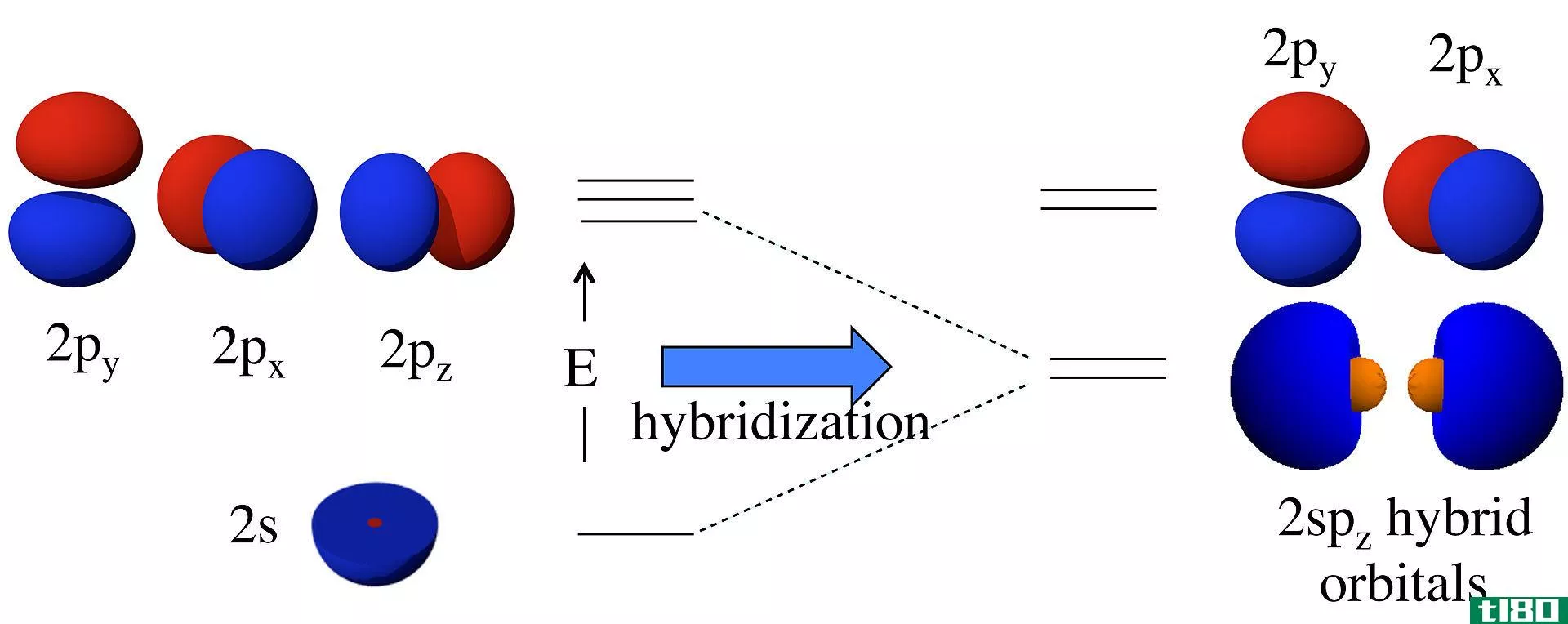
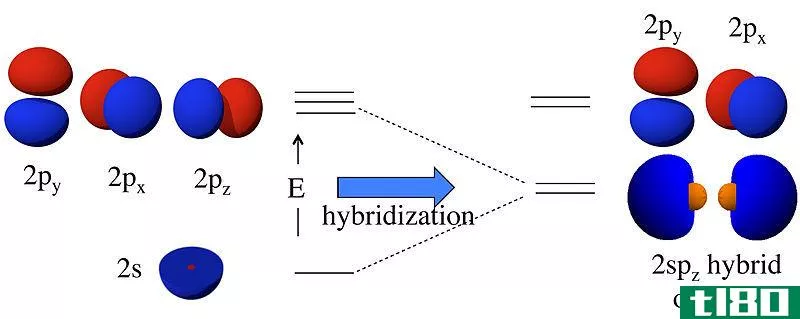
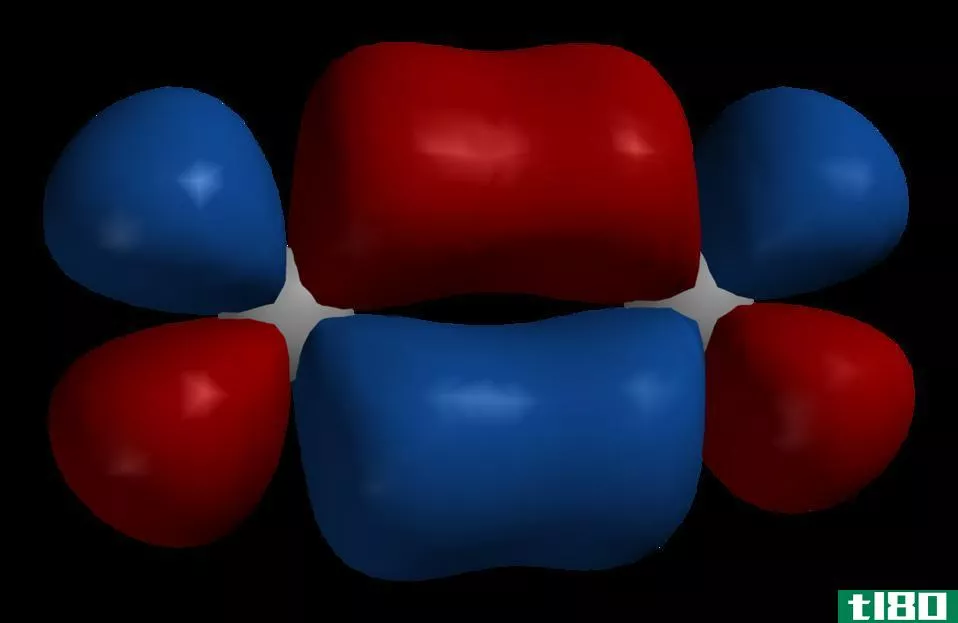
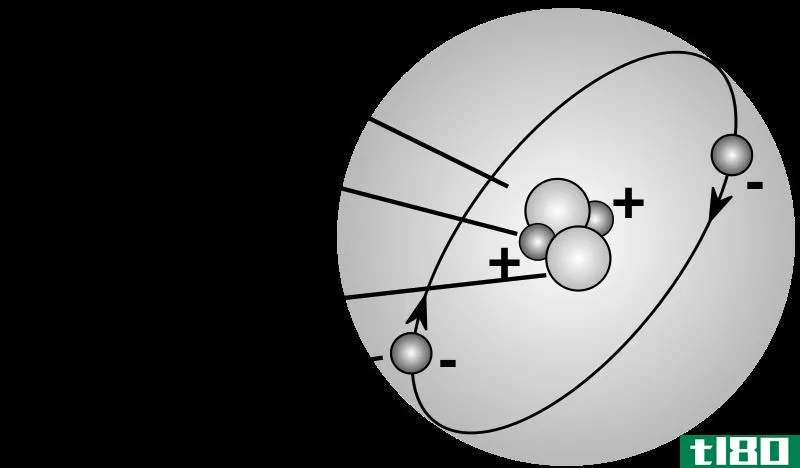
根据海森堡测不准原理,在任何给定的时刻,在离原子核的任何距离和任何方向都可以找到一个电子。p轨道是一个哑铃形或波瓣状区域,描述了在一定概率范围内可以找到电子的位置。哑铃的节点出现在原子核上,因此在原子核中找到电子的概率很低(但不是零)。轨道的形状取决于与能量状态相关的量子数。

所有p轨道的l=1,m有三个可能值(-1,0,+1)。当m=1或m=-1时,波函数是复的。
来源
- 格里菲斯,大卫(1995)。量子力学导论。普伦蒂斯大厅。第190-191页。ISBN 978-0-13-124405-4。
- 莱文,爱尔兰共和军(2000年)。量子化学(第5版)。普伦蒂斯大厅。第144-145页。ISBN 978-0-13-685512-5。
- 奥钦,弥尔顿;麦康伯,罗杰S。;品哈斯,艾伦;Wilson,R.Marshall(2005年)。原子轨道理论。
- 发表于 2021-09-21 14:35
- 阅读 ( 277 )
- 分类:化学
你可能感兴趣的文章
杂交(hybridization)和重叠(overlapping)的区别
...。 轨道是可以充满电子的假想结构。根据不同的发现,科学家们提出了这些轨道的不同形状。轨道主要有三种类型:原子轨道、分子轨道和杂化轨道。杂交轨道是通过杂交过程形成的。杂化和重叠是两个相关的化学概念。原子...
- 发布于 2020-10-15 21:29
- 阅读 ( 513 )
混合的(hybrid)和简并轨道(degenerate orbitals)的区别
...50%p轨道特性。 图01:Sp杂交 杂化的概念首先被讨论是因为科学家发现价键理论不能正确地预测某些分子如CH4的结构。虽然根据碳原子的电子构型,碳原子只有两个不成对的电子,但它可以形成四个共价键。为了形成四个键,必须...
- 发布于 2020-10-16 17:47
- 阅读 ( 908 )
分子轨道(molecular orbital)和原子轨道(atomic orbital)的区别
...·狄拉克提出的新理论,人们以一种新的方式来理解分子中的键合。当量子力学与他们的发现结合在一起时,人们发现电子既有粒子特性又有波特性。基于此,薛定谔发展了方程来发现电子的波动性质,并提出了波动方程和波函...
- 发布于 2020-10-24 07:58
- 阅读 ( 574 )
质子(proton)和电子(electron)的区别
...一种亚原子粒子,带正电荷。我们通常用p来表示它。当科学家发现电子时,他们对一种叫做质子的粒子一无所知。戈尔茨坦发现了一种由气体产生的带正电荷的粒子。这些被称为阳极射线。与电子不同的是,根据所用气体的不...
- 发布于 2020-10-24 20:27
- 阅读 ( 563 )
键对(bond pair)和孤独的一对(lone pair)的区别
...和孤对两种类型。键对和孤对的主要区别是键对由两个键中的电子组成,而孤对由两个不在键中的电子组成。 覆盖的关键领域 1.什么是键对-定义、识别、示例2.什么是孤对-定义、识别、示例3.键对和孤对的区别是什么-关键区别...
- 发布于 2021-06-29 09:14
- 阅读 ( 642 )
vsepr公司(vsepr)和价键理论(valence bond theory)的区别
...它不同于s-s轨道重叠和p-p轨道重叠。为了解释这种键合,科学家莱纳斯·鲍林发现了轨道杂化。杂化导致杂化轨道的形成。杂化轨道主要有以下三种类型。 sp3杂化轨道 这个轨道是在s轨道和3p轨道杂交时形成的(S轨道是球形的,p...
- 发布于 2021-06-29 09:45
- 阅读 ( 703 )
s(s)和p块元素(p block elements)的区别
...有s块元素都是金属。大多数p块元素都是非金属元素。p块中的其余元素是类金属的。s和p块元素的主要区别在于s块元素的价电子在s轨道上,p块元素的价电子位于p轨道。 覆盖的关键领域 1.什么是S块元素–定义、特征属性、成员2...
- 发布于 2021-06-29 09:51
- 阅读 ( 557 )
价键理论(valence bond theory)和分子轨道理论(molecular orbital theory)的区别
...原子间的化学键。然而,价键理论不能用来解释复杂分子中的键合。它非常适合于双原子分子。但是分子轨道理论可以用来解释任何分子中的成键。因此,它比价键理论有许多先进的应用。这就是价键理论和分子轨道理论的区别...
- 发布于 2021-06-29 10:32
- 阅读 ( 417 )
杂化轨道(hybrid orbitals)和分子轨道(molecular orbitals)的区别
...tals) 轨道是可以充满电子的假想结构。根据不同的发现,科学家们提出了这些轨道的不同形状。轨道有三种主要类型:原子轨道、分子轨道和杂化轨道。原子轨道是位于原子核周围的假想轨道。分子轨道是两个原子之间形成共价...
- 发布于 2021-06-29 11:00
- 阅读 ( 528 )
轨道(orbitals)和能级(energy levels)的区别
...连续运动。因此,我们不能给出电子在原子中的具**置。科学家们引入了“概率”的概念,而不是确定电子的确切位置。换句话说,确定了电子最有可能运动的最可能路径。这个路径叫做轨道。这些轨道是根据这些轨道中的电子...
- 发布于 2021-06-29 11:11
- 阅读 ( 407 )