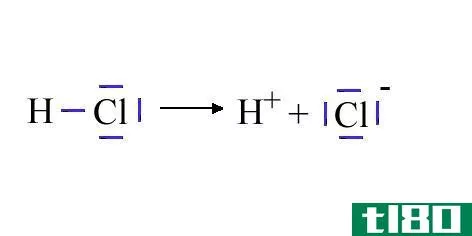化学示例:强电解质和弱电解质
强电解质

强电解质包括强酸、强碱和盐。这些化学物质在水溶液中完全分解成离子。
分子实例
- 盐酸
- 氢溴酸
- 氢碘酸
- 氢氧化钠
- Sr(OH)2-氢氧化锶
- 氯化钠

弱电解质

弱电解质在水中只能部分分解成离子。弱电解质包括弱酸、弱碱和各种其他化合物。大多数含氮化合物是弱电解质。
分子实例
- 氢氟酸
- CH3CO2H-乙酸
- 氨
- H2O-水(自身弱解离)
非电解质

非电解质在水中不会分解成离子。常见的例子包括大多数碳化合物,如糖、脂肪和酒精。
分子实例
- 甲醇
- C2H5OH-乙醇
- C6H12O6-葡萄糖
- 发表于 2021-09-23 22:37
- 阅读 ( 174 )
- 分类:科学
你可能感兴趣的文章
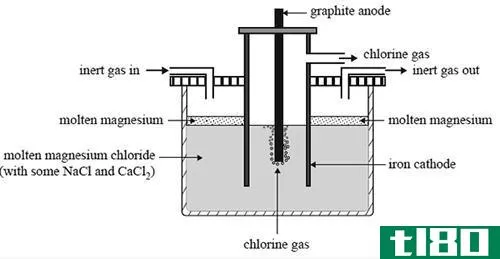
熔化的(molten)和水电解(aqueous electrolysis)的区别
...得熔融状态。因此,我们可以将分析物的熔融状态命名为电解质。 熔融电解过程中,阳离子向负电极移动,阴离子向正极移动。在电极上,原子(负离子)变成负离子。在正电极或阳极,离子失去电子变成原子。 什么是水电解(...
- 发布于 2020-09-17 20:38
- 阅读 ( 395 )
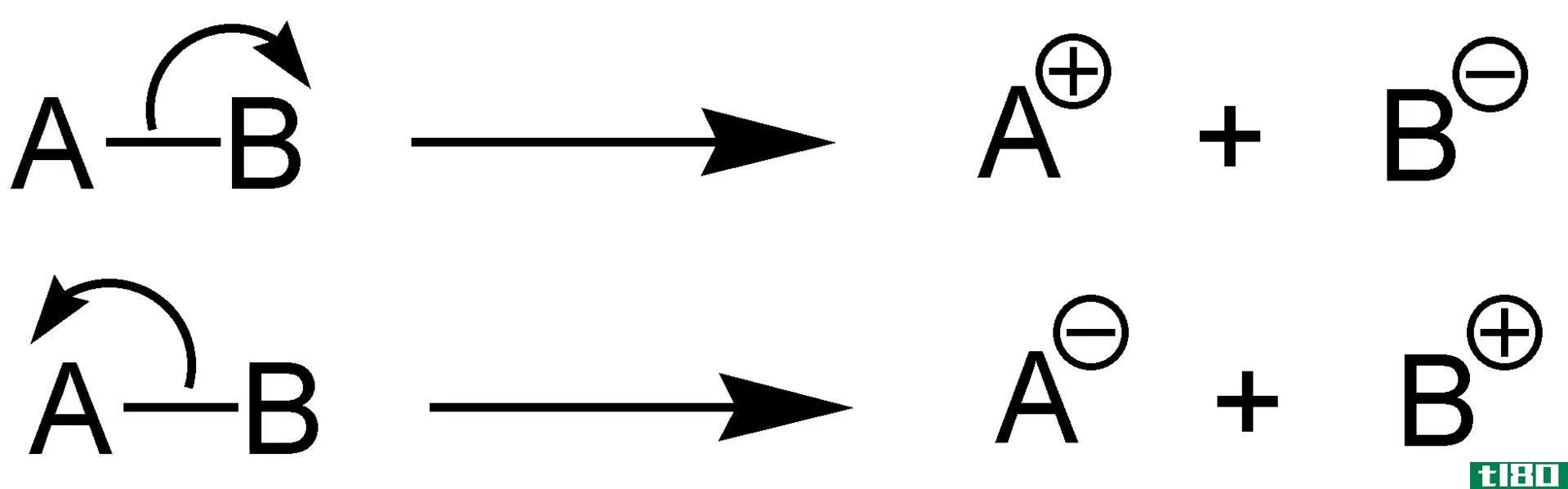
是的(true)和电位电解液(potential electrolyte)的区别
真实电解质和电位电解液的关键区别在于,真正的电解质完全分解成离子,而电位电解质则部分分解成离子。 根据它们产生离子和导电的能力,我们可以把所有化合物分为电解质和非电解质两类。电解是将电流通过电解溶液...
- 发布于 2020-09-21 00:04
- 阅读 ( 266 )
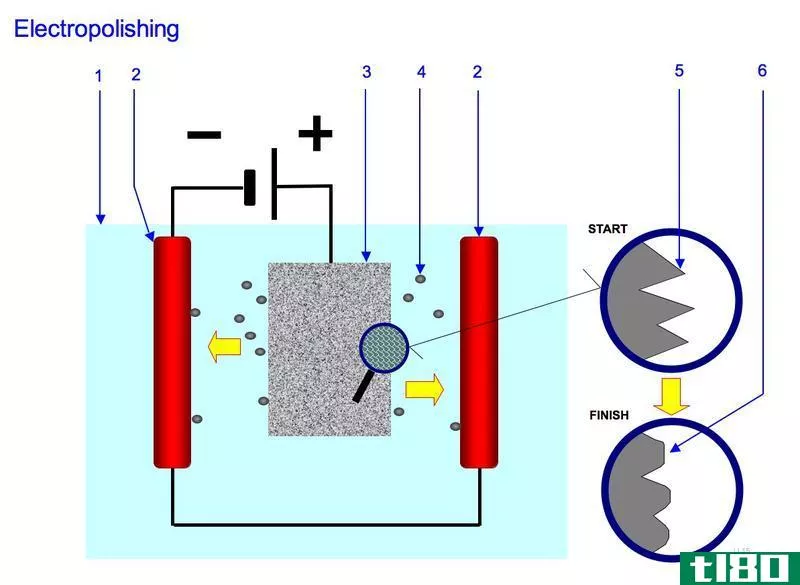
电解抛光(electropolishing)和钝化(passivation)的区别
... 电解抛光是从金属表面去除材料以降低表面粗糙度的电化学过程,而钝化是在金属表面涂覆一层以降低化学反应性的过程。与钝化相比,电抛光最终产生持久的效果。也就是说,电抛光可以在基底表面形成一层持久的涂层。 目...
- 发布于 2020-09-28 03:56
- 阅读 ( 489 )
酸性自由基(acidic radical)和碱基(basic radical)的区别
...此,我们称这种分裂为分离。这些自由基使这些盐成为强电解质。 目录 1. 概述和主要区别 2. 什么是酸性自由基 3. 什么是基本根 4. 并列比较-酸性自由基和碱性自由基的表格形式 5. 摘要 什么是酸性自由基(acidic radical)? 酸性自...
- 发布于 2020-10-17 22:58
- 阅读 ( 336 )
电解质(electrolytes)和非电解质(nonelectrolytes)的区别
电解质和非电解质的主要区别在于,电解质在水中溶解时能产生离子,而非电解质则不能产生离子。 根据它们产生离子和导电的能力,我们可以把所有化合物分为电解质和非电解质两类。将电流通过电解溶液并迫使正负离子...
- 发布于 2020-11-06 17:55
- 阅读 ( 292 )
液体(liquid)和水的(aqueous)的区别
...溶液。 水溶液根据它们是否导电或成为不良导体而有强电解质或弱电解质。良导体在溶液中有更多的电离。为了理解两种水溶液之间的反应,计算是基于溶解前溶质优先形式的“浓度”和溶液的“极性”。 总结: 水溶液和液体...
- 发布于 2021-06-23 23:34
- 阅读 ( 309 )
坚强的(strong)和弱电解质(weak electrolytes)的区别
主要区别强(main difference strong) vs. 弱电解质(weak electrolytes) 电解质是溶解在水中时产生离子的物质。三种主要电解质类型为酸、碱和盐,这些化合物在水中溶解时被分解成离子。正电荷和负电荷离子可以通过这些化合物的水溶液...
- 发布于 2021-06-29 14:13
- 阅读 ( 335 )
电解(electrolysis)和电镀(electroplating)的区别
...。电解槽由两个电极浸入同一溶液中组成。这种溶液叫做电解质。电解液发生的反应应通过电诱导。 在电解槽中,阳极带正电荷,阳极上发生氧化反应;由于阴极上的还原反应,阴极带负电。由于反应是非自发的,它会吸收外...
- 发布于 2021-06-29 14:20
- 阅读 ( 939 )
电解质(electrolytes)和非电解质(nonelectrolytes)的区别
电解质的主要区别(main difference electrolytes) vs. 非电解质(nonelectrolytes) 化合物根据其在水溶液中导电的能力可分为两类。这两类是电解质和非电解质。电解质是一种能溶于水形成离子的化合物。这些离子可以通过溶液导电。非电解...
- 发布于 2021-06-29 15:50
- 阅读 ( 579 )
强电解质(strong electrolytes)和弱电解质(weak electrolytes)的区别
强电解质被称为溶质,具有与溶液完全或部分电离的特性。另一方面,弱电解质被称为溶质,具有部分溶解在溶液中的特征,通常含有大约1-10%的混合液。 对比图 区分依据 强电解质 弱电解质 定义 具有与溶液完全或部分...
- 发布于 2021-07-08 13:50
- 阅读 ( 535 )