主要区别
饱和烃与不饱和烃的主要区别在于,饱和烃是碳链上含有单共价键的碳氢化合物,而不饱和烃是主链上含有双键或三键的碳氢化合物。
饱和烃(saturated hydrocarb***) vs. 不饱和烃(unsaturated hydrocarb***)
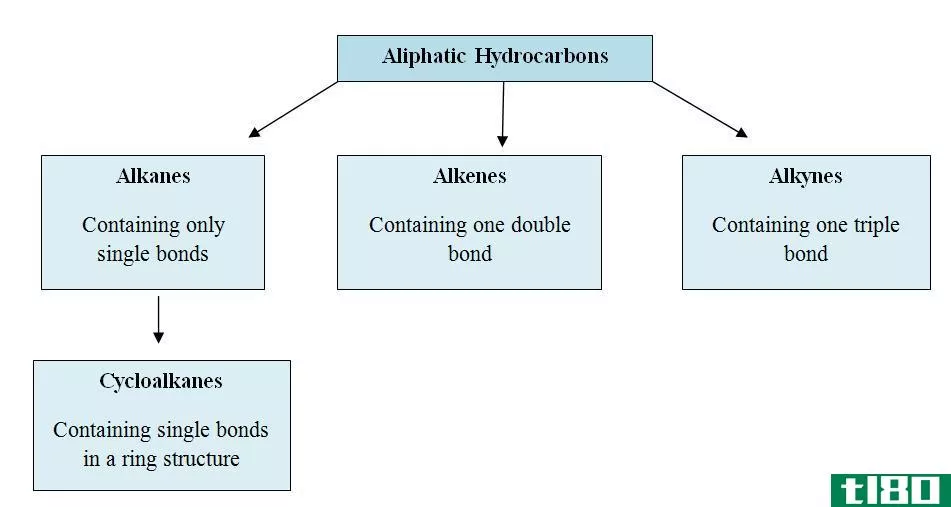
饱和烃是指碳链上只有一个单键的碳氢化合物,而不饱和烃是指在主碳链上含有双键或三键的碳氢化合物。饱和烃总是烷烃的一个例子,而不饱和烃总是只有烯烃和炔烃。饱和烃的活性比不饱和烃小得多,而不饱和烃比饱和烃更具活性。饱和烃在空气中燃烧时产生蓝色的非烟熏火焰,而不饱和碳氢化合物在空气中燃烧时产生黄色和烟灰火焰。饱和烃的碳含量比氢少,而不饱和烃的碳含量比氢高。饱和烃通常是从动物和植物化石中获得的,而不饱和烃通常是从植物材料中获得的。饱和烃可以发生取代反应,而不饱和烃可以发生加成反应。饱和烃含氢量高,而不饱和烃含氢量少。饱和烃是环烷烃的一个例子,而不饱和烃总是环烯烃的一个例子。饱和烃具有自由基机理,而不饱和烃具有亲电加成反应。饱和烃只有sigma键,而不饱和烃有sigma键和pi键。
比较图
什么是饱和烃(saturated hydrocarb***)?
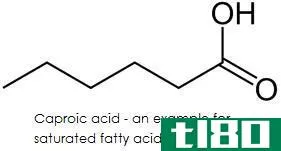
饱和烃是在主碳链上具有单键的碳氢化合物。饱和烃没有自由电子,反应性很低。饱和烃的烷烃中氢的数量很低,而饱和烃的烷烃中碳的数量很高。烷烃通常被认为是饱和烃的最好例子。在空气中,由于燃烧的结果,它会产生蓝色且不含烟灰的火焰。饱和烃的来源是动植物化石材料.it不含多键为共价双键或三键。在它中,碳的四个价态都被氢原子的单原子所满足。饱和烃主要称为单质烃。饱和烃是极性较小或非极性的有机化合物。饱和烃总是反对加成反应,如氧化加成、加氢和Lewis碱结合。饱和这个词来自拉丁语单词“saturate”意思是“填充”。饱和烃总是含有比π键强得多的sigma键。这就是为什么它不那么被动。碳和氢的电负性几乎相似。所以,电负性的差别很小。这就是为什么碳氢化合物是非极性的。饱和烃不溶于水等极性溶剂。
例子
甲烷、丙烷、乙烷等。
什么是不饱和烃(unsaturated hydrocarb***)?
不饱和烃是一种以多重共价键(如三键或双键)形式不饱和的碳氢化合物。不饱和烃是非常活泼的,因为它们有自由电子。氢的含量很低,而碳的含量很高。烯烃和炔烃是不饱和烃的最好例子。在空气中,燃烧会产生黄色和烟熏的火焰。不饱和烃的最佳和主要来源是植物的原料。它的名字已经表明它在主碳链上有两个或三个键。在这个过程中,碳的四个价态都不完全满足,并与链中的另一个原子形成双键或三键。不饱和烃是极性的,由于化合物中存在不饱和度,因此可溶于水。它们不是简单的碳氢化合物。它包含sigma和pi键。这就是为什么它可以很容易地进行加成反应,如氧化加成、氢化和路易斯碱结合。不饱和烃对其他有机化合物的形成非常有用,对各自的饱和烃的形成也非常有用。不饱和烃的结构为直支环状结构。环烯烃,不饱和烃的环状结构也包含在不饱和烃中。
例子
乙烯、丙烯、丁烯、环己烯等。
主要区别
- 饱和烃是指在主碳链上只有一个单键的碳氢化合物,而不饱和烃是指具有双键和三键等多键的碳氢化合物。
- 饱和烃的反应性很低,而不饱和烃的反应性很强。
- 饱和烃产生蓝色和非煤烟火焰,而不饱和碳氢化合物产生黄色和黑色火焰。
- 饱和烃是从动植物化石中获得的,而不饱和烃是从植物材料中获得的。
- 饱和烃有大量的氢,而不饱和烃有大量的氢。
- 饱和烃含有极少量的碳,而不饱和烃含有大量的碳。
结论
以上讨论得出结论,饱和烃和不饱和烃都是碳氢化合物的类型。饱和烃是指在主碳链上只有一个单键的碳氢化合物,而不饱和烃是指具有双键和三键等多键的碳氢化合物。饱和烃也包括烷烃,而不饱和烃也包括烯烃和炔烃。