能斯特电位和Zeta电位的关键区别在于,能斯特电位是针对生物细胞或电化学细胞的,而Zeta电位是针对胶体分散体的。
能斯特电位和zeta电位是物理化学中描述某些东西之间的电位差的术语,如细胞膜、电化学电池、分散介质中分散粒子的膜等。
目录
1. 概述和主要区别
2. 什么是能斯特势
3. 齐塔电位是多少
4. 并列比较-能斯特电位与Zeta电位的表格形式
5. 摘要
什么是能斯特势(nernst potential)?
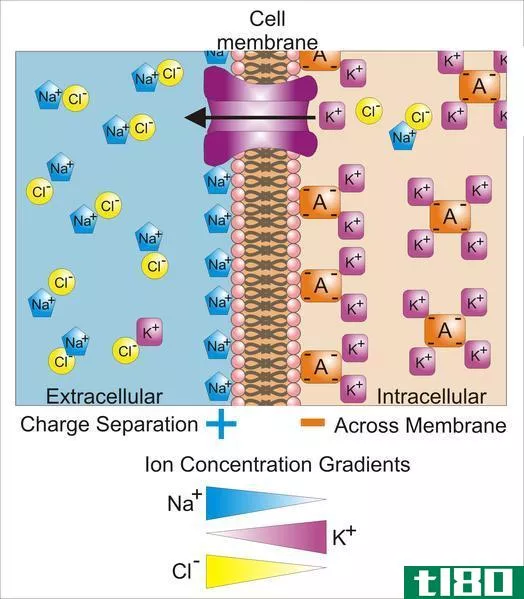
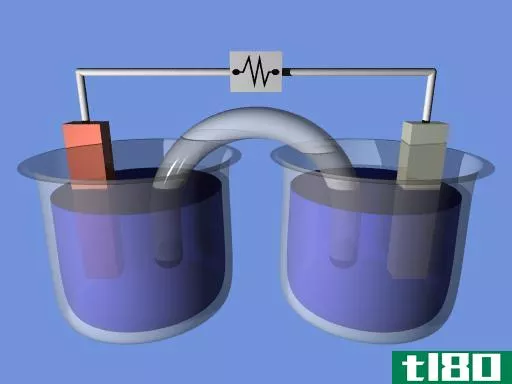
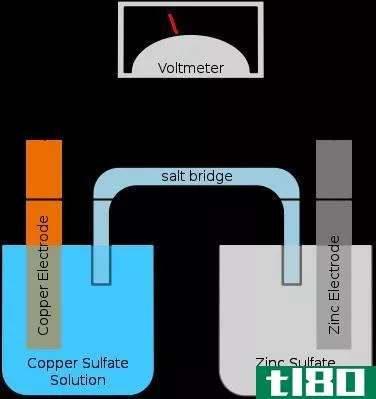
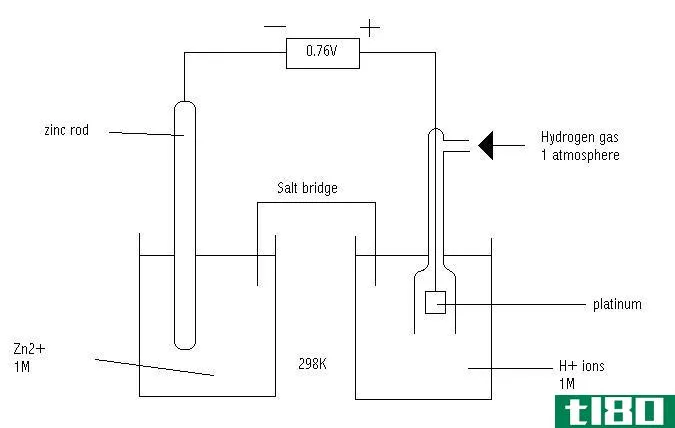
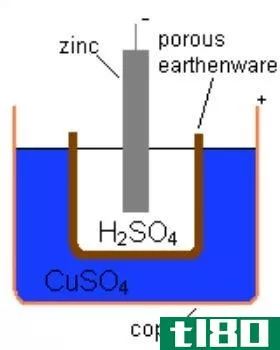
能斯特电位(Nernst电位)或逆转电位(reversion potential)是指通过细胞膜阻止特定离子净扩散的电位。因此,这个术语在生物化学中有应用。我们可以通过细胞内外特定离子(试图穿过细胞膜)浓度的比值来确定能斯特电位。然而,这个术语也用于电化学,关于电化学电池。用来确定能斯特势的方程称为能斯特方程。
能斯特方程可以描述为一个数学表达式,它给出了电化学电池的还原电位与标准还原电位之间的关系。这个方程式是以科学家沃尔特·能斯特的名字命名的。此外,还考虑了影响电化学氧化还原反应的其他因素,如氧化还原过程中化学物质的温度和化学活性,建立了该方程。
为了得到能斯特方程,我们必须考虑吉布斯自由能的标准变化,这种变化与电池中发生的电化学转变有关。电化学电池的还原反应如下:
Ox+z e–⟶红色
在热力学中,反应的实际自由能变化是,
E=还原-氧化
我们可以将吉布斯自由能(ΔG)与E(电位差)联系起来,如下所示:
ΔG=-nFE
式中,n是反应进行时化学物质之间转移的电子数,F是法拉第常数。如果考虑标准条件,则方程如下:
ΔG0=-nFE0
我们可以通过下面的方程把非标准条件的吉布斯自由能和标准条件的吉布斯能联系起来。
ΔG=ΔG0+RTlnQ
然后将上述方程代入标准方程,得到能斯特方程如下:
-nFE=-nFE0+RTlnQ
则能斯特方程如下:
E=E0–(RTlnQ/nF)
什么是zeta电位(zeta potential)?
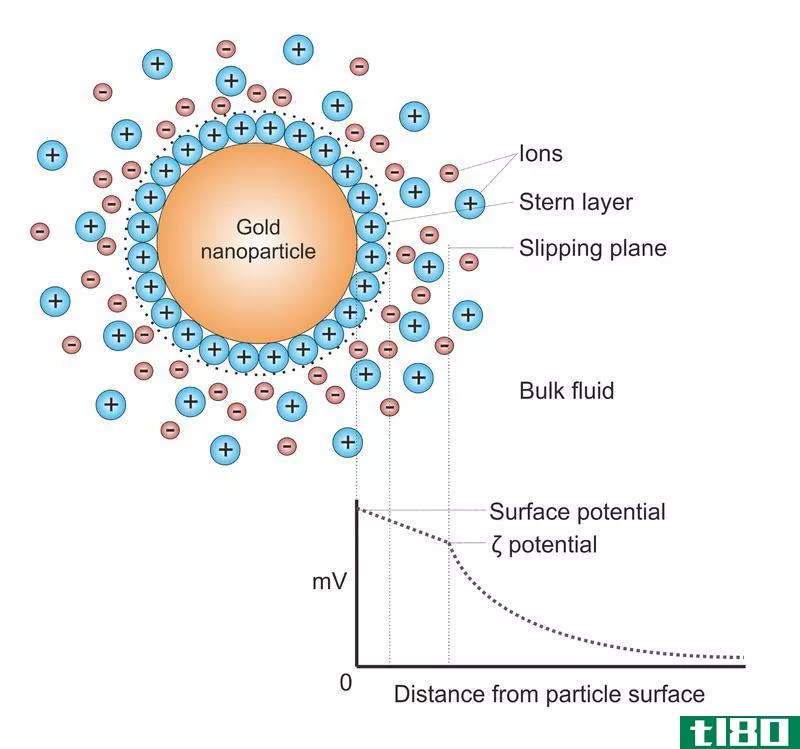
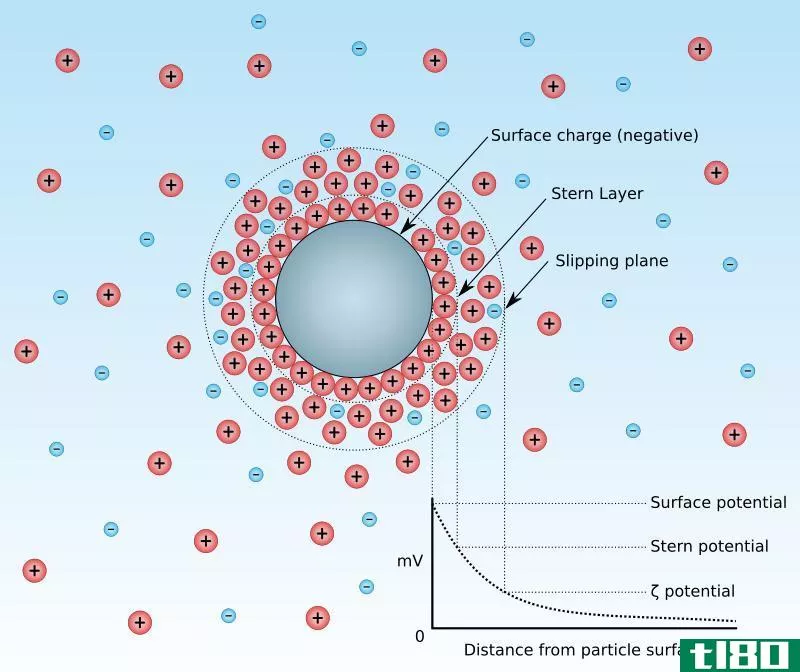
Zeta电位是胶体分散体的电动电位。这个词来自希腊字母“zeta”。一般来说,我们称之为电动势zeta势。换言之,zeta电位是分散介质和附着在胶体分散体分散粒子上的流体固定层之间的电位差。这意味着zeta电势这个术语给我们提供了粒子表面电荷的指示。我们可以识别出两种类型的zeta电位:正的和负的zeta电位。此外,这个势就是我们测量的,粒子在直流电场中的速度。
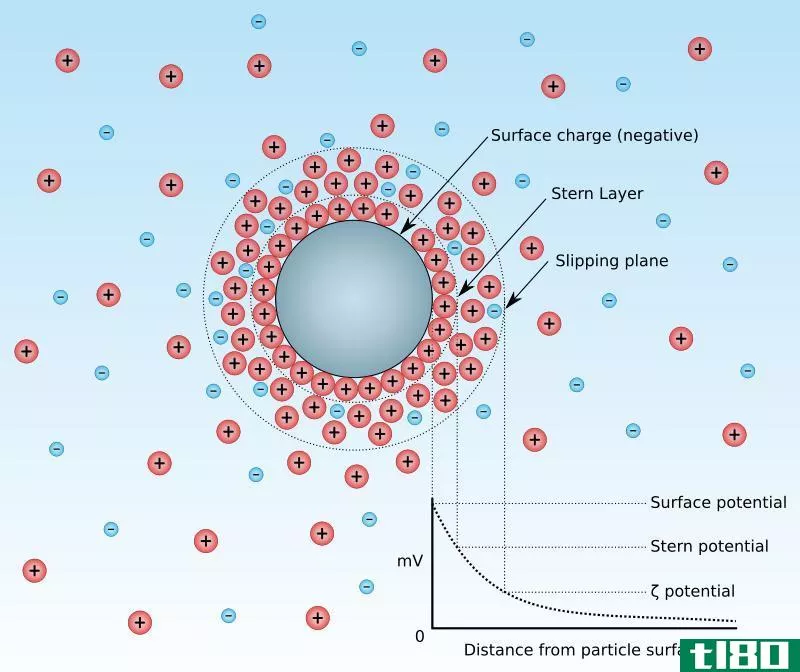
图01:胶体悬浮液中的颗粒
在这两种类型中,正的zeta电位表明在我们测量zeta电位的悬浮液中分散的粒子带有正电荷。此外,当我们考虑这些值时,正zeta电位和负zeta电位之间没有显著差异。
另一方面,负的zeta电位表明我们测量zeta电位的悬浮液中的分散粒子带负电荷;因此,分散粒子的电荷是负的。
能斯特势(nernst potential)和zeta电位(zeta potential)的区别
能斯特势和zeta势用于物理化学。能斯特电位和Zeta电位的关键区别在于,能斯特电位是针对生物细胞或电化学细胞的,而Zeta电位是针对胶体分散体的。
下图显示了能斯特势和Zeta势之间的更多差异。

总结 - 能斯特势(nernst potential) vs. zeta电位(zeta potential)
能斯特势和zeta势在物理化学中被使用。能斯特电位和Zeta电位的关键区别在于,能斯特电位是针对生物细胞或电化学细胞的,而Zeta电位是针对胶体分散体的。
引用
1“Zeta潜力”,维基百科。2020年6月23日,可在此处获取。