浓度与溶解度
集中
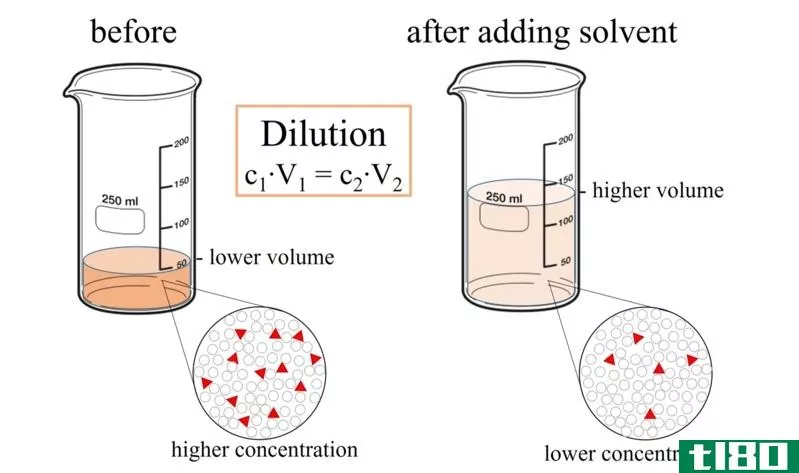
浓度是化学中一种重要而普遍的现象。用于指示物质的定量测量。如果你想测定溶液中铜离子的含量,可以用浓度测量法。几乎所有的化学计算都使用浓度测量来得出混合物的结论。要确定浓度,我们需要混合各种成分。要计算每种成分的浓度,必须知道溶液中溶解的相对量。
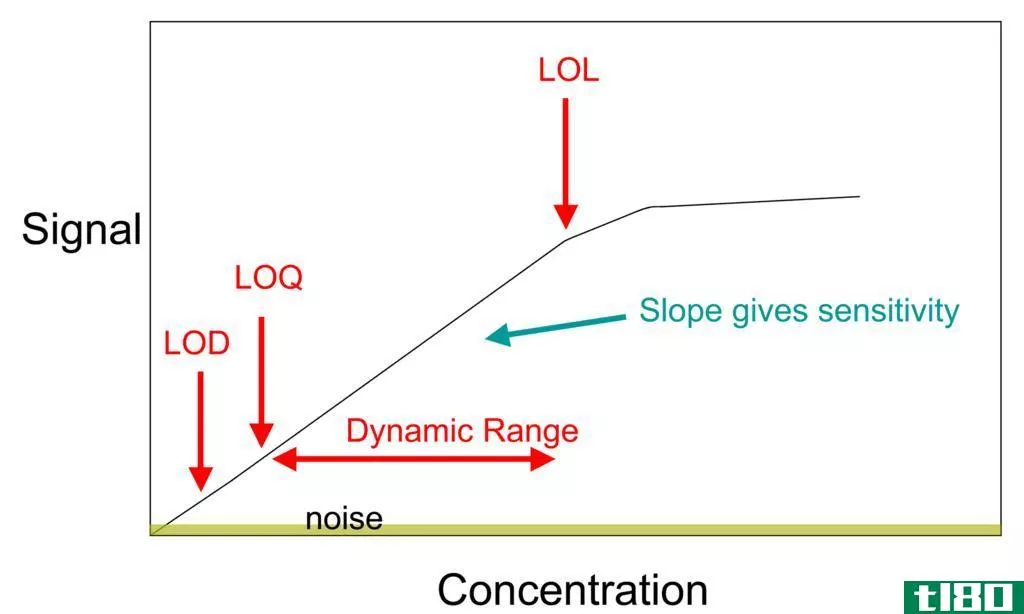
测量浓度的方法很少。它们是质量浓度、数浓度、摩尔浓度和体积浓度。所有这些指标都是分子代表溶质量分母代表溶剂量的比值。在所有这些方法中,溶质的表示方法都是不同的。然而,分母总是溶剂的体积。在质量浓度中,溶解溶质在一公升溶剂中的质量是已知的。同样,在数浓度,溶质的数目,和摩尔浓度,溶质的摩尔数。进一步给出了溶质的体积浓度。除此之外,浓度可以表示为摩尔分数,其中溶质的摩尔数与混合物中物质的总量有关。同样,摩尔比,质量分数,质量比可以用来表示浓度。也可以用百分比值表示。根据需要,必须选择合适的浓度指示方法。然而,化学学生应该知道这些单元之间的转换,以便使用它们。
溶解度
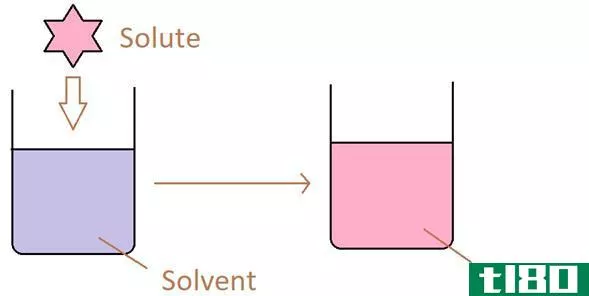
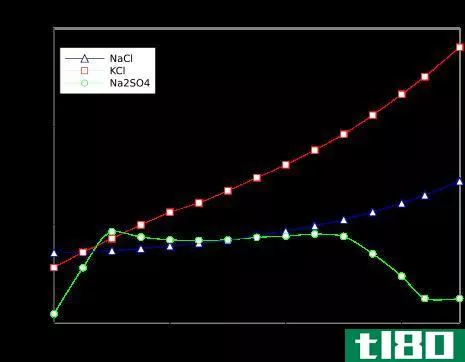
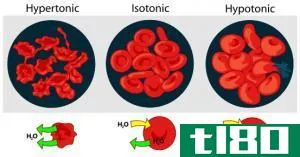
溶剂是一种具有溶解能力的物质,因此可以溶解另一种物质。溶剂可以是液体、气体或固态。溶质是一种溶于溶剂中形成溶液的物质。溶质可以是液态、气态或固相。所以,溶解度是溶质在溶剂中溶解的能力。溶解度取决于各种因素,如溶剂和溶质类型、温度、压力、搅拌速度、溶液饱和水平等。只有当它们相似(“喜欢溶解”时,物质才相互溶。例如,极性物质可溶于极性溶剂,而不溶于非极性溶剂。糖分子之间具有弱的分子间相互作用。当溶解在水中时,这些相互作用将破裂,分子将被分离。债券破裂需要能量。这种能量将由水分子形成氢键提供。由于这个过程,糖在水中很好地溶解。同样,当像氯化钠这样的盐溶于水时,钠和氯离子就会释放,它们将与极性水分子相互作用。以上两个例子得出的结论是,溶质在溶剂中溶解后,会产生其基本粒子。当一种物质首先加入溶剂时,首先它会迅速溶解。经过一段时间的可逆反应,溶解速率将降低。当溶解速率和沉淀速率相等时,溶液就被称为溶解度平衡。这种解称为饱和解。
| 浓度和溶解度的区别是什么?•浓度表示溶液中物质的数量。溶解度是一种物质在另一种物质中溶解的能力。•如果一种物质在溶剂中的溶解度很高,那么它在溶液中的浓度就会很高。同样,如果溶解度低,浓度也会低。 |