主要区别
阶数与分子数的区别在于,反应的阶数是反应中原子浓度提高到的幂的代数和,而分子量是参与一个基本反应的反应物的数量,这个反应由其化学方程式来表示。
秩序(order) vs. 分子量(molecularity)
反应级数是反应中原子浓度提高到的幂的代数和,而分子量则是参与化学反应的反应物的数量,由反应的化学方程式来指示。一个反应的级数减少一个反应物是过量的,而另一方面,在分子量的情况下,对反应物没有这种依赖性。
一个反应的阶数通常是1,2,3,或者可能是零,或者分数或者负数,但是反过来,一个反应的分子量总是自然数。一个反应的级数只能通过实验来确定,不能根据平衡化学方程来预测,而根据平衡方程可以很容易地预测反应的分子量,不需要复杂的实验。
当一个反应在压力、温度和浓度等变化时,反应的顺序可能会发生变化,与此相反,分子量只是参与化学反应的几个反应物,它与大气中的这些变化无关,并使其保持不变。计算一个反应的级数,没有速率决定步骤,用总反应来计算一个反应的级数;但是,用速率决定步骤来获得分子量,不需要整个反应。
有零级反应、一级反应和二级反应,这些反应按顺序分类;然而,根据分子量,有单分子反应、双分子反应和三分子反应。反应级数适用于简单反应和基本反应,而分子量只计算简单反应,没有迹象表明计算复杂反应的分子量。
比较图
什么是秩序(order)?
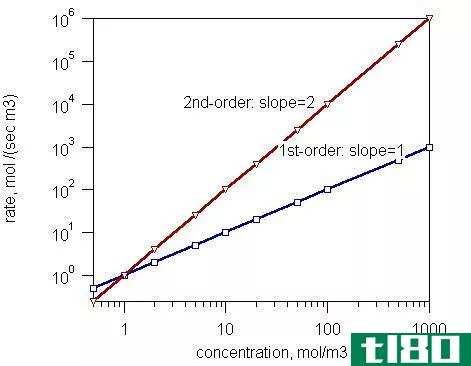
反应的速率级定义为反应中原子浓度提高到的幂的代数和。它也被称为反应过程中每个反应物速率的功率依赖关系。它是导出的速率定律的指数之和,它可能不取决于每种反应物的化学计量系数。由于这个原因,定律的速率是通过实验确定的。
它是关于反应速率的定量测量。速率定律是提出的方程。一个反应的级数通常是1,2,3,或者可能是零,或者分数或者负数。反应的速率级只能通过实验来确定,通常不能根据平衡化学方程来预测。在X+Y+Z→A+B+C的例子中,速率定律的结论是R=k[X]p[Y]q[Z]R。
式中,R是反应速率的缩写,X,Y,Z是反应物,p,q,R是X,Y,Z的反应级数。这里K被认为是比例常数,它反映了反应的性质。化学家讨论p,q,r的和作为反应的动力学方向。实验计算了这些值的顺序。
这个反应的顺序将通过考虑整个反应来计算,不像在分子量中,速率决定步骤决定分子量。根据它们的顺序有几种反应类型。在零级反应中,反应速率不取决于反应物的浓度。一级反应是那些依赖于反应物的审议和对应于单分子反应的反应。一个二级反应物或两个一级反应物都是二级反应,可以通过这两个级反应来决定。
当一个反应受到压力、温度和浓度等变化的影响时,反应的顺序可能会发生变化。为了计算反应的顺序,没有速度决定步骤,用整个反应来计算反应的顺序,反应的顺序适用于简单反应和基本反应。
什么是分子量(molecularity)?
分子量是指参与一个化学反应的反应物的数量,这个反应由它的化学方程式来指示。在分子量的情况下,反应物的过量与反应顺序无关。一个反应的分子量可以是自然数,因为它是特定反应中反应物的数量。
根据反应的平衡方程,可以很容易地预测反应的分子量,不需要复杂的实验。它不依赖于外部环境,因为它只是参与化学反应的反应物的数量,这使得它与大气中的这些变化无关,并使其保持不变。速率测定步骤用于获得分子量,不需要整个反应。
根据分子量,有单分子反应、双分子反应和三分子反应。在单分子反应中,一个单分子在反应过程中发生修正,它只有一个反应物和一个速率决定步骤。在双分子反应中,两个反应物参与并完成反应。然而,在三分子反应中,有三种反应物参与反应的速率决定步骤。分子量只是简单反应的计算;只是没有迹象表明复杂或多步反应的分子量。
主要区别
- 反应级数是反应中原子浓度的幂的代数和,而分子量只是参与化学反应的反应物的数量。
- 零级反应、一级反应和二级反应按顺序分类;但根据分子量,有单分子反应、双分子反应和三分子反应。
- 一个反应的级数降低,就好像在一个反应中发现一个反应物过量,而另一方面,在分子量的情况下,对反应物没有这种依赖性。
- 反应的阶数一般为1、2或3,也可以为零、违规或负数,但另一方面,反应的分子量始终可以是自然数。
- 反应的速率级只能通过实验来确定,而反应的分子量可以根据其平衡方程来预测。
- 当一个反应在压力、温度和浓度等变化时,反应的顺序可能会发生变化,与此相反,分子量只是参与化学反应的几个反应物,不受外界环境条件的影响。
- 没有速率决定步骤,整个反应用于计算反应的阶数;但是,速率确定步骤用于获得分子量。
- 反应的顺序适用于简单和复杂的反应,或是由多个步骤同时完成的反应,而分子量仅适用于简单反应。
结论
反应级数是反应中原子浓度增加到分数或负数的幂的代数和,而分子量是参与基本反应的反应物的数量,并且是中性数。