过渡金属与金属
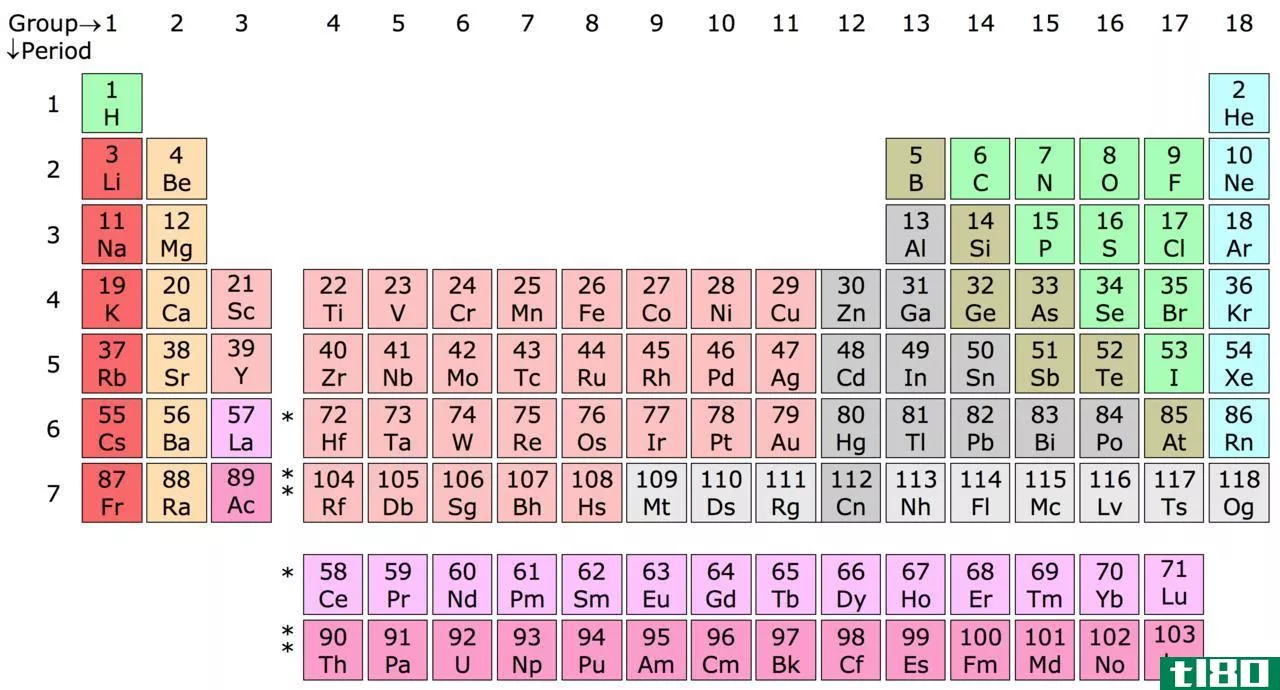
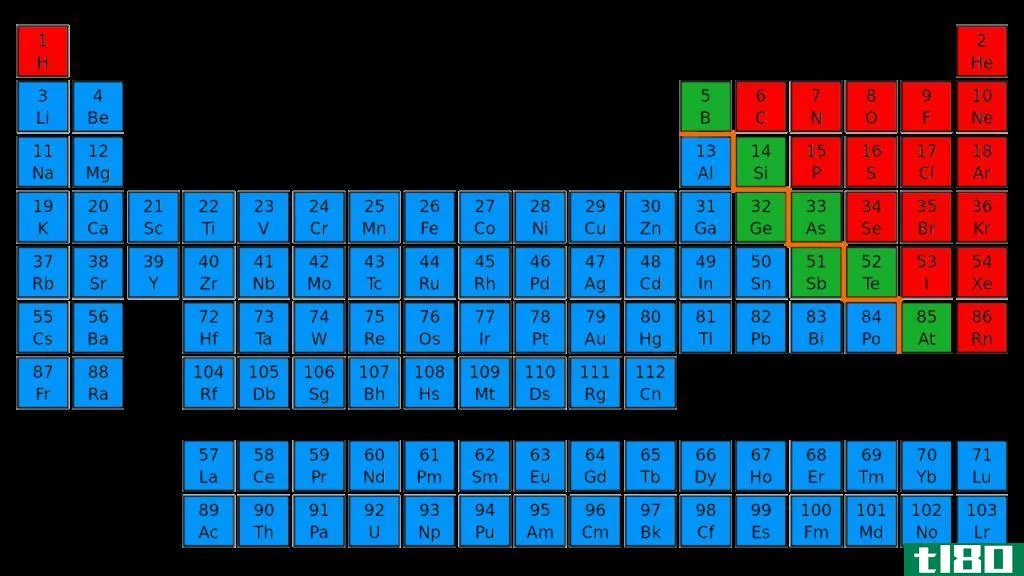
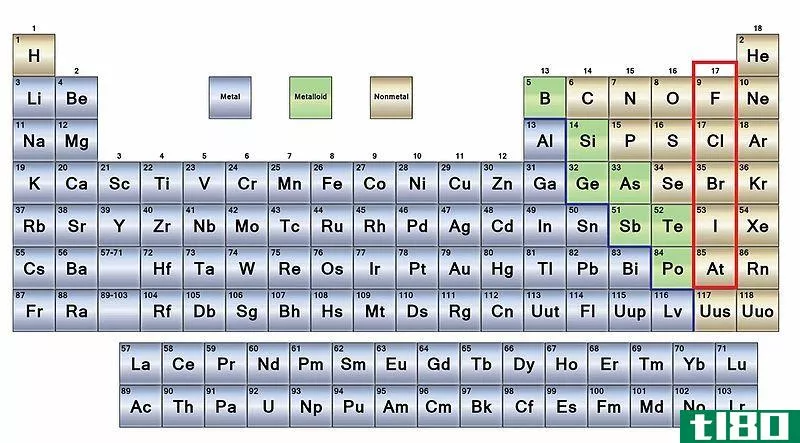
元素周期表中的元素主要可分为两类:金属和非金属。其中,大部分是金属,p块中的非金属元素较少。
金属
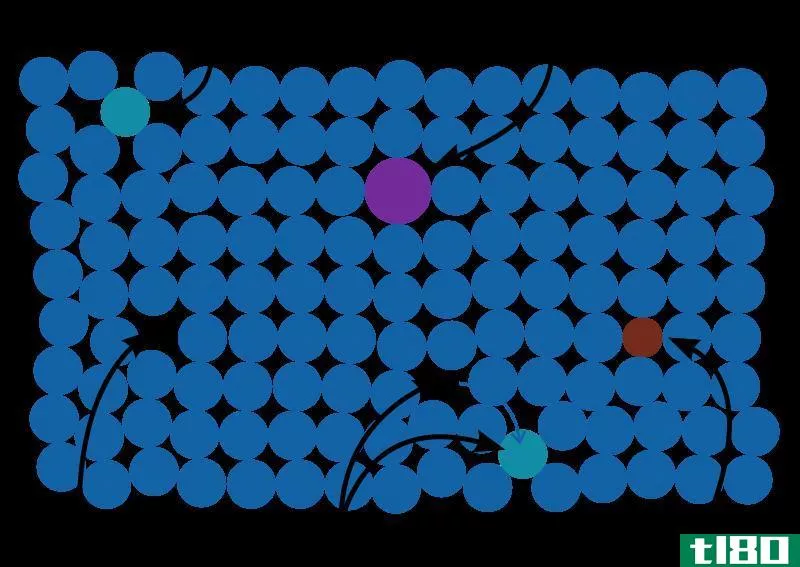
金属为人类所知已有很长一段时间了。有证据证明,早在公元前6000年就有金属的使用。金和铜是最早被发现的金属。这些金属被用来**工具、珠宝、雕像等。从那时起,在很长的一段时间里,只发现了很少的其他金属。现在我们已经熟悉了86种不同类型的金属。金属因其独特的特性而非常重要。通常金属是坚硬的(也有例外,比如钠)。钠可以用刀切)。水银是液态的金属。除汞外,其他金属都是固态的,与其他非金属元素相比,很难破碎或改变形状。金属有光泽的外表。它们大多数都有银色的光泽(除了金和铜)。由于一些金属和大气中的气体如氧气有很强的反应性,随着时间的推移,它们往往会变得暗淡。这主要是由于金属氧化物层的形成。另一方面,像金和铂这样的金属是非常稳定和不活泼的。金属具有延展性和延展性,这使得它们可以用来**某些工具。金属是原子,可以通过除去电子而形成阳离子。所以它们是正电的。金属原子之间形成的键的类型称为金属键合。金属在外层释放电子,这些电子分散在金属阳离子之间。因此,它们被称为离域电子的海洋。电子和阳离子之间的静电相互作用称为金属键合。电子可以移动,因此金属有导电的能力。而且,它们是良好的热导体。由于金属键合,金属具有有序的结构。金属的高熔点和沸点也是由于这种牢固的金属结合。此外,金属的密度比水高。IA族和IIA族元素是轻金属。它们与上述金属的一般特征有些不同。
过渡金属
根据IUPAC的定义,过渡金属是一种元素,其原子具有不完整的d亚壳层,或者可以生成具有不完整d亚壳层的阳离子”。我们通常把周期表中的d块元素作为过渡金属。所有这些都具有金属的特性,但它们与s块和p块中的金属略有不同。产生这些差异的原因主要是由于d电子。过渡金属在化合物中有多种氧化状态。通常,它们的反应性比其他金属(例如s块中的金属)要低。由于d-d电子跃迁,过渡金属具有形成有色化合物的能力。此外,它们还可以形成顺磁性化合物。除此之外,由于金属键合,它们还具有一般的金属性质。它们是良好的电导体和热导体,具有高熔点、高沸点和高密度等。
| 过渡金属和金属有什么区别?•过渡金属属于金属族。•d块体元素通常被称为过渡金属。•过渡金属与其他金属相比反应性较小。•过渡金属可形成有色化合物。•过渡金属在化合物中可以有各种氧化状态,但是其他金属的氧化状态有限(大多数情况下是一种状态)。 |