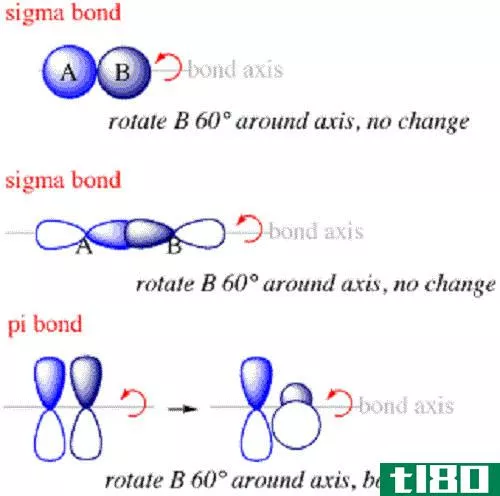
西格玛与π键
正如美国化学家G.N.Lewis提出的那样,当原子的价壳层中含有8个电子时,原子是稳定的。大多数原子的价壳层中的电子少于8个(周期表第18组中的稀有气体除外);因此,它们是不稳定的。这些原子趋向于相互反应以变得稳定。因此,每一个原子都可以实现稀有气体的电子组态。这可以通过形成离子键、共价键或金属键来实现。其**价键是一种特殊的键合形式。与其他化学键不同,在共价键中,两个原子之间有形成多个键的能力。当两个原子具有相似或极低的电负性差时,它们一起反应,通过共享电子形成共价键。当每个原子的共享电子数超过一个时,就会产生多个键。通过计算键序,可以确定分子中两个原子间共价键的数目。多重键有两种形式。我们称之为sigma键和pi键。
西格玛键
符号σ用来表示sigma键。当两个电负性差相似或很低的原子之间共享两个电子时,就会形成单键。这两个原子可以是同一类型的,也可以是不同类型的。例如,当同一个原子结合形成Cl2、H2或P4等分子时,每个原子通过一个共价键与另一个原子结合。甲烷分子(CH4)在两种元素(碳原子和氢原子)之间具有单共价键。此外,甲烷是原子间具有极低电负性差的共价键的分子的一个例子。单共价键也被称为sigma键。Sigma键是最强的共价键。它们是在两个原子之间通过结合原子轨道而形成的。当形成西格玛键时,可以看到头对头的重叠。例如在乙烷中,当两个等量的sp3杂化分子线性重叠时,就会形成C-Cσ键。此外,碳的一个sp3杂化轨道和氢的s轨道之间的线性重叠形成了C-Hσ键。只有通过sigma键结合的基团,才有能力围绕该键相互旋转。这种旋转使分子具有不同的构象结构。
π键
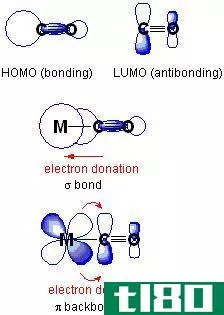
希腊字母π用来表示π键。这也是一种共价化学键,通常在p轨道之间形成。当两个p轨道横向重叠时,形成π键。当这种重叠发生时,p轨道的两个叶瓣与另一个p轨道的两个叶瓣相互作用,两个原子核之间形成一个节面。当原子间存在多个键时,第一个键是sigma键,第二个键和第三个键是pi键。
| 西格玛键和π键的区别是什么?•Sigma键是由轨道的头对头重叠形成的,而pi键是由横向重叠形成的。•Sigma键比pi键更强。•Sigma键可以在s和p轨道之间形成,而pi键主要是在p和d轨道之间形成的。•原子间的单个共价键是Sigma键。当原子之间有多个键时,可以看到π键。•π键产生不饱和分子。•Sigma键允许原子自由旋转,而pi键限制自由旋转。 |