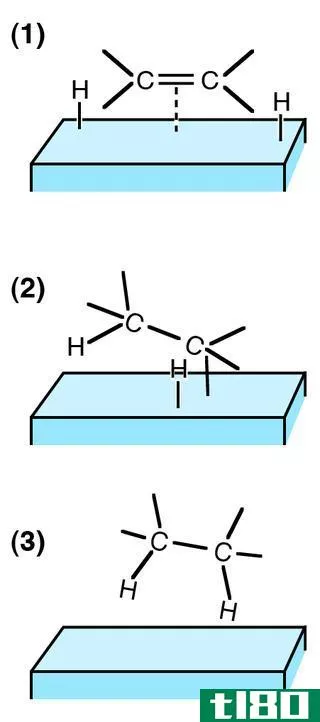
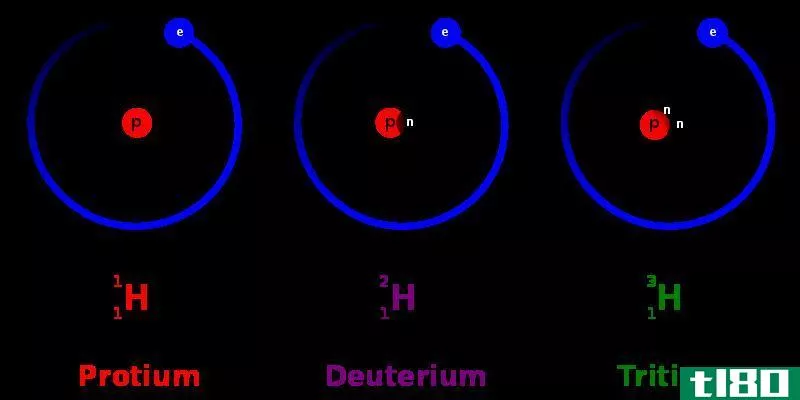
氘与氢
同一元素的原子可以不同。同一元素的这些不同原子称为同位素。它们因拥有不同数量的中子而彼此不同。由于中子数不同,它们的质量数也不同。元素可能有几种同位素。每种同位素的性质决定了元素的性质。氘是氢同位素,下面的文章描述了它们的区别。
氢
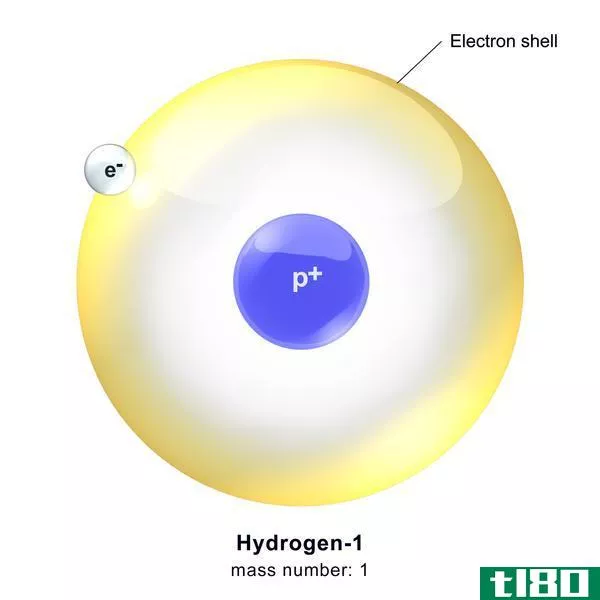
氢是元素周期表中第一个也是最小的元素,用氢来表示,它有一个电子和一个质子。由于它的电子构型为1s1,它在周期表中被归为1组和1周期。氢可以吸收一个电子形成一个带负电的离子,也可以很容易地把电子捐赠出来产生一个带正电的质子,或者分享电子形成共价键。由于这种能力,氢存在于大量的分子中,是地球上含量非常丰富的元素。氢有三种同位素,分别是protium-1H(无中子)、氘-2H(一个中子)和氚-3H(两个中子)。蛋白质是三种植物中最丰富的一种,相对丰度约为99%。氢以双原子分子(H2)的形式存在于气相中,是无色无味的气体。此外,氢是一种极易燃烧的气体,燃烧时会发出淡蓝色的火焰。在正常室温下,氢的反应性不是很强。然而,在高温下,它可以快速反应。H2处于零氧化状态,因此可以作为还原剂,还原金属氧化物或氯化物,释放金属。氢用于化学工业,如哈伯法合成氨。液氢被用作火箭和车辆的燃料。
氘
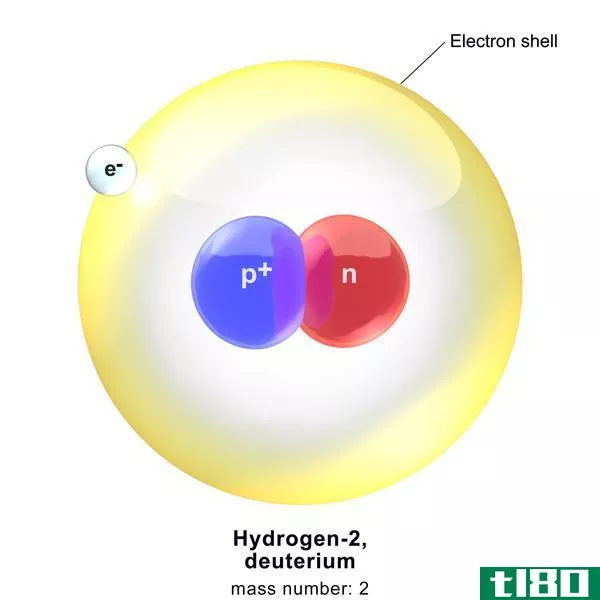
氘是氢的同位素之一。它是一种稳定同位素,天然丰度为0.015%。氘核中有一个质子和一个中子。因此,它的质量数是2,原子序数是1。这也被称为重氢。氘表示为2H,但通常用D表示。氘可以作为化学式D2的双原子气体分子存在。然而,由于氘的丰度较低,在自然界中连接两个D原子的可能性很低。因此,大部分氘与一个1H原子结合,形成一种称为HD(氢氘化氢)的气体。两个氘原子可以与一个氧结合形成水的模拟物D2O,也就是重水。含氘的分子表现出与氢类似物不同的化学和物理性质。例如,氘可以表现出动力学同位素效应。氘化物在核磁共振、红外光谱和质谱上表现出特征性的差异,因此可以用这些方法进行鉴别。氘的自旋是一。所以在核磁共振中,氘耦合产生了三重态。在红外光谱中,它吸收的红外频率与氢不同。由于质量差异大,在质谱中,氘和氢可以区分开来。
| 氢和氘的区别是什么?•氘是氢的同位素。•与其他氢同位素相比,氘的质量数为2(原子核中有一个中子和一个质子)。•氢的原子量为1.007947,而氘的质量为2.014102。•当氘被纳入分子而不是氢时,某些性质如键能和键长是不同的 |