水和冰的关键区别在于水没有规则的分子排列,而冰有一定的晶体结构。
从地球进化的最初阶段起,水一直是地球的主要组成部分。今天,水覆盖了地球表面70%以上的面积。从这一点来看,大部分的水是在海洋中,约占97%。河流、湖泊和池塘有0.6%的水,约2%存在于极地冰盖和冰川中。地下有一定量的水,还有一小部分是以气体形式存在的蒸汽和云中。其中,人类直接使用的水只剩下不到1%。这种纯净水也日益受到污染,应该有一个适当的计划来节约用水。
目录
1. 概述和主要区别
2. 水是什么
3. 冰是什么
4. 并列比较——表格形式的水与冰
5. 摘要
什么是水(water)?
水是一种无机化合物,化学式为H2O。我们离不开水。两个氢原子与一个氧原子共价键合形成水分子。此外,分子呈弯曲形状,以尽量减少电子孤对键的排斥作用,H-O-H角为104o。水是一种清澈、无色、无味、无味的液体。此外,它可以有各种形式,如雾、露水、雪、冰、蒸汽等。当在正常大气压下加热到100℃以上时,它就会变成气相。
水确实是一种神奇的分子。它是生物中含量最丰富的无机化合物。我们身体75%以上是由水组成的。在那里,它是细胞的组成部分,充当溶剂和反应物。然而,它在室温下是一种液体,尽管它的分子量为18gmol-1。

图01:水处于液相
水形成氢键的能力是它的一个独特特性。在那里,一个水分子可以形成四个氢键。氧比氢更具电负性,使水分子中的O-H键极性。由于极性和形成氢键的能力,水是一种强大的溶剂。此外,由于它能溶解大量的物质,我们称之为通用溶剂。此外,水具有高表面张力、高附着力、内聚力。它能承受温度的变化,而不会变成气体或固体。我们将其命名为具有高热容,这反过来又对生物体的生存很重要。
什么是冰(ice)?
冰是水的固体形式。当我们称水低于0摄氏度时,它就开始结冰。冰要么是透明的,要么是稍微不透明的。然而,有时它的颜色取决于它所含的杂质。此外,该化合物具有有序规则的晶体结构。

图02:水面上的浮冰
氢键对于在冰中形成这种有序的固体结构很重要。氢键使水分子保持一定距离,形成晶体结构。在这个过程中,相同质量的H2O的体积膨胀(这意味着在结冰形成冰时,水的质量得到了相对较大的体积)。由于水结冰时体积膨胀,冰的密度比水低。因此,它可以浮在水面上。这样可以防止水体底部的水在冬季结冰,从而保护水生生物。
水(water)和冰(ice)的区别
冰是水的固体形式,它有一定的晶体结构,但水没有这样规则的分子排列。所以,这就是水和冰的关键区别。由于水分子之间的氢键的存在,所以产生了氢键。在冷冻过程中,氢键使水分子保持一定距离,使冰形成晶体结构。而且,这个过程会增加体积。因此,作为水和冰的另一个重要区别,我们可以说冰的密度比水低。因此它可以漂浮在水面上。
此外,我们还可以根据水和冰的体积和密度来区分它们。也就是说,对于同样的质量,水的体积比冰要小。因为水的密度比冰的密度高。下图显示了冰和冰之间的差异。
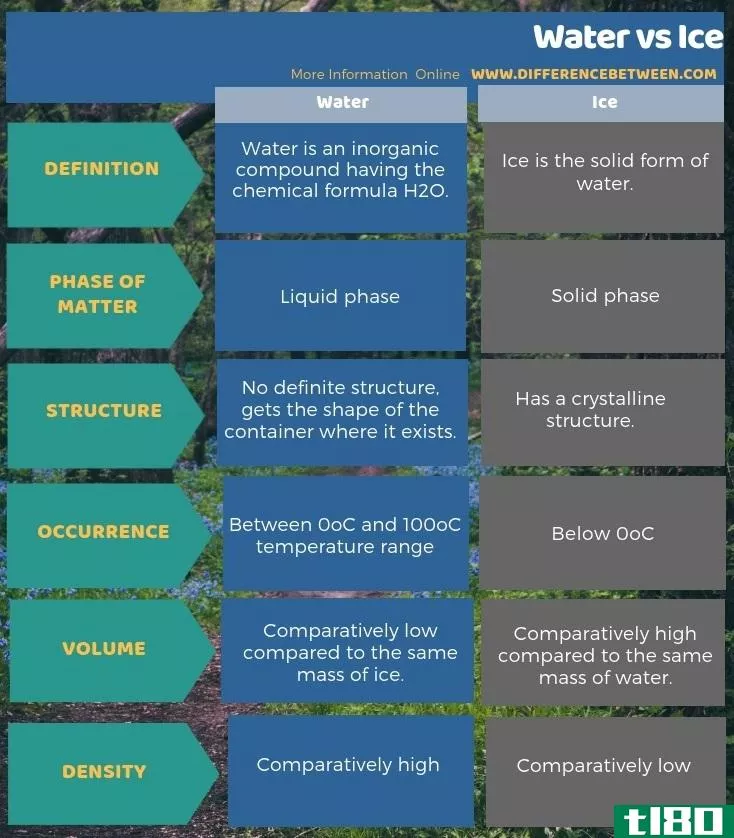
总结 - 水(water) vs. 冰(ice)
冰是水的固体形式。然而,由于水分子之间存在氢键,当我们在0℃以下冷却时,冰会形成规则排列的水分子。因此,水和冰的关键区别在于水没有规则的分子排列,而冰具有一定的晶体结构。
引用
1“冰、水和简单的化学反应。”四分之一学习指南,出版商名称四分之一研究指南出版商徽标,2018年4月17日。这里有2个。Zumdahl,Steven S.“水”,百科全书《大英百科全书》,2018年10月4日,可在此处获取
2Zumdahl,Steven S.“水”,《大英百科全书》,百科全书《大英百科全书》,2018年10月4日















