基态与激发态
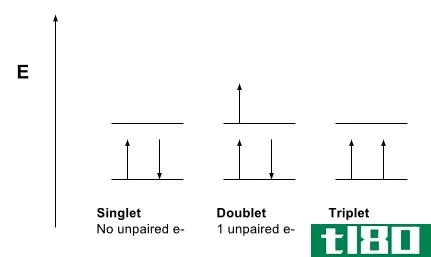
基态和激发态是原子结构下讨论的两种原子态。基态和激发态的概念广泛应用于天文学、量子力学、化学分析、光谱学甚至医学科学等领域。对基态和激发态有一个清楚的认识是至关重要的,这样才能在这方面取得优异的成绩。本文将讨论什么是激发态和基态,它们的相似性,基态和激发态的应用,最后讨论激发态和基态的区别。
基态
要了解基态,首先必须了解原子结构。最简单的原子是氢原子。它由一个质子和一个围绕原子核运行的电子组成。原子的经典模型是原子核和环绕原子核的电子。经典模型足以描述原子的基态和激发态,但需要一些量子力学的概念。量子力学系统的基态被称为系统的基态。一维量子波的波函数是正弦波的一半。当系统处于绝对零度时,系统被称为获得了基态。
激发态
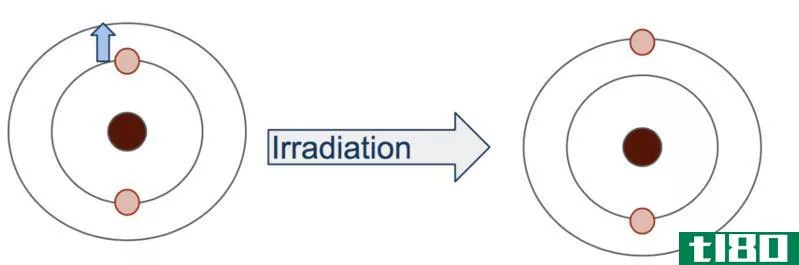
原子或任何其他系统的激发态也取决于系统的结构。为了理解这一点,让我们更深入地了解原子结构。原子由原子核和围绕它运转的电子组成。与原子核的距离取决于电子的角速度。角速度依赖于电子的能量。这个系统的量子力学解释告诉我们,电子不能仅仅以任何值作为能量。电子的能量是离散的。因此,电子不能与原子核保持任何距离。电子所处的距离函数也是离散的。当给一个电子能量时,光子的能量正好是系统当前能量和系统能获得的更高能量之间的能隙,电子就会吸收光子。电子将进入更高的能量状态。任何高于基态能量的能级都被称为激发能级。在这些能级上运行的电子称为激发电子。如上所述,电子的激发态不能取任意值。它只能取一定的量子力学值。
| 基态和激发态的区别是什么?•基态是系统的最低能量状态,而激发态是高于基态的任何能量状态。•系统只有一个基态能量,但每个系统可能有许多可能的激发态。 |