激发(excitation)和电离势(ionization potential)的区别
激发电势和电离势这两个术语与移动电子所需的能量有关,但根据电子运动的目的地,它们之间存在差异。换句话说,在这两种情况下,电子运动后的目的地是不同的。用这种方法可以识别出两个电子的运动。电子可以移动到原子或分子中更高的能级,也可以从原子核中脱离并远离原子。这两个过程都需要一定数量的能量。电子不能移动,除非所需的能量没有被吸收。激发势和电离势的关键区别在于激发势是从一个能级跃迁到另一个能级所需的能量,而电离势是从原子中除去电子所需的能量。
什么是激发电位(excitation potential)?
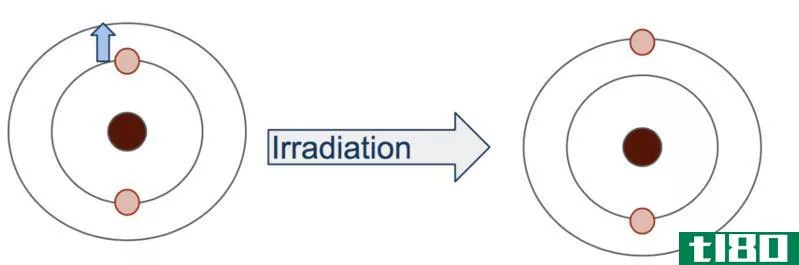
Atoms have energy levels that are called orbits. Electr*** move around the nucleus in these orbits. Electr*** can’t choose arbitrary orbits; they are placed in certain orbits according to their energy levels and they are restricted to move or jump to another energy level unless they absorb the required amount of energy. Moving from one orbit to another after absorbing the required amount of energy is called excitation and the energy absorbed to move from one orbit to other is called excitation potential or excitation energy. 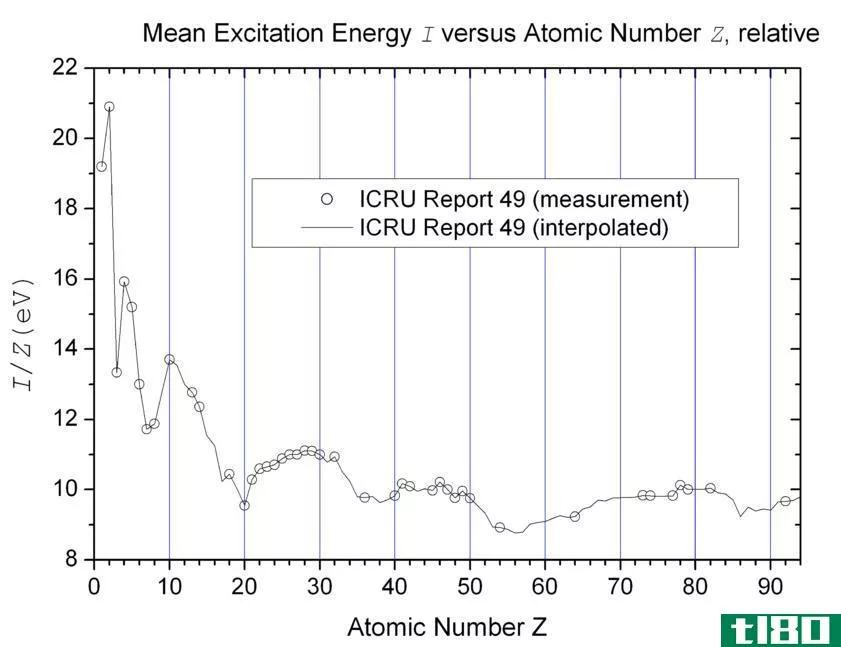
什么是电离势(ionization potential)?
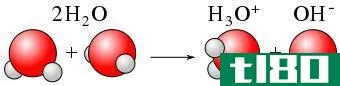
电离是从价壳层中除去一个电子的过程。一般来说,电子通过强大的静电力与原子核结合。因此,从原子中完全除去一个电子需要能量。这被定义为将一个电子从原子或分子移到无限远的地方。这个过程所需的能量称为“电离能”或“电离势”。
换言之,这是电子束缚在原子核上的初始状态和电子不再附着在原子核上的最终状态之间的势能差。
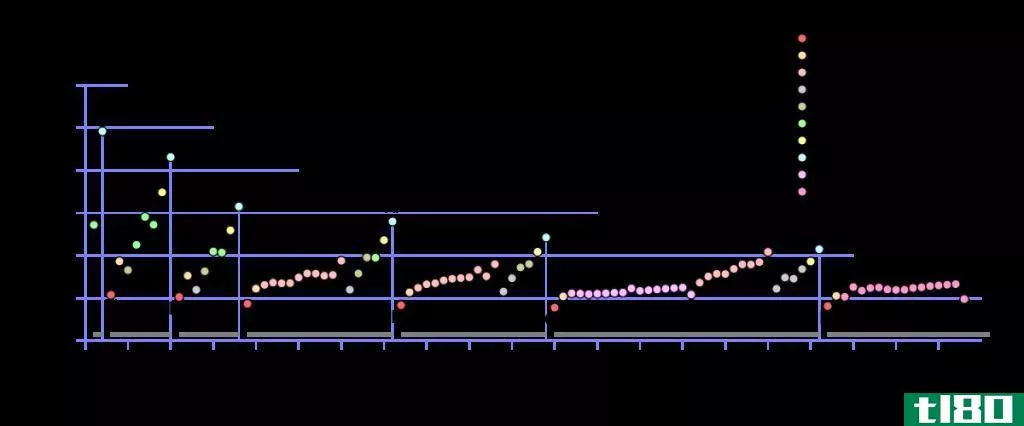
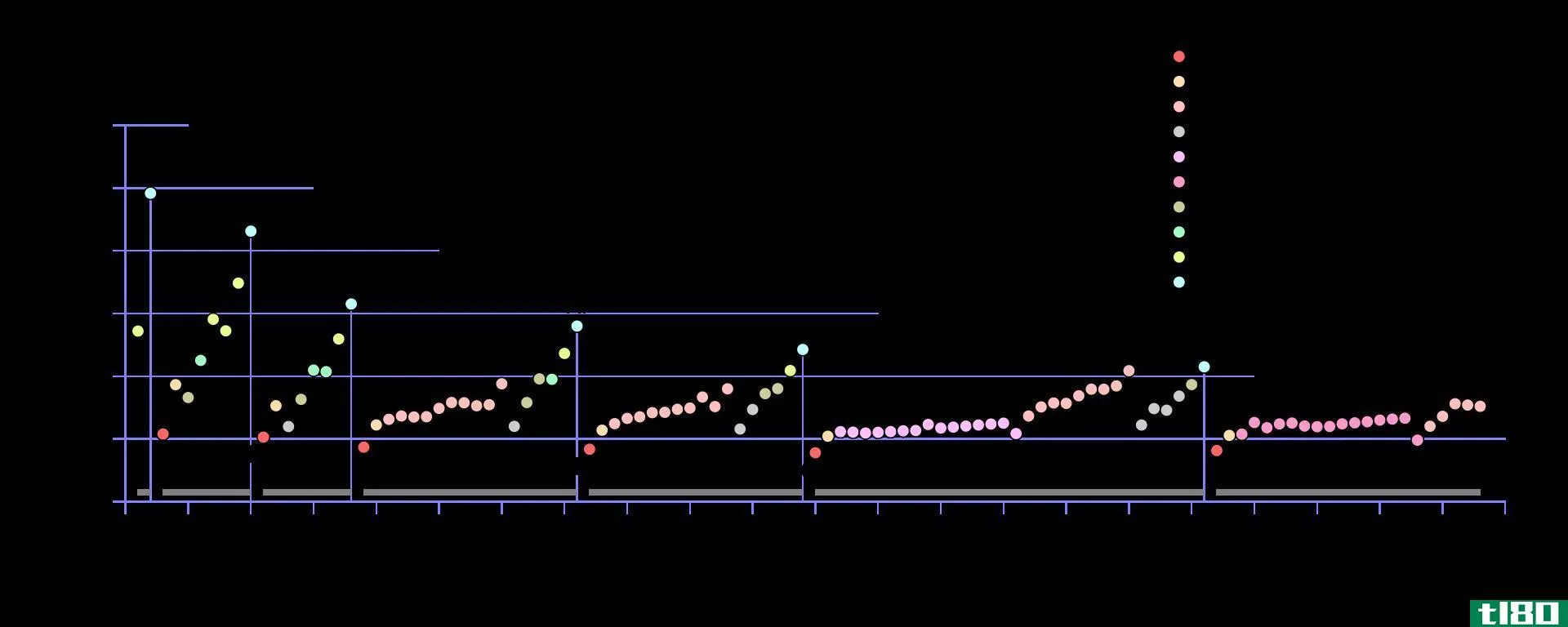
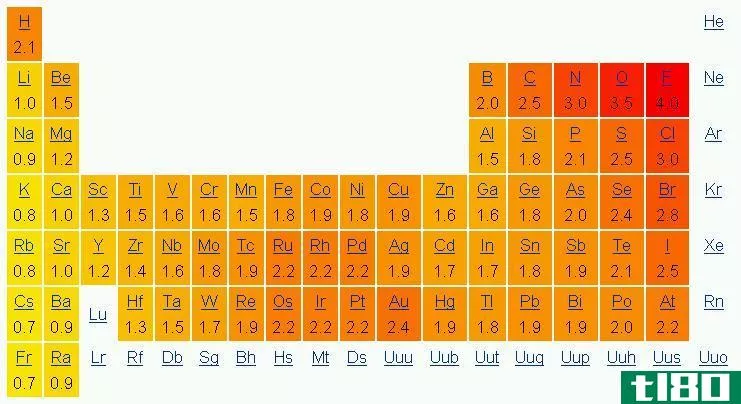
电离能(IE)与质子数的周期趋势
激发(excitation)和电离势(ionization potential)的区别
激发和电离势的定义
激发电位:
从一个激发态到另一个能级的能量叫做“从一个激发态到另一个能级的能量”。这通常是初始状态和最终状态之间的能量差。
注:电子在原子内部运动,但能级不同。
电离电位:
从原子中除去电子所需的能量称为“电离势”或“电离能”。这是电子与原子核结合,电子从原子中移除的两种状态之间的电位差。当电子处于无限远的距离时,能量被认为是零。
注:电子从原子中被移除,当它被移除时,原子核就没有吸引力了。
计算:
激发电位:
当一个电子从基态(n=1)跃迁到另一个(n=2)能级时,相应的能量称为第一激发势。
| 第一激发电势=能量(n=2级)-能量(n=1级)=-3.4 ev–(-13.6 ev)=10.2 ev |
当一个电子从基态(n=1)跃迁到另一个(n=3)能级时,相应的能量称为第二激发势。
| 第二激发电势=能量(n=3级)-能量(n=1级)=-1.5 ev–(-13.6 ev)=12.1 ev |
电离电位:
考虑从n=1能级移除一个电子。电离势是将电子从n=1能级移到无穷大所需的能量。
| 电离势=E无穷大-E(n=1电平)=0–(-13.6 ev)=13.6 ev |
在原子中,最松散束缚的电子首先被移除,电离势随着电离而逐渐增加。
Image Courtesy:
“Mean Excitation Potential” by HPaul – Own work. (Public Domain) via Wikimedia Comm***