电离能和结合能的关键区别在于,电离能是除去孤立的中性气体原子或分子中最松散束缚的电子所需的最小能量,而结合能是从粒子系统中移除粒子所需的最小能量。
化学体系的电离能和结合能是两个不同的术语,描述了两种不同的现象。让我们在本文下面讨论更多细节。
目录
1. 概述和主要区别
2. 什么是电离能
3. 什么是结合能
4.并列比较-电离能与结合能的表格形式
5. 摘要
什么是电离能(ionization energy)?
电离能是一个孤立的中性气体原子或分子中束缚最松散的电子所需的最小能量。我们可以把这个电离反应表示为:
X(g)+能量⟶X+(g)+e–
在这个方程中,X是任何原子或分子,而X+是从原子或分子中移除松散束缚电子的离子,而e-是被移除的电子。一般来说,这是一个吸热过程。通常,最外层的电子离原子核越远,电离能越低,反之亦然。
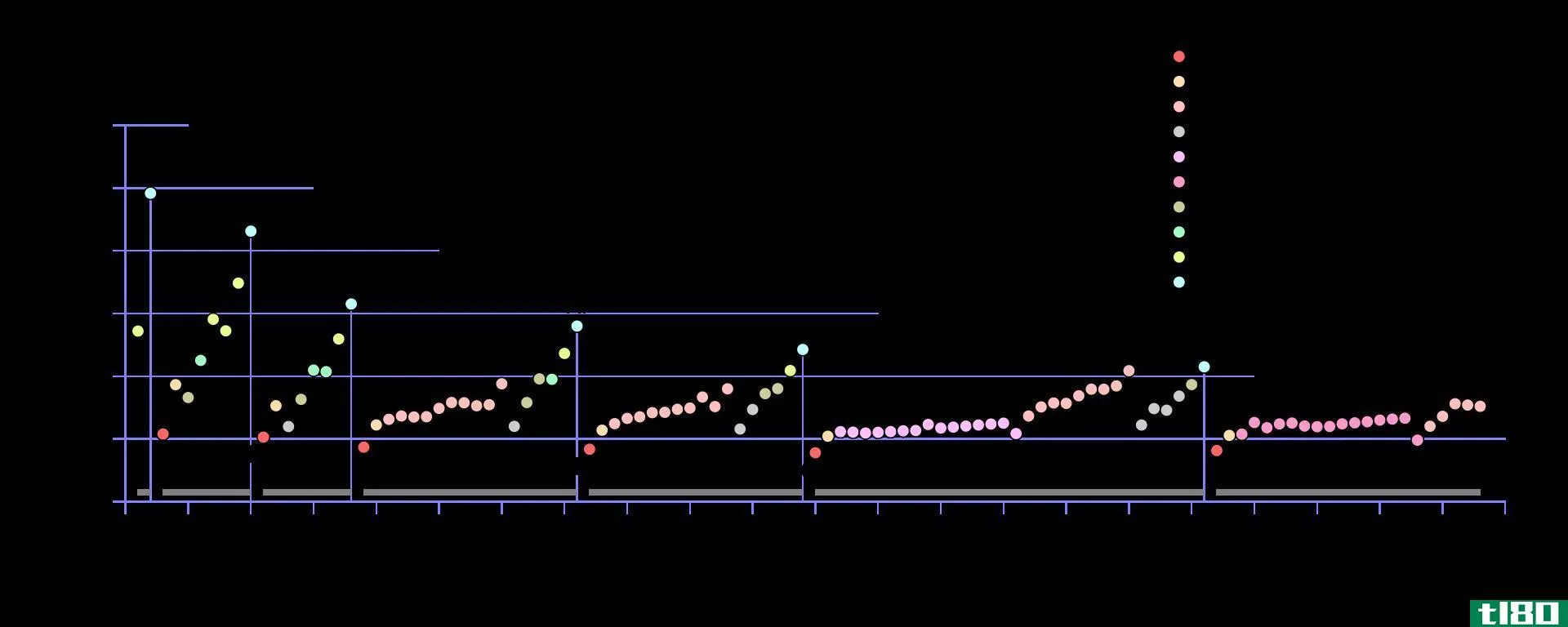
图01:元素周期表中的第一电离能趋势
在物理化学中,电离能以电子伏(eV)为单位表示。然而,这个单位通常不用于化学术语,因为我们计算的是“每摩尔”单位的值。因此,电离能的测量单位是千焦每摩尔(kJ/mol)。此外,在周期表中,电离能也有周期性的变化趋势,在给定的周期内,电离能通常从左到右递增,电离能一般从上到下依次递减。
什么是结合能(binding energy)?
结合能是从粒子系统中除去一个粒子所需的最小能量。我们也可以把它描述为将一个粒子系统分解成各个部分所需的最小能量。然而,在核物理中,使用的是分离能,而不是结合能。一般来说,束缚系统的能级比它的非束缚成分要低。
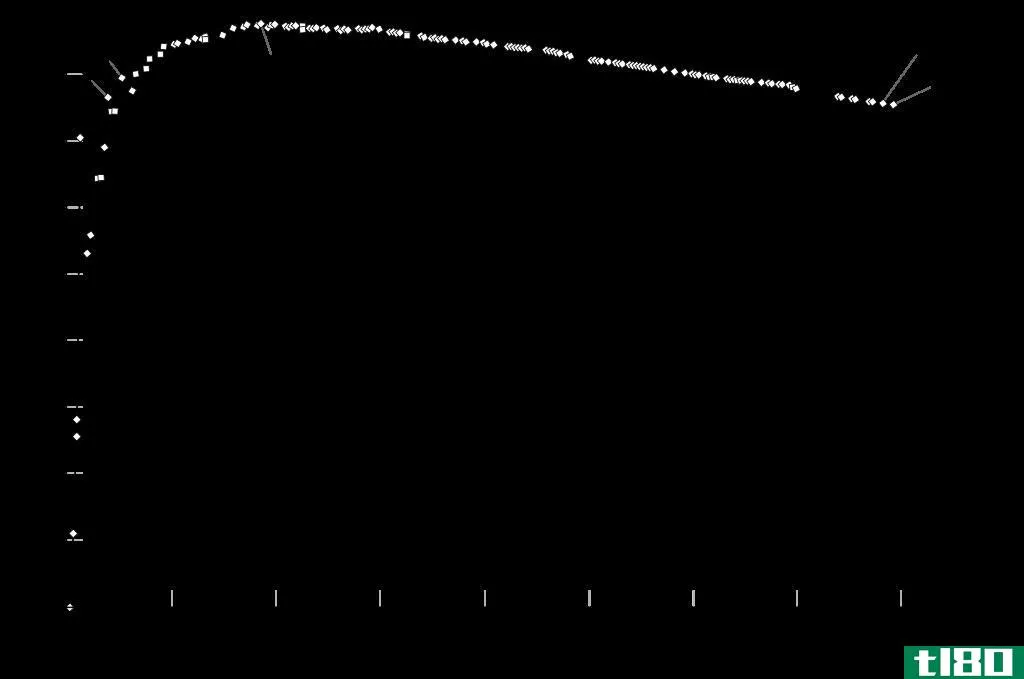
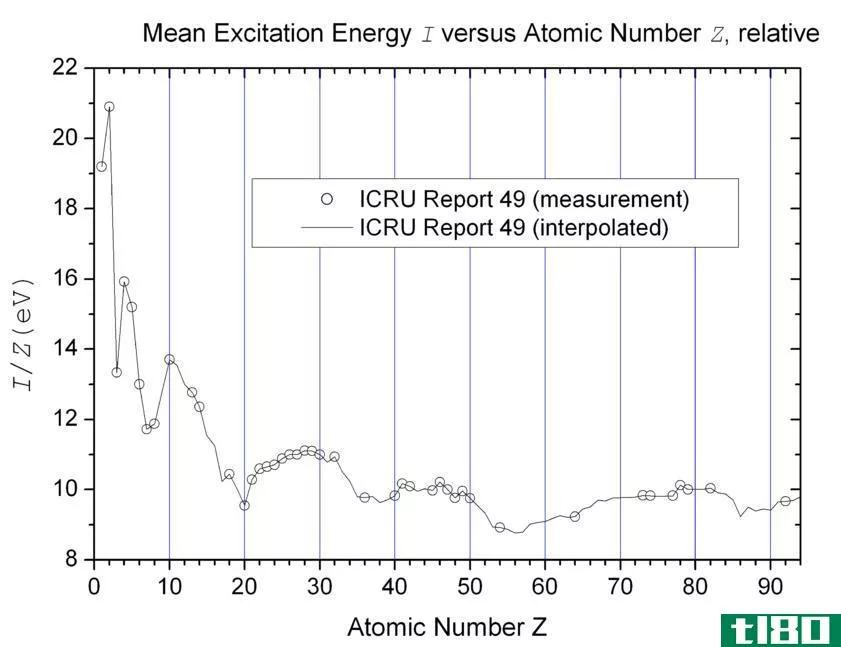
图02:不同化学元素的结合能曲线
结合能有不同类型:电子结合能或电离能、原子结合能、键离解能、核结合能、引力结合能等。
电离能(ionization energy)和结合能(binding energy)的区别
电离能是一种结合能。电离能和结合能的关键区别在于电离能是分离孤立的中性气体原子或分子中最松散束缚的电子所需的最小能量,而结合能是从粒子系统中移除粒子所需的最小能量。
下面是电离能和结合能的区别。
总结 - 电离能(ionization energy) vs. 结合能(binding energy)
电离能是一种结合能。电离能和结合能的关键区别在于,电离能是除去孤立的中性气体原子或分子中最松散束缚的电子所需的最小能量,而结合能是从粒子系统中移除粒子所需的最小能量。