第一(first)和二次电离能(i1e(second ionization energy (i1e)的区别
在分析第一电离能和第二电离能的区别之前,让我们先讨论电离能是什么。一般来说,电离能是指从气态原子或离子中除去电子所需的能量。由于电子被吸引到正原子核上,需要为这个过程提供能量。这被认为是一个吸热过程。电离能用kJ-mol-1表示。第一电离能和第二电离能之间的关键区别在它们的定义中得到了最好的解释;中性气态原子吸收的产生+1带电荷离子(除去电子)的能量称为第一电离能,而带正电荷的(+1)气态离子吸收的能能能产生带+2电荷的离子称为第一电离能二次电离能。电离能计算为1摩尔的原子或离子。换句话说,第一电离能与中性气态原子有关,第二电离能与带(+1)电荷的气态离子有关。电离能的大小取决于原子核的电荷、原子核的电子形式的距离以及原子核和外层电子之间的电子数。
什么是第一电离能(first ionization energy (i1e))?
第一电离能定义为1mol中性气态原子吸收的能量,以除去原子中最松散束缚的电子,产生1mol带+1电荷的气态离子。在周期表中,第一电离能的大小随着周期表中一个周期的增加而减小。第一电离能具有周期性,在周期表上有相同的重复模式。
什么是二次电离能(second ionization energy (i2e))?
The second ionization energy is defined as the energy absorbed by 1 mol of positively charged gaseous i*** to produce 1 mol of gaseous i*** with a +2 charge, by removing the loosely bound electron from the +1 ion. Second ionization energy also shows periodicity.
第一(first)和二次电离能(i1e(second ionization energy (i1e)的区别
第一和第二电离能的定义
从1到1的气态离子中释放出大部分的正离子。
X(g)X+(g)+e-
(1摩尔)(1摩尔)(1摩尔)
二次电离能(I2E):从带+1电荷的1摩尔气态离子中除去最松散束缚的电子以产生带+2电荷的摩尔气态离子所需的能量。
X+(g)X2+(g)+e–
(1摩尔)(1摩尔)(1摩尔)
一、二电离能特性
能量需求
通常,从基态气态原子中排出第一个电子比从带正电荷的离子中排出第二个电子要容易得多。因此,第一电离能小于第二电离能,第一电离能与第二电离能之间的能量差很大。
| 元素 | 第一电离能(I1E)/kJ mol-1 | 二次电离能(I2E)/kJ mol-1 |
| 氢(H) | 1312 | 目标 |
| 氦(He) | 2372 | 5250 |
| 锂(Li) | 520 | 7292 |
| 铍(Be) | 899 | 1757 |
| 硼(B) | 800 | 2426 |
| 碳(C) | 1086 | 2352 |
| 氮(N) | 1402 | 2855 |
| 氧气(O) | 1314 | 3388 |
| 氟(F) | 680 | 3375 |
| 霓虹灯(Ne) | 2080 | 3963 |
| 钠(Na) | 496 | 4563 |
| 镁(Mg) | 737 | 1450 |
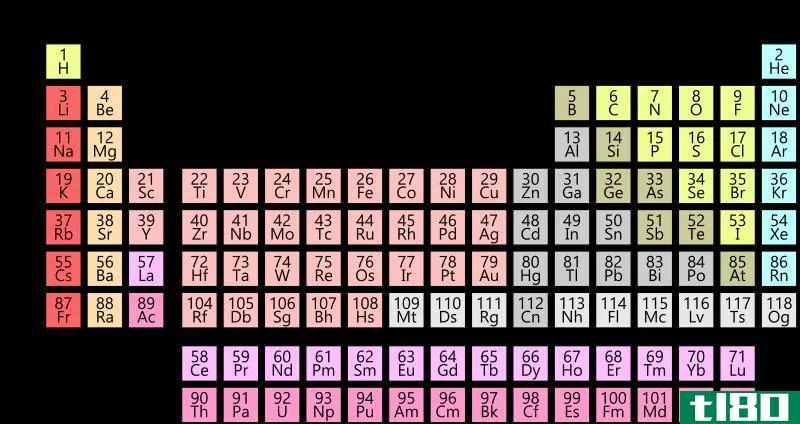
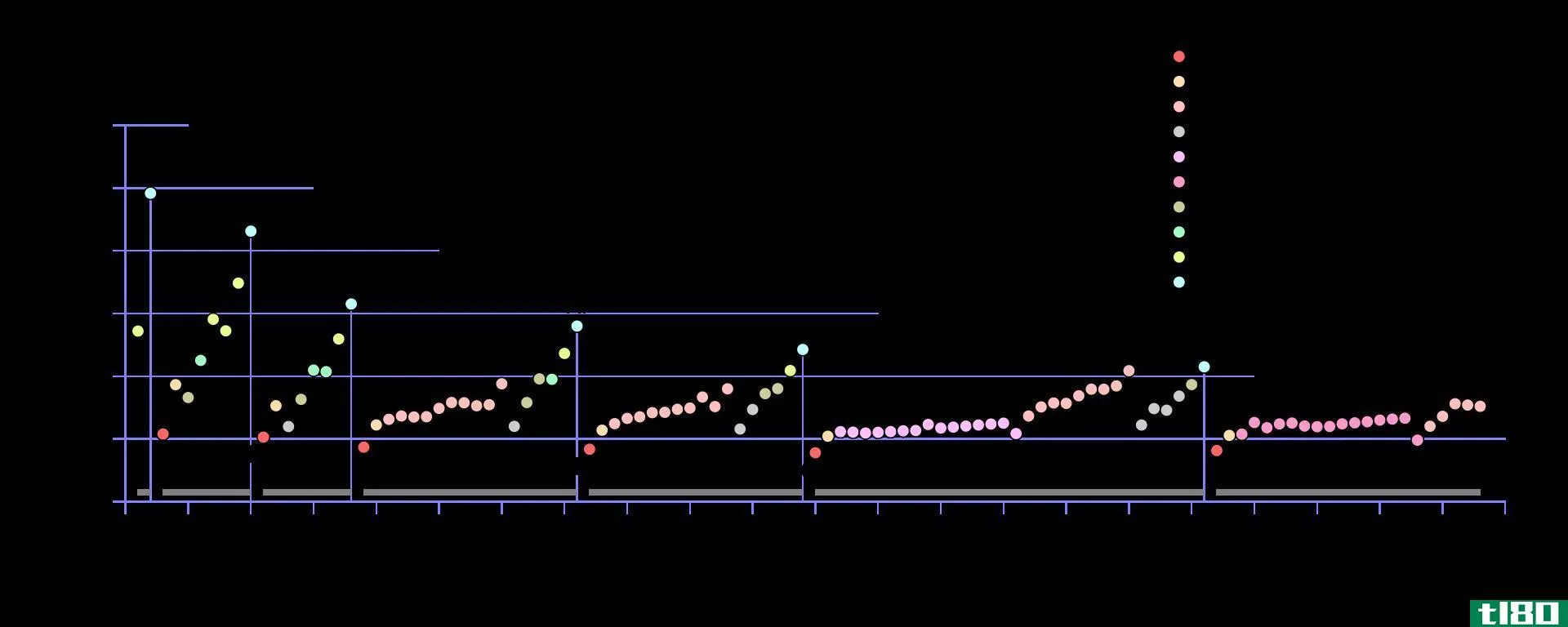
周期表中电离能的变化趋势
第一电离能(I1E):原子在每个周期的第一电离能值都呈现相同的变化。量级总是小于第二电离能值
“Ionization energy periodic table” by Cdang and Adrignola. (CC BY-SA 3.0) via Wikimedia Comm***