一级反应和二级反应的关键区别在于,一级反应的速率取决于速率方程中反应物浓度的一次方,而二级反应的速率取决于速率方程中浓度项的二次方。
反应级数是速率定律方程中反应物浓度升高到的幂次之和。根据这一定义,反应有几种形式:零级反应(这些反应不取决于反应物的浓度)、一级反应和二级反应。
目录
1. 概述和主要区别
2. 什么是一级反应
3. 什么是二级反应
4. 并列比较-表格形式的一级反应与二级反应
5. 摘要
什么是一级反应(first order reacti***)?
一级反应是一种化学反应,其反应速率取决于参与反应的一种反应物的摩尔浓度。因此,根据上述反应级数的定义,速率定律方程中反应物浓度升高的幂次之和始终为1。可以有一个单一的反应物参与这些反应。反应物的浓度决定了反应的速率。但有时,有不止一种反应物参与这些反应,那么其中一种反应物将决定反应速率。
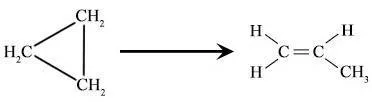
让我们考虑一个例子来理解这个概念。在N2O5的分解反应中,生成NO2和O2气体。由于它只有一个反应物,我们可以写出反应和速率方程如下。
2N2O5(g)→4NO2(g)+O2(g)
速率=k[N2O5(g)]m
这里k是这个反应的速率常数,m是反应的级数。因此,根据实验测定,m值为1。因此,这是一个一级反应。
什么是二级反应(second order reacti***)?
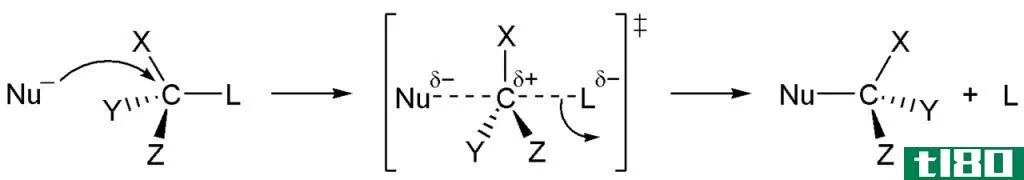
二级反应是化学反应,其反应速率取决于两个反应物的摩尔浓度或一个反应物的二次幂。因此,根据上述反应级数的定义,速率定律方程中反应物浓度升高到的幂之和总是2。如果有两种反应物,反应速率将取决于每种反应物浓度的一次方。
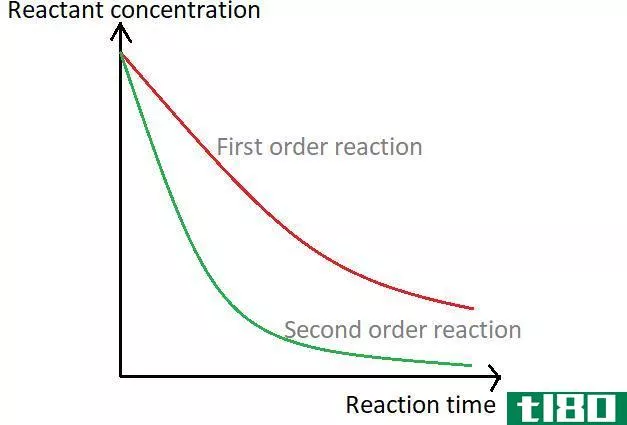
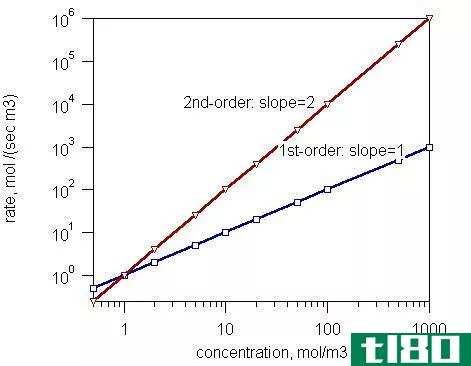
用图01比较两种反应物的反应时间顺序。
如果我们把一个反应物的浓度增加2倍(如果速率方程中有两个反应物),那么反应速率增加4倍。例如,让我们考虑以下反应。
2A→P
这里A是反应物,P是产物。如果这是一个二级反应,这个反应的速率方程如下。
速率=k[A]2
但是对于两种不同反应物的反应,如下所示:;
A+B→P
速率=k[A]1[B]1
第一(first)和二级反应(second order reacti***)的区别
一级反应是一种化学反应,其反应速率取决于参与反应的一种反应物的摩尔浓度。因此,如果我们把反应物的浓度增加2倍,反应速率就会增加2倍。二级反应是化学反应,其反应速率取决于两个反应物的摩尔浓度或一个反应物的二次幂。因此,如果我们把反应物的浓度增加2倍,反应速率就会增加4倍。下面的信息图以表格形式展示了一阶和二阶反应之间的差异。

总结 - 第一(first) vs. 二级反应(second order reacti***)
根据反应的顺序,有三种主要的反应类型:零级反应、一级反应和二级反应。一级反应和二级反应的关键区别在于,一级反应的速率取决于速率方程中反应物浓度的一次方,而二级反应的速率取决于速率方程中浓度项的二次方。