电离(ionization)和离解(dissociation)的区别
离子化和离解是化学中两个重要的过程。离子化和离解经常被混淆,特别是在离子化合物溶解的情况下。人们可能认为溶解离子化合物会导致电离,因为离子化合物溶解在水中,产生带电粒子或离子。但这是一个离解的例子,因为离子化合物已经由离子组成。因此,离子化和离解的关键区别在于电离是通过电子的获得或损失而产生新的离子,而离解是化合物中已经存在的离子的分裂或分离。
内容1。概述和主要区别2。什么是电离3。什么是分离4。并排比较——电离与解离5。摘要
什么是电离(ionization)?
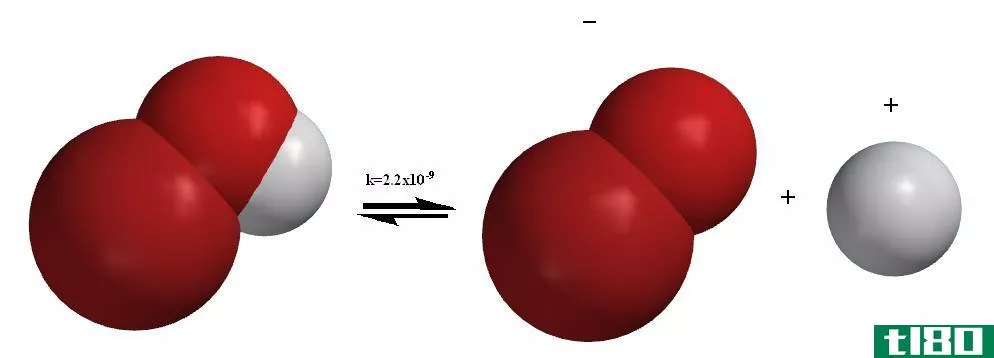
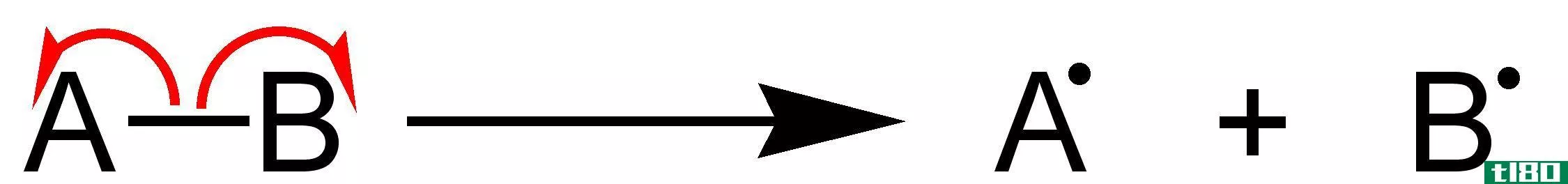
电离是通过电子的增加或减少而产生带电荷的原子或分子的过程。这个过程产生带电粒子。在这个过程中,电中性原子变成带电粒子。这个电荷可以是正的也可以是负的。这取决于电子的增益或损耗。如果一个原子或一个分子失去一个电子,它就会带正电荷,而如果它从外部获得一个电子,它就会带负电。电离过程通常是不可逆的,这意味着,如果一个原子或分子获得了一个电子,它不会释放出那个电子;如果一个原子失去了一个电子,它就不会拿回一个电子。当这个电子的损失或增加产生一个稳定的离子时,就会发生这种情况,这个离子遵循八位体规则。
有时电离这个词会和离解混淆。如果考虑到像氯化钠(NaCl)这样的离子化合物,它在水中溶解时会形成离子。虽然这会形成离子,但这不是电离。因为它的离子键不能分裂成固体,所以称之为离子键。因此,离子键的分裂不是一个电离过程,因为一个电子已经被另一个原子给了一个原子,只有一个静电引力存在。因此,可以说,具有离子键的化合物不会参与电离。虽然离子化合物不能电离,但原子间有共价键的共价化合物可以经历电离过程。在以前的化合物中,由于这些化合物中的共享电子会产生新的离子化,而在这些新的化合物中又会出现共价键。但电离只发生在极性共价化合物中,原子的电负性差别很大。否则,强共价键就不会发生电离。金属中也会发生电离。在那里,带正电荷的金属离子是通过从金属原子中释放电子而产生的。
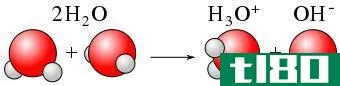
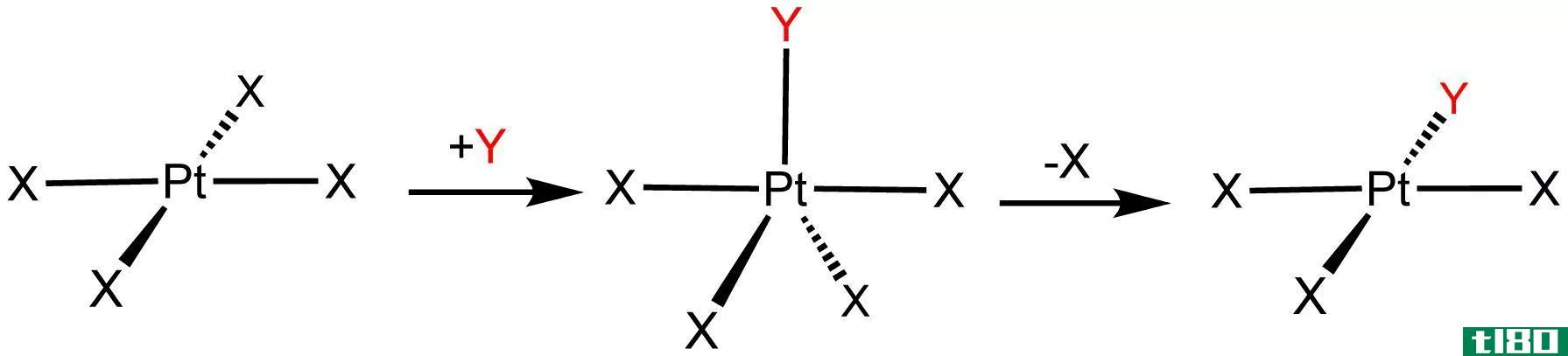
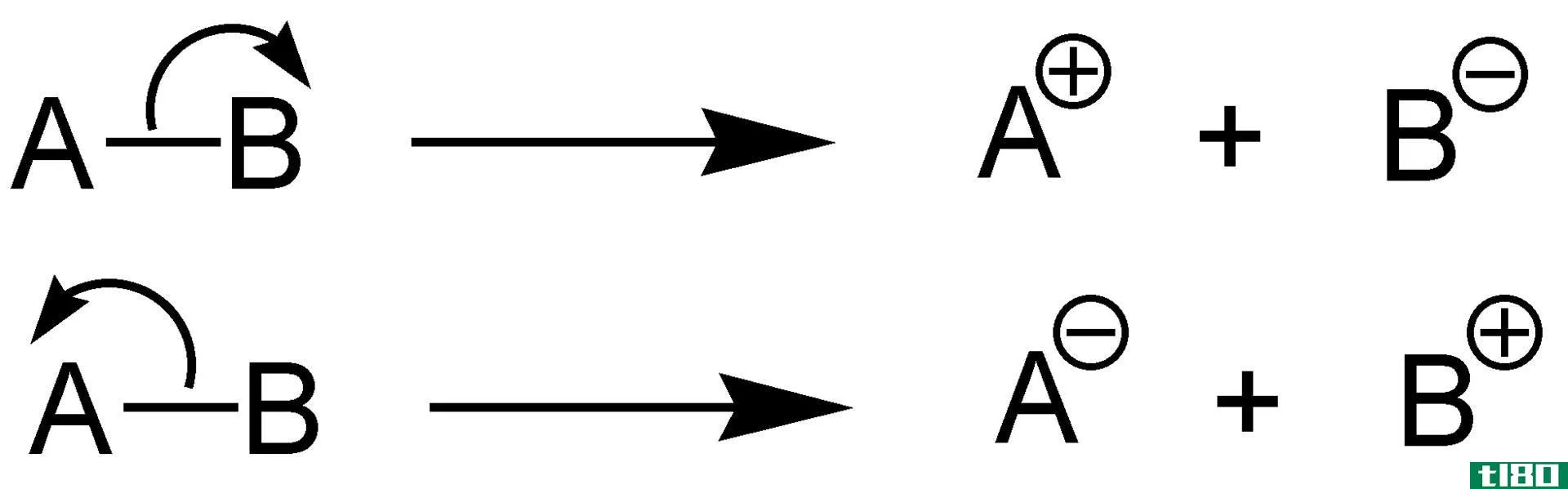
图01:电离
什么是离解(dissociation)?
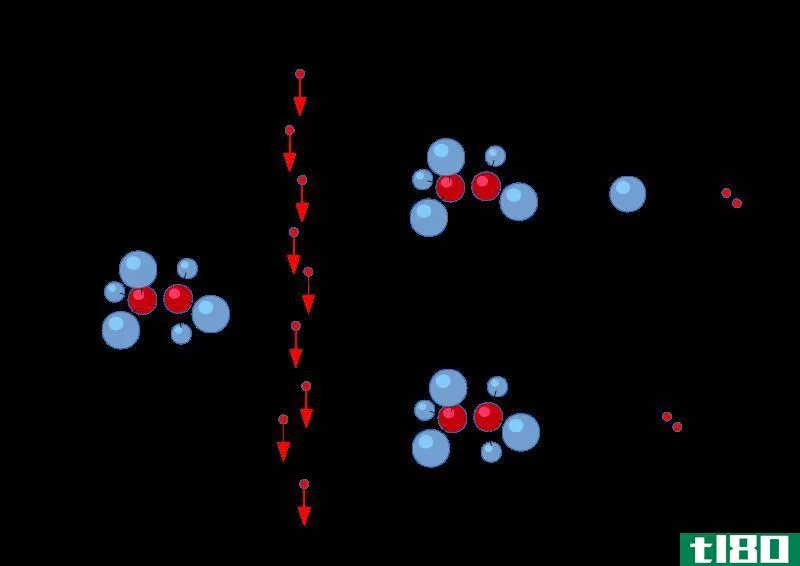
离解是指化合物分解成更小的粒子。离解过程可以产生带电或中性的产物。这并不涉及原子获得或失去电子。与电离过程不同,离解是化合物中已经存在的离子的分离。有时,离解也会产生中性粒子。例如,N2O4的分解会产生两个NO2分子。解离过程在大多数情况下是可逆的。这意味着,分离的离子可以重新排列以产生先前的化合物。例如,如上所述,氯化钠的溶解是一个离解过程,它产生两个带电粒子。但是,在一定的条件下,可以再次得到固体NaCl,证明了解离是可逆的。与电离不同,离解发生在离子化合物中。
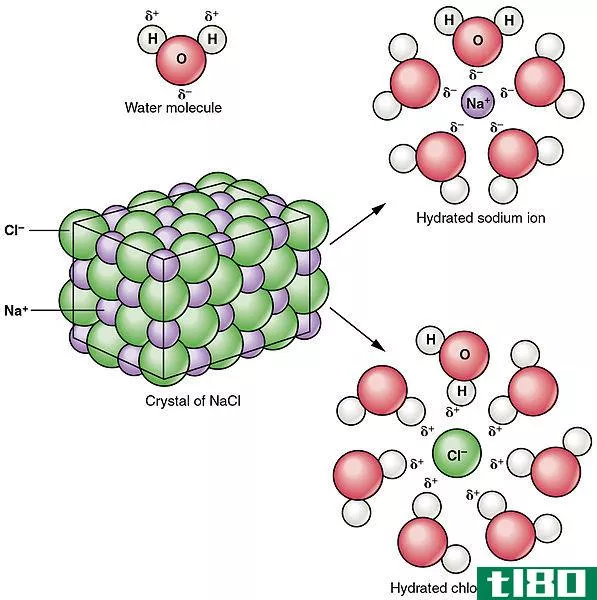
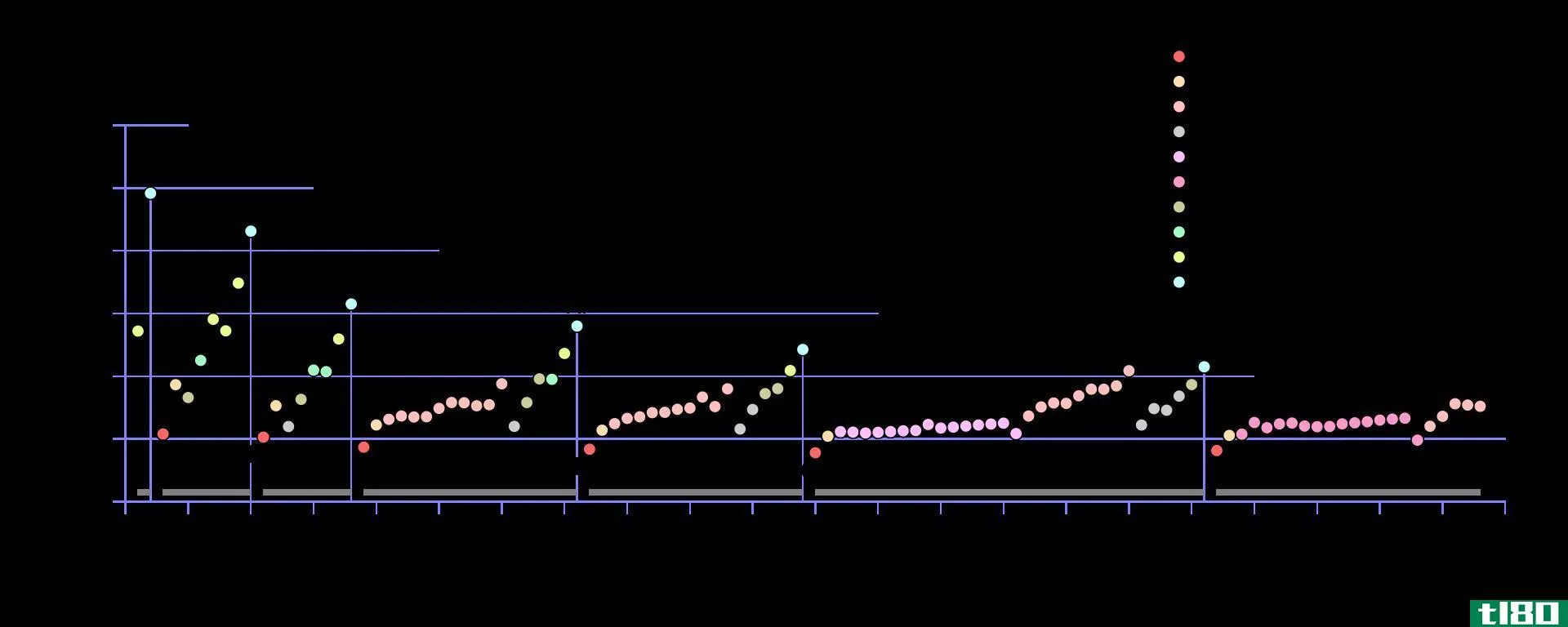
图02:水中氯化钠的离解
电离(ionization)和离解(dissociation)的区别
| 电离与解离 | |
| 电离是产生新的带电粒子的过程。 | 离解是化合物中已经存在的带电粒子的分离。 |
| 初始化合物 | |
| 电离涉及极性共价化合物或金属 | 离解涉及离子化合物。 |
| 产品 | |
| 电离总是产生带电粒子 | 离解产生带电粒子或电中性粒子。 |
| 过程 | |
| 电离过程是不可逆的。 | 解离是可逆的。 |
| 债券 | |
| 电离涉及原子间的共价键 | 离解涉及化合物中的离子键。 |
总结 - 电离(ionization) vs. 离解(dissociation)
电离和解离是两个不同的过程。因此,了解这两个过程之间的区别是非常重要的。离子化和离解的关键区别在于离解是将化合物中已经存在的带电粒子分离的过程,而离子化则是形成新的带电粒子,而这些粒子在以前的化合物中是不存在的。
R参考文献:1。Hamza,S.A.,2014年。幻灯片共享。[在线]网址:https://www.slideshare.net/sheikhamirhamza/dsassociation-vs-ionizationppt[访问日期:2017年5月29日].2。Chang,R.,2010年。化学。第10版,纽约:麦格劳希尔。