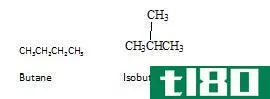
同素异形体和同位素的主要区别在于同素异形体是在分子水平上考虑的,而同位素是在原子水平上考虑的。
根据原子序数,周期表中大约有118个元素。元素是一种只由单一原子组成的化学物质,因此它们是纯的。同素异形体是同一化合物的不同形式,而同位素是同一元素的不同形式。
目录
1. 概述和主要区别
2. 什么是同素异形体
3. 什么是同位素
4. 并列比较-同素异形体与同位素的表格形式
5. 摘要
什么是同素异形体(allotropes)?
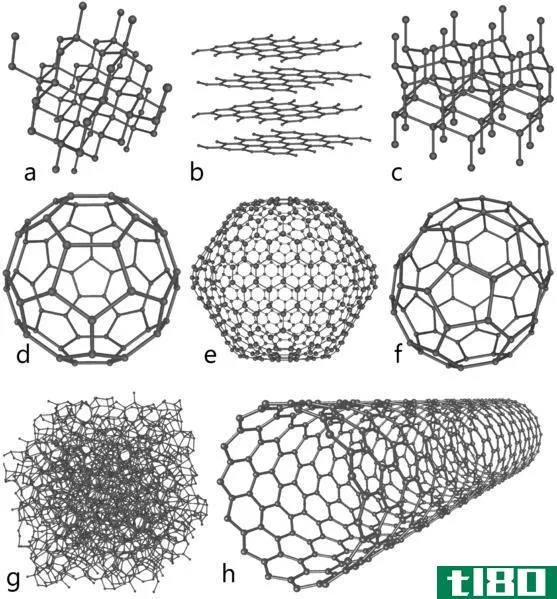
同一分子水平上的同素异形体是不同的。它们表现出不同的物理性质。在所有的化学元素中,碳、氧、硫和磷是具有同素异形体的主要元素。碳有大量的同素异形体。碳的八个同素异形体之间差别很大。例如,金刚石是碳中最强的同素异形体,而石墨则不那么牢固。碳纳米管、富勒烯和无定形碳是碳的其他同素异形体。
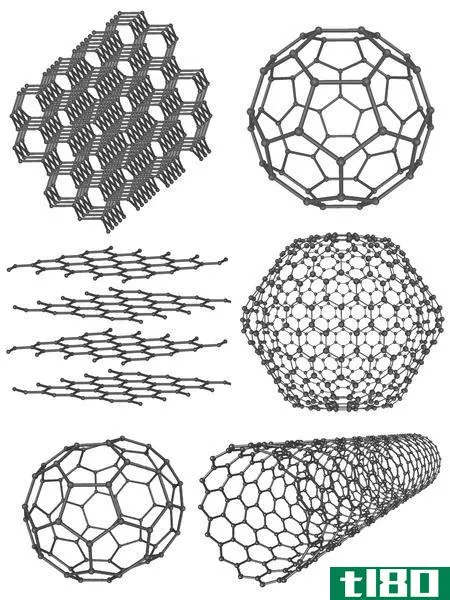
图1:碳的同素异形体
对于氧元素,有两种常见的同素异形体,即O2和O3。O2比O3丰富。通常,在自然界中,一些同素异形体由于其稳定性而比其他同素异形体更丰富。磷有红磷、白磷和黑磷三种同素异形体。其中红磷和白磷最为常见。同素异形体因原子排列、原子数目等而不同。
什么是同位素(isotopes)?
同位素是同一化学元素的不同形式的原子。它们彼此不同,因为它们有不同数量的中子。由于中子数不同,它们的质量数也不同。
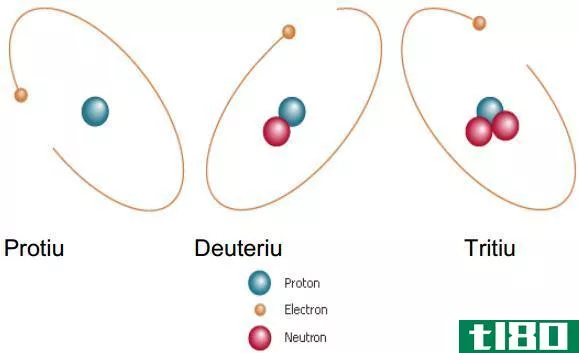
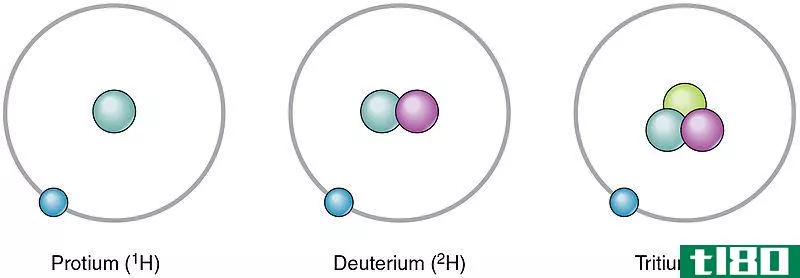
然而,同一元素的同位素具有相同数量的质子和中子。不同的同位素以不同的数量存在,我们可以用一个称为相对丰度的百分比来表示。例如,氢有三种同位素,如钚、氘和氚。它们的中子数和相对丰度如下。

图2:化学元素氢的不同同位素
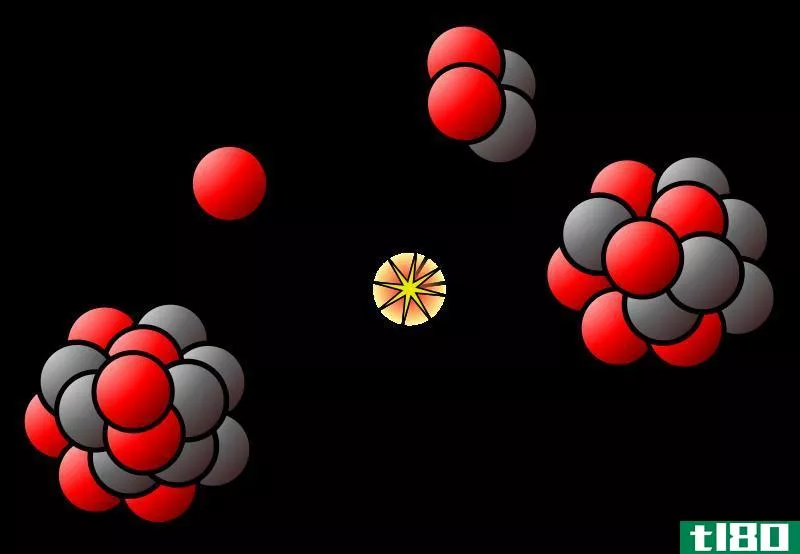
一个原子核所能容纳的中子数因元素而异。在这些同位素中,只有一些是稳定的。例如,氧有三种稳定同位素,锡有十种稳定同位素。大多数情况下,简单元素的中子数和质子数相同。但是,在重元素中,中子比质子多。中子数对平衡原子核的稳定性很重要。当原子核太重时,它们就会变得不稳定;因此,这些同位素就具有放射性。例如,238U发出辐射,衰变成更小的原子核。同位素由于质量不同,可能有不同的性质。例如,它们可能有不同的自旋,因此它们的核磁共振波谱也不同。然而,它们的电子数是相似的,因此产生了相似的化学行为。
同素异形体(allotropes)和同位素(isotopes)的区别
同一分子水平上的同素异形体是不同的。同位素是同一化学元素的不同形式的原子。同素异形体和同位素的关键区别在于同素异形体是在分子水平上考虑的,而同位素是在原子水平上考虑的。此外,同素异形体和同位素之间的另一个不同之处在于,同素异形体在原子排列方式上各不相同,而同位素在中子数上却各不相同。
下面的信息图显示了同素异形体和同位素之间差异的更多细节。

总结 - 同素异形体(allotropes) vs. 同位素(isotopes)
尽管同素异形体和同位素这两个词听起来很相似,但根据它们的含义,它们是截然不同的。同素异形体和同位素的关键区别在于同素异形体是在分子水平上考虑的,而同位素是在原子水平上考虑的。
引用
1Helmenstine,Anne Marie,“同素异形体的定义和示例”,ThoughtCo,2019年1月13日,可在此处查阅。Helmenstine,Anne Marie,“化学中的同位素定义和示例”,ThoughtCo,2018年10月22日,可在此处查阅。
2Helmenstine,Anne Marie,“化学中的同位素定义和示例”,ThoughtCo,2018年10月22日,