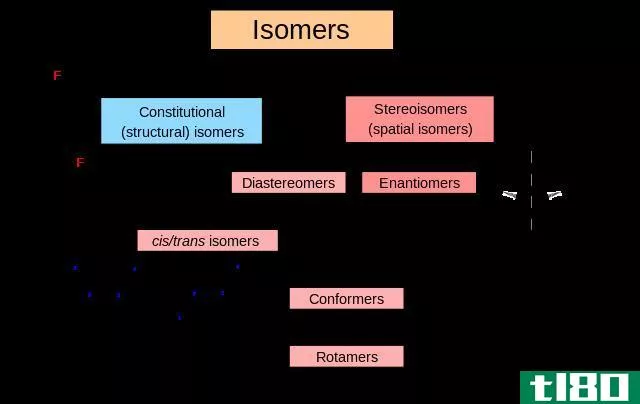
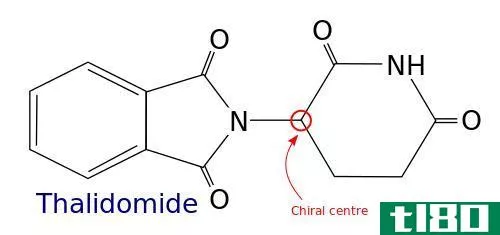
氨基酸手性
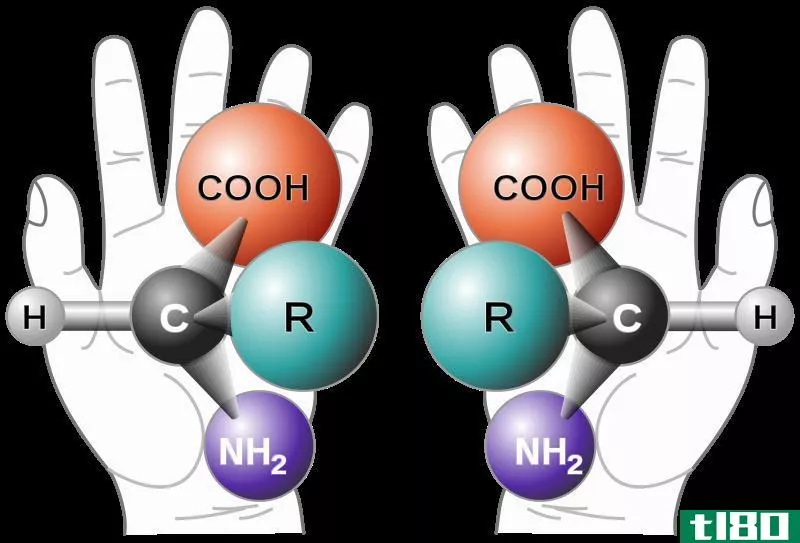
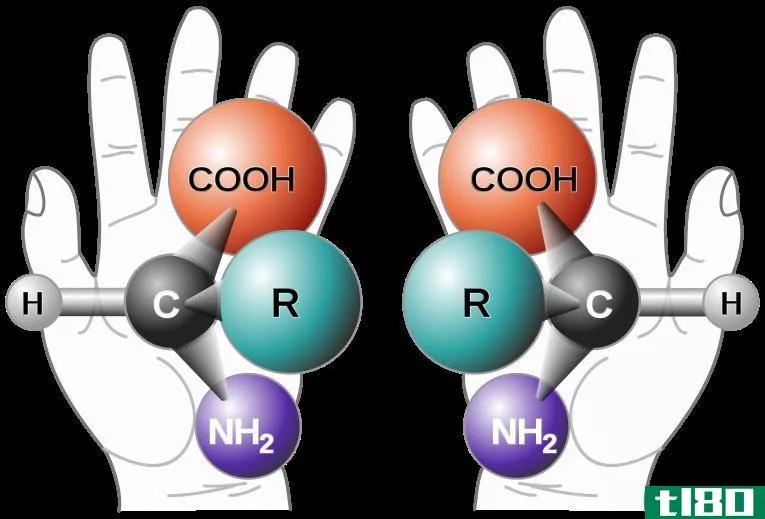
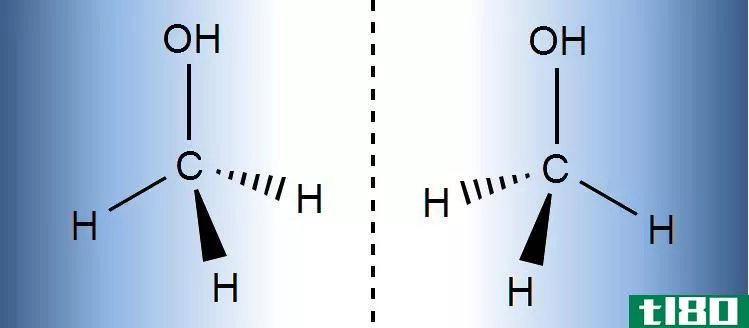
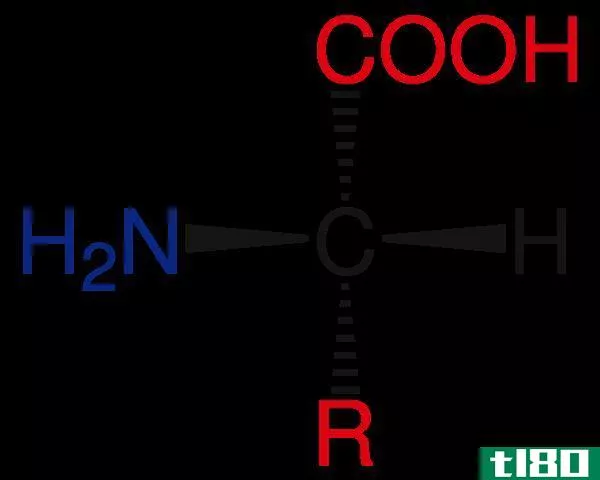
氨基酸(除了甘氨酸)在羧基(CO2-)附近有一个手性碳原子。这个手性中心允许立体异构。氨基酸形成两个立体异构体,它们是彼此的镜像。这些结构不能相互叠加,就像你的左手和右手一样。这些镜像称为对映体。

氨基酸手性的d/l和r/s命名约定
对映体有两个重要的命名系统。D/L系统基于光学活性,指的是拉丁语单词dexter(右)和laevus(左),反映了化学结构的左右利手性。具有右旋构型(右旋)的氨基酸将以(+)或D前缀命名,例如(+)-丝氨酸或D-丝氨酸。具有laevus构型(左旋)的氨基酸将以(-)或L开头,例如(-)-丝氨酸或L-丝氨酸。
以下是确定氨基酸是D对映体还是L对映体的步骤:
- 把分子画成费歇尔投影,上面是羧酸基团,下面是侧链。(胺基不在顶部或底部。)
- 如果胺基位于碳链的右侧,则化合物为D。如果胺基位于左侧,则分子为L。
- 如果你想画一种氨基酸的对映体,只需画它的镜像。
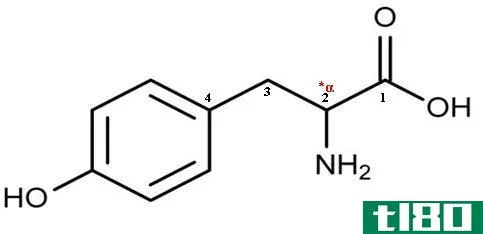
R/S符号与之类似,其中R代表拉丁直肌(右、正或直),S代表拉丁黑体(左)。R/S命名遵循Cahn Ingold Prelog规则:
- 定位手性或立体基因中心。
- 根据连接到中心的原子的原子序数为每个组分配优先级,其中1=高,4=低。
- 按照高优先级到低优先级(1到3)的顺序确定其他三组的优先级方向。
- 如果顺序为顺时针,则中心为R。如果顺序为逆时针,则中心为S。
尽管大多数化学已转换为(S)和(R)指示符,用于对映体的绝对立体化学,但氨基酸通常使用(L)和(D)系统命名。
天然氨基酸的异构性
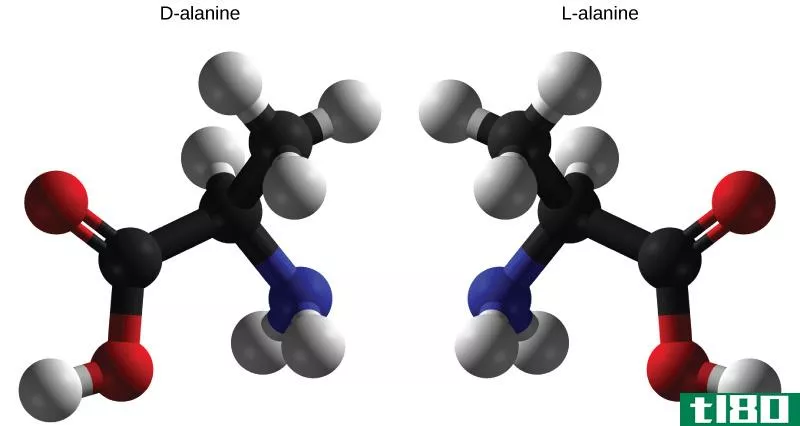
在蛋白质中发现的所有氨基酸都以手性碳原子的L-构型存在。甘氨酸是一个例外,因为它在α碳上有两个氢原子,除非通过放射性同位素标记,否则不能相互区分。
D-氨基酸并非天然存在于蛋白质中,也不参与真核生物的代谢途径,尽管它们在细菌的结构和代谢中很重要。例如,D-谷氨酸和D-丙氨酸是某些细菌细胞壁的结构成分。人们相信D-丝氨酸可能是一种大脑神经递质。存在于自然界的D-氨基酸是通过蛋白质的翻译后修饰产生的。
关于(S)和(R)命名法,蛋白质中几乎所有的氨基酸都位于α碳位。半胱氨酸是(R),甘氨酸不是手性的。半胱氨酸不同的原因是它在侧链的第二个位置有一个硫原子,它的原子序数比第一个碳原子上的基团的原子序数大。按照命名惯例,这使得分子(R)而不是(S)。
- 发表于 2021-09-11 17:09
- 阅读 ( 357 )
- 分类:化学
你可能感兴趣的文章
手性(chirality)和螺旋度(helicity)的区别
...不同的原子团,形成四个单一的共价键。 图01:一个普通氨基酸的两个手性对映体 手性中心导致化合物的光学异构。换句话说,具有手性中心的化合物不会与其镜像叠加。因此,具有手性中心的化合物和与其镜像相似的分子是...
- 发布于 2020-10-11 11:44
- 阅读 ( 563 )
异构化(epimerization)和外消旋化(racemization)的区别
...构化和外消旋化的关键区别在于,差向异构化涉及到向其手性对应物的转化,而外消旋则是将光学活性物种转化为光学不活跃物种。 异构化和消旋化是化学转化。它们在过程、最终产物、反应条件等方面都有不同之处,即差向...
- 发布于 2020-10-15 06:01
- 阅读 ( 591 )
立体中心(stereocenter)和手性中心(chiral center)的区别
立体中心和手性中心的关键区别在于,当两个基团在这个点上交换时,立体中心是分子中任何一个能产生立体异构体的点,而手性中心是分子中的一个原子,当这个中心的两个基团互换时,它能产生一个对映体。 立体中心和...
- 发布于 2020-10-18 18:28
- 阅读 ( 1365 )
非致命的(achiral)和中观(meso)的区别
关键区别-非致命伤与中耳炎 非手性与meso的主要区别在于非手性化合物没有手性中心,而meso化合物具有多个手性中心。 手性中心是有机分子中的一个碳原子,它有四个不同的取代基。换言之,分子中存在手性中心表明分子在...
- 发布于 2020-10-18 20:00
- 阅读 ( 232 )
我(l)和d氨基酸(d amino acids)的区别
主要区别——l和d氨基酸 L氨基酸和D氨基酸是氨基酸的两种形式。L和D氨基酸之间的关键区别在于,L氨基酸是能够逆时针旋转平面偏振光(左侧)的氨基酸的对映体,而D氨基酸是能够顺时针旋转平面偏振光(右侧)的氨基酸...
- 发布于 2020-10-19 04:46
- 阅读 ( 353 )
左边(left)和右旋氨基酸(right handed amino acids)的区别
左右手氨基酸的关键区别在于,左旋氨基酸的胺基出现在分子的左手侧,而右手侧氨基酸的胺基则在分子的右手侧。 手性是有机化学中的一个重要现象。它描述了一个碳原子的存在,它有四个不同的基团。也就是说,手性化...
- 发布于 2020-10-21 21:49
- 阅读 ( 754 )
谷氨酰胺(glutamine)和l-谷氨酰胺(l-glutamine)的区别
谷氨酰胺与L-谷氨酰胺 氨基酸是由C、H、O、N和S组成的简单分子,它具有以下一般结构。 大约有20种常见的氨基酸。所有的氨基酸都有一个-COOH、-NH2基团和a-H键合到碳上。碳是一种手性碳,α-氨基酸是生物界最重要的。D-氨...
- 发布于 2020-10-24 17:25
- 阅读 ( 173 )
l-酪氨酸(l-tyrosine)和酪氨酸(tyrosine)的区别
...振光的能力。酪氨酸是一种具有生物活性的天然非必需α-氨基酸。由于在手性碳原子周围形成两种不同的对映体,它可以以两种异构体形式出现。它们分别被称为L形和D形,或分别相当于左手和右手的构型。这些L型和D型被称为...
- 发布于 2020-10-24 23:23
- 阅读 ( 285 )
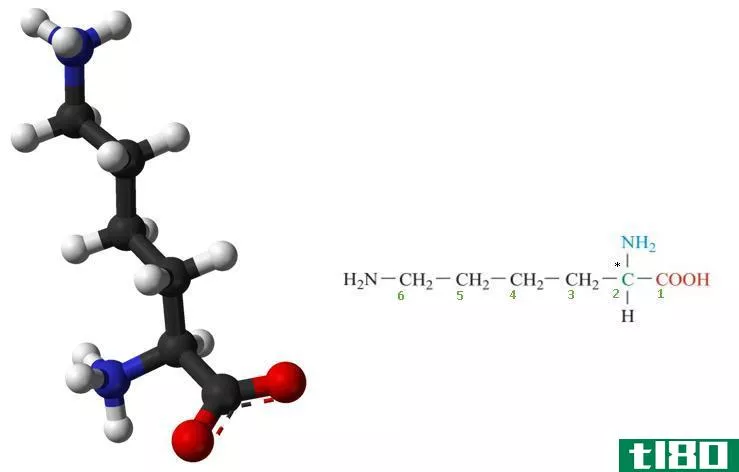
赖氨酸(lysine)和赖氨酸(l-lysine)的区别
...(lysine)和赖氨酸(l-lysine)的区别 赖氨酸和赖氨酸都是两种氨基酸,它们具有相同的物理性质,但它们之间有一些区别。赖氨酸和赖氨酸之间的关键区别在于能够旋转平面偏振光。赖氨酸是一种具有生物活性的天然必需α-氨基酸。...
- 发布于 2020-10-28 22:29
- 阅读 ( 346 )
美国宇航局的“化学笔记本电脑”可以帮助未来的探测器在外星行星上寻找生命
...标:找到与生命有关的分子。特别是,它被设计用来寻找氨基酸和脂肪酸,它们分别是地球生命中蛋白质和细胞膜的关键。 在火星或其他地方获得的样品需要先溶解在水中,然后才能进行分析。这种化学笔记本电脑使用的东...
- 发布于 2021-05-02 14:10
- 阅读 ( 143 )