氡和镭的主要区别在于氡是一种惰性气体,而镭是一种放射性元素。
虽然氡和镭的名字听起来很相似,但它们是完全不同的化学元素。它们以不同的物理状态出现。然而,由于原子序数大,这两种元素都是放射性元素。
目录
1. 概述和主要区别
2. 什么是氡
3. 什么是镭
4. 并列比较——表格形式的氡与镭
5. 摘要
什么是氡(radon)?
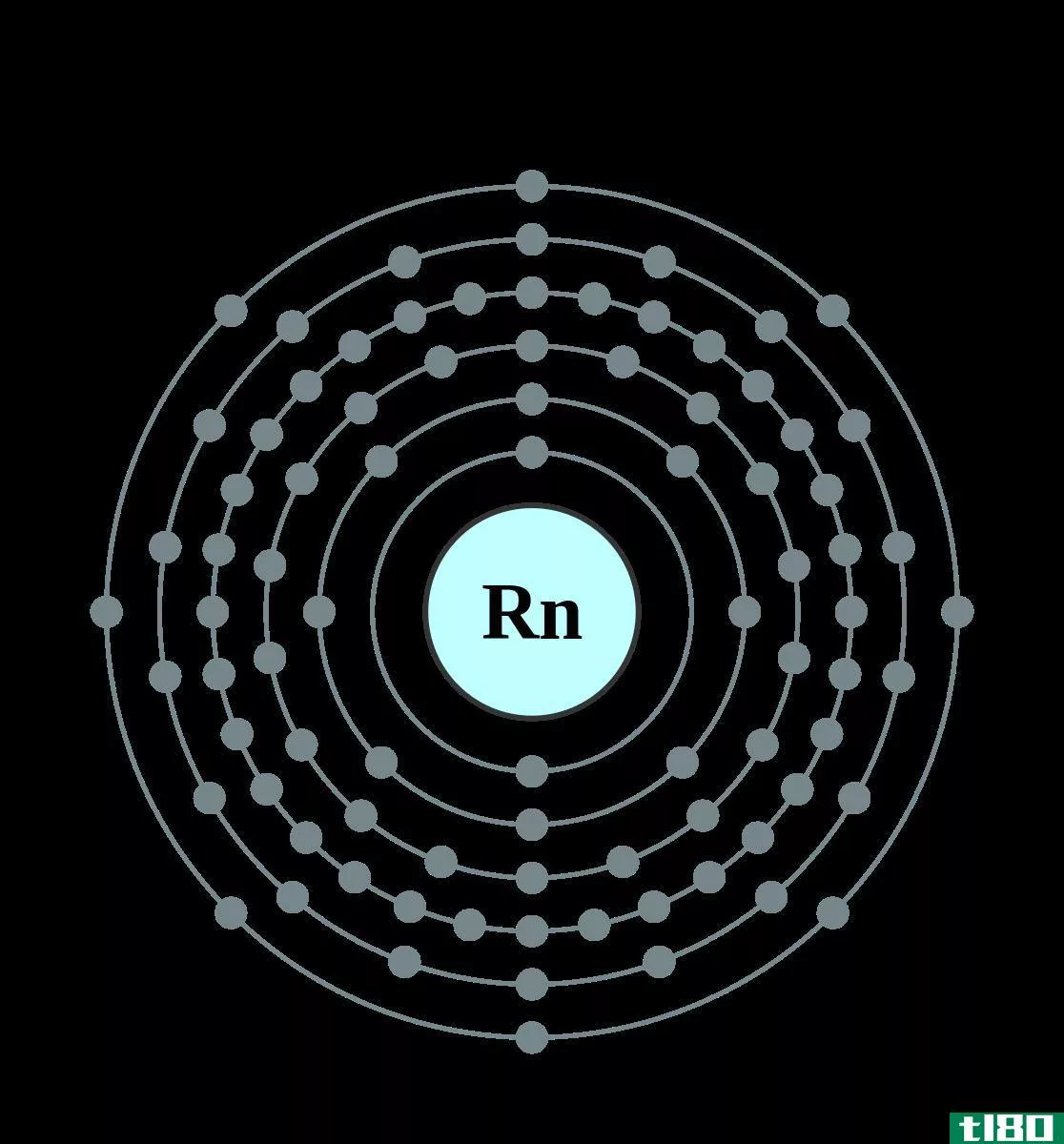
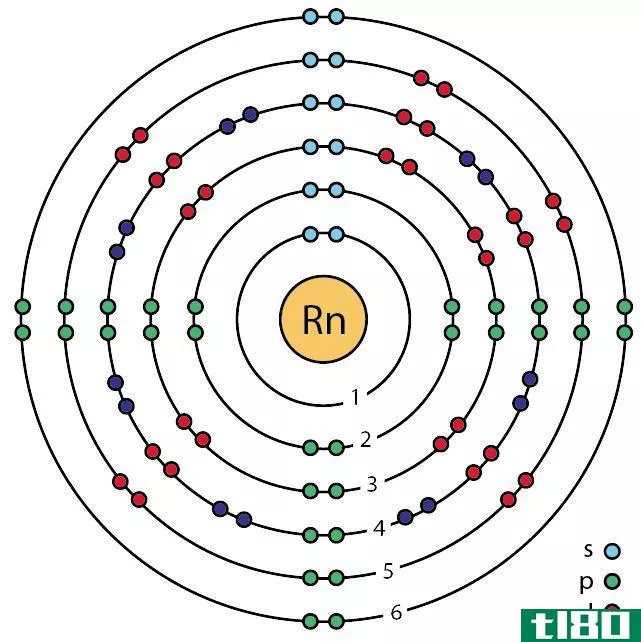
氡是一种稀有气体,化学符号为Rn,原子序数为86。它是一种放射性元素,因为它的原子序数大,使它不稳定。它是一种无色、无味、无味的惰性气体。自然,这种元素出现在钍和铀放射性衰变的中间阶段。氡是镭的中间衰变产物。氡最常见和最稳定的同位素的原子质量是222。然而,这种稳定同位素的半衰期约为3.8天。由于氡衰变很快,它是地球上最稀有的化学元素之一。
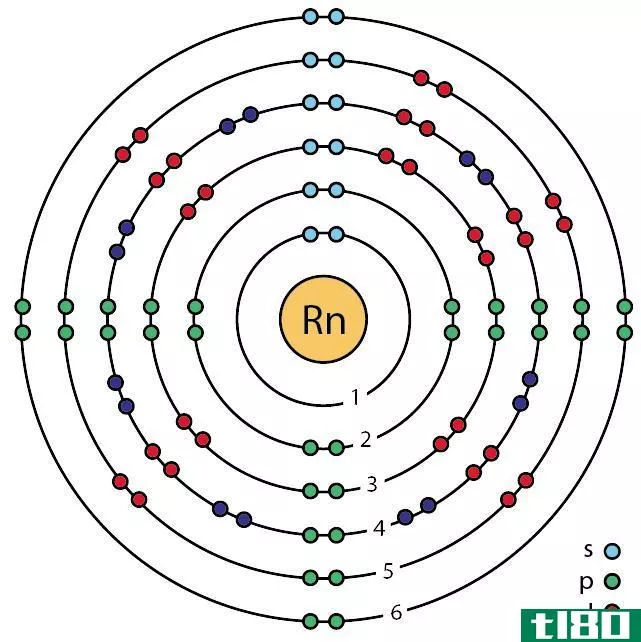
图01:氡
氡是第18组和第6周期的p块元素。根据八位元规则,它有一个完整的电子结构。它的熔点和沸点都是负值,这使得它在室温和压力条件下是一种基本气体。此外,它还具有面心立方晶体结构。考虑到它的磁性,它是非磁性的,因为氡原子中没有未配对的电子。此外,它是密度最大的惰性气体,是惰性气体。
什么是镭(radium)?
镭是一种放射性化学元素,化学符号为Ra,原子序数为88。它被归类为碱土金属,因为它在周期表的第2组。在它纯净的状态下,它是白色的。一旦暴露在空气中,它很容易与氮反应,形成黑色的氮化镭。镭最稳定的同位素是Ra-226。这种同位素的半衰期大约是1600年。

图02:纯镭的外观
镭在周期表的第2组和第7周期中。它是一个s-block元素。它完全充满了原子轨道,但它没有所有的电子都服从八位元定律。在标准温度和压力下,该元件可以存在于固态。它有一个以体为中心的立方晶体结构。由于没有未配对的电子,所以它是非磁性的。镭是周期表第2组中唯一的放射性元素。在纯态下,这种化学元素具有挥发性。它有很高的熔点和沸点。
氡(radon)和镭(radium)的区别
氡和镭的主要区别在于氡是一种惰性气体,而镭是一种放射性元素。然而,这两种元素都具有放射性,因为它们的原子序数很大。此外,氡是镭的中间衰变产物。另外,氡的半衰期约为3.8天,镭的半衰期约为1600年。
下表总结了氡和镭之间的区别。

总结 - 氡(radon) vs. 镭(radium)
虽然氡和镭的名字听起来很相似,但它们是完全不同的化学元素。氡和镭的主要区别在于氡是一种惰性气体,而镭是一种放射性元素。然而,这两种元素都具有放射性,因为它们的原子序数很大。
引用
1Hanusa,Timothy P.“镭”,《大英百科全书》,不列颠百科全书公司,2019年3月14日,
2“镭”,维基百科,维基媒体基金会,2020年4月24日,
三。“氡”,维基百科,维基媒体基金会,2020年5月20日,