分子几何导论
分子几何或分子结构是分子内原子的三维排列。能够预测和理解分子的分子结构很重要,因为物质的许多性质是由其几何结构决定的。这些性质的例子包括极性、磁性、相、颜色和化学反应性。分子几何学也可用于预测生物活性、设计药物或破译分子的功能。

价层、键对和vsepr模型
分子的三维结构由其价电子决定,而不是原子核或原子中的其他电子。原子的最外层电子是它的价电子。价电子是最常参与形成键和形成分子的电子。
一个分子中的原子之间共享成对的电子,并将原子固定在一起。这些对称为“键合对”。
预测原子内电子相互排斥方式的一种方法是应用VSEPR(价壳层电子对排斥)模型。VSEPR可用于确定分子的一般几何结构。
预测分子几何
这是一张图表,根据分子的键行为描述了分子的通常几何结构。要使用这个键,首先画出一个分子的路易斯结构。计算存在多少电子对,包括键对和孤对。将双键和三键视为单电子对。A表示中心原子。B表示A周围的原子。E表示孤电子对的数量。按以下顺序预测粘结角:
孤对与孤对排斥>孤对与键对排斥>键对与键对排斥
分子几何实例
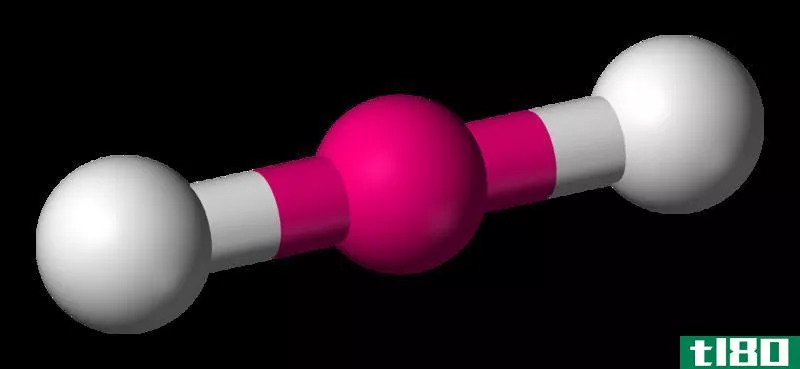
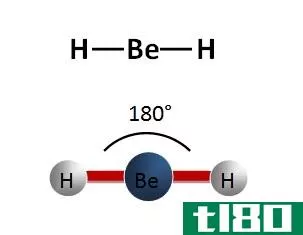
在线性分子几何结构的分子中,中心原子周围有两个电子对,两个成键电子对和0个孤对。理想的结合角为180°。
| 几何学 | 类型 | #电子对数 | 理想键角 | 例子 |
| 线性的 | AB2 | 2. | 180° | 氯化铍 |
| 三角平面 | AB3 | 3. | 120° | BF3 |
| 四面体 | AB4 | 4. | 109.5° | 甲烷 |
| 三角双锥 | AB5 | 5. | 90°, 120° | 五氯化磷 |
| 八面体 | AB6 | 6. | 90° | 六氟化硫 |
| 弯曲 | AB2E | 3. | 120° (119°) | 二氧化硫 |
| 三角锥体 | AB3E | 4. | 109.5° (107.5°) | 氨气 |
| 弯曲 | AB2E2 | 4. | 109.5° (104.5°) | 水 |
| 跷跷板 | AB4E | 5. | 180°,120° (173.1°,101.6°) | SF4 |
| T形 | AB3E2 | 5. | 90°,180° (87.5°,<180°) | 三氟化氯 |
| 线性的 | AB2E3 | 5. | 180° | 二氟化氙 |
| 四方锥 | AB5E | 6. | 90° (84.8°) | 五氟化溴 |
| 正方形平面 | AB4E2 | 6. | 90° | 四氟化氙 |
分子几何中的异构体
具有相同化学式的分子的原子排列可能不同。这些分子被称为异构体。异构体之间可能具有非常不同的性质。有不同类型的异构体:
- 构成异构体或结构异构体具有相同的公式,但原子之间并非通过相同的水连接。
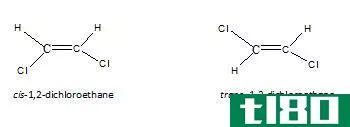
- 立体异构体具有相同的公式,原子以相同的顺序键合,但原子群围绕键旋转的方式不同,从而产生手性或手性。立体异构体的偏振光彼此不同。在生物化学中,它们往往表现出不同的生物活性。
分子几何的实验测定
你可以用刘易斯结构来预测分子的几何结构,但最好用实验来验证这些预测。有几种分析方法可用于对分子成像,并了解其振动和旋转吸光度。例子包括x射线晶体学、中子衍射、红外光谱、拉曼光谱、电子衍射和微波光谱。最佳的结构测定是在低温下进行的,因为提高温度会使分子获得更多的能量,从而导致构象变化。物质的分子几何结构可能不同,这取决于样品是固体、液体、气体还是溶液的一部分。
分子几何关键外卖
- 分子几何描述分子中原子的三维排列。
- 从分子几何结构中获得的数据包括每个原子的相对位置、键长、键角和扭转角。
- 预测分子的几何形状可以预测其反应性、颜色、物相、极性、生物活性和磁性。
- 可以使用VSEPR和Lewis结构预测分子几何结构,并使用光谱和衍射进行验证。
参考资料
- 科顿,F.阿尔伯特;威尔金森,杰弗里;穆里洛,卡洛斯A。;《高级无机化学》(第六版),纽约:威利国际科学出版社,ISBN 0-471-19957-5。
- 约翰·E·麦克默里(1992),有机化学(第三版),贝尔蒙特:沃兹沃思,ISBN 0-534-16218-5。
- Miessler G.L.和Tarr D.A.无机化学(第二版,Prentice Hall 1999),第57-58页。
- 发表于 2021-10-04 21:17
- 阅读 ( 236 )
- 分类:化学
你可能感兴趣的文章
线性的(linear)和非线性分子(nonlinear molecules)的区别
线性分子和非线性分子的关键区别在于,线性分子的化学结构是直线的,而非线性分子的化学结构是锯齿形或交联的。 根据分子的形状,我们知道的分子可以分为线性分子和非线性分子两类。如果一个分子的化学结构具有线...
- 发布于 2020-09-25 02:34
- 阅读 ( 738 )
人类(homo)和卢莫(lumo)的区别
...供电子,而Lumo接收电子。 术语HOMO和LUMO在普通化学的“分子轨道理论”的副标题下。术语HOMO代表“最高占据分子轨道”,而术语LUMO代表“最低未占用分子轨道”。我们称之为“前沿轨道”。分子轨道给出了电子在原子中最可能...
- 发布于 2020-10-17 15:34
- 阅读 ( 294 )
同核(homonuclear)和异核双原子分子(heteronuclear diatomic molecules)的区别
同核(homonuclear)和异核双原子分子(heteronuclear diatomic molecules)的区别 双原子分子是由每个分子两个原子组成的物质。这些分子是由两个原子通过共价化学键相互结合而成的。原子可以通过单键、双键或三键结合。根据双原子分...
- 发布于 2020-10-24 02:37
- 阅读 ( 477 )
形状(shape)和分子几何学(geometry of a molecule)的区别
分子形状和几何结构的关键区别在于分子的形状是分子的结构,不包括中心原子上的孤对,而分子的几何描述了分子中心原子周围的孤对电子和键对电子的排列。 我们通常交替使用分子的形状和几何形状这两个术语。然而,...
- 发布于 2020-11-02 15:58
- 阅读 ( 516 )
几何异构体(geometric isomers)和结构异构体(structural isomers)的区别
几何异构体与结构异构体 异构体是具有相同分子式的不同化合物。有各种类型的异构体。异构体主要分为两大类:组成异构体和立体异构体。组分异构体是分子中原子连接性不同的异构体。在立体异构体中,原子以相同的顺...
- 发布于 2020-11-02 17:20
- 阅读 ( 434 )
电子几何(electron geometry)和分子几何学(molecular geometry)的区别
...原子都由三个基本粒子组成——质子、电子和中子。一个分子由一组两个或多个原子组成,这些原子以一定的几何图形结合在一起。当两个或两个以上的原子牢固地结合在一起形成一个分子时,每个原子和它的近邻之间都有化学...
- 发布于 2021-06-25 21:13
- 阅读 ( 367 )
电子几何(electron geometry)和分子几何学(molecular geometry)的区别
... 电子几何的主要区别(main difference electron geometry) vs. 分子几何学(molecular geometry) 分子的几何形状决定了该分子的反应性、极性和生物活性。分子的几何结构可以用电子几何结构或分子几何结构来表示。VSEPR理论(价壳层电子...
- 发布于 2021-06-29 09:25
- 阅读 ( 347 )
vsepr公司(vsepr)和价键理论(valence bond theory)的区别
...中用来解释共价化合物性质的两种理论。VSEPR理论解释了分子中原子的空间排列。这个理论利用孤电子对和键电子对之间的排斥作用来预测某个分子的形状。价键理论解释了原子间的化学键。这个理论解释了轨道的重叠以形成sigm...
- 发布于 2021-06-29 09:45
- 阅读 ( 689 )
粘结(bonding)和反键分子轨道(antibonding molecular orbitals)的区别
主要差异粘合(main difference bonding) vs. 反键分子轨道(antibonding molecular orbitals) 分子轨道理论解释了分子中原子间的化学键。它指出两个原子轨道相互重叠以形成键。这种重叠导致两个轨道的混合,形成一个分子轨道。分子...
- 发布于 2021-06-29 10:40
- 阅读 ( 588 )
键的极性(bond polarity)和分子极性(molecular polarity)的区别
主差键极性(main difference bond polarity) vs. 分子极性(molecular polarity) 在化学中,极性是指导致分子产生偶极矩的电荷分离。在这里,部分正电荷和部分负电荷在键或分子中分开。这主要是因为原子电负性值的不同。原子的电负性是...
- 发布于 2021-06-29 20:34
- 阅读 ( 473 )