关键区别–kd vs km
Kd和Km是平衡常数。Kd和Km的主要区别在于Kd是一个热力学常数,而Km不是热力学常数。
Kd为离解常数,Km为米氏常数。这两个常数在酶反应的定量分析中都非常重要。
目录
1. 概述和主要区别
2. 什么是Kd
3. 什么是公里
4. 并列比较——Kd与Km表格形式
5. 摘要
什么是kd公司(kd)?
Kd是离解常数。由于在平衡体系中的应用,它也被称为平衡离解常数。离解常数是大化合物可逆地转化为小组分的反应的平衡常数。这种转化过程也被称为离解。离子分子总是离解成离子。那么离解常数或Kd是一个表示溶液中某一特定物质分解成离子的程度的量。因此,这等于各离子浓度除以未解离分子浓度的乘积。
AB型↔ A+B组
在上述一般反应中,离解常数Kd可给出如下。
Kd=[A][B]/[AB]。
此外,如果存在化学计量关系,则应在方程式中包括化学计量系数。
哈勃↔ aA+bB型
上述反应的离解常数Kd方程如下:
Kd=[A]A[B]B/[AB]x
具体地说,在生化应用中,Kd有助于确定酶存在下的化学反应产物的数量。酶反应的Kd表达配体受体亲和力。换句话说,它说明了底物离开酶受体的能力。另一方面,它描述了底物与酶结合的强度。
什么是公里(km)?
Km是米氏常数。与Kd不同,Km是一个动力学常数。它主要应用于酶动力学,即确定底物与酶结合的亲和力。酶的存在速度与底物的浓度有关。因此,Michaelis常数或Km是当反应速度达到其最大速度的一半时底物的浓度。
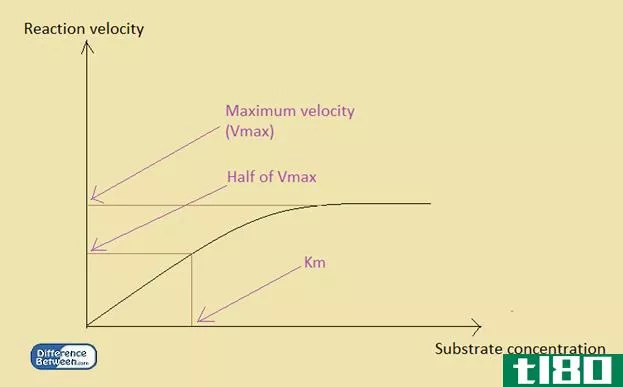
图1:酶反应中反应速度与底物浓度的关系。
在酶(E)与底物(S)反应期间,产物(P)的形成如下:
E+S公司↔ E-S复合体↔ E+P公司
If the equilibrium c***tants of above reaction are as follows, you can derive Km from these c***tants.
公里=K-1+K+2/K+1
基于迈克尔概念的km确定
Michaelis利用底物浓度[S]和最大反应速度Vmax建立了一个关系式。底物浓度与酶反应Km之间的关系如下:
v=v最大[S]/Km+[S]
v是任何时间的速度,而[S]是特定时间的底物浓度,Vmax是反应的最大速度。Km是反应中酶的米氏常数。米氏常数的值取决于酶。因此,Km值很小表明酶被少量底物饱和。然后在低底物浓度下得到Vmax。相比之下,高Km值表明酶需要大量底物才能饱和。
kd公司(kd)和公里(km)的区别
| Kd vs公里 | |
| Kd是离解常数。 | Km是米氏常数。 |
| 自然 | |
| Kd是一个热力学常数。 | Km是一个动力学常数。 |
| 细节 | |
| Kd代表酶对底物的亲和力。 | Km代表底物浓度与反应速度的关系。 |
总结 - kd公司(kd) vs. 公里(km)
Kd和Km是描述酶反应性质的平衡常数。Kd和Km的主要区别在于Kd是一个热力学常数,而Km不是热力学常数。














