超共轭(hyperconjugation)和共振(resonance)的区别
超共轭和共振可以用两种不同的方式稳定多原子分子或离子。这两个过程的要求是不同的。如果一个分子可以有一个以上的共振结构,这个分子就具有共振稳定性。但是,超共轭发生在σ-键与相邻的空的或部分填充的p-轨道或π-轨道之间。这就是超共轭和共振的关键区别
什么是超共轭(hyperconjugation)?
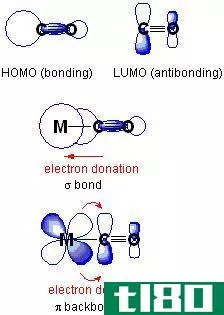
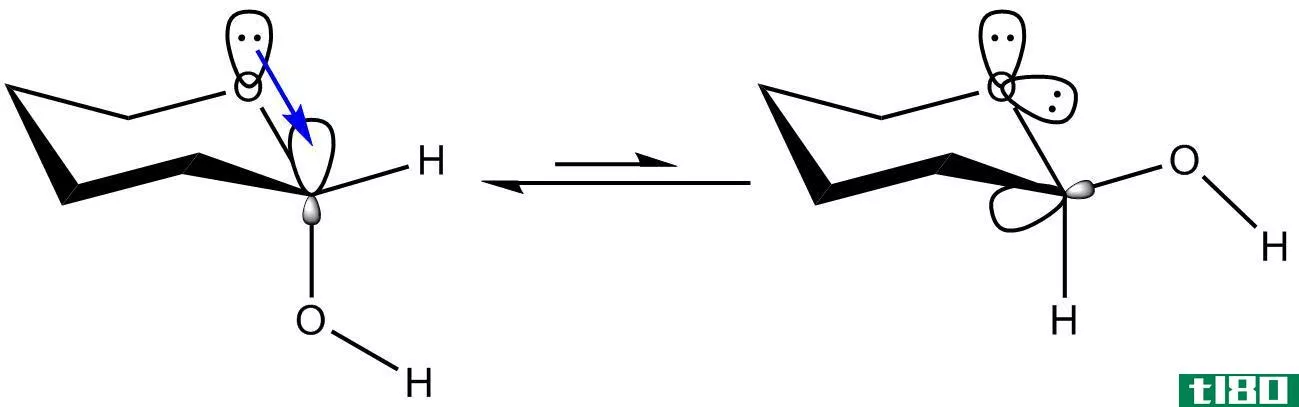
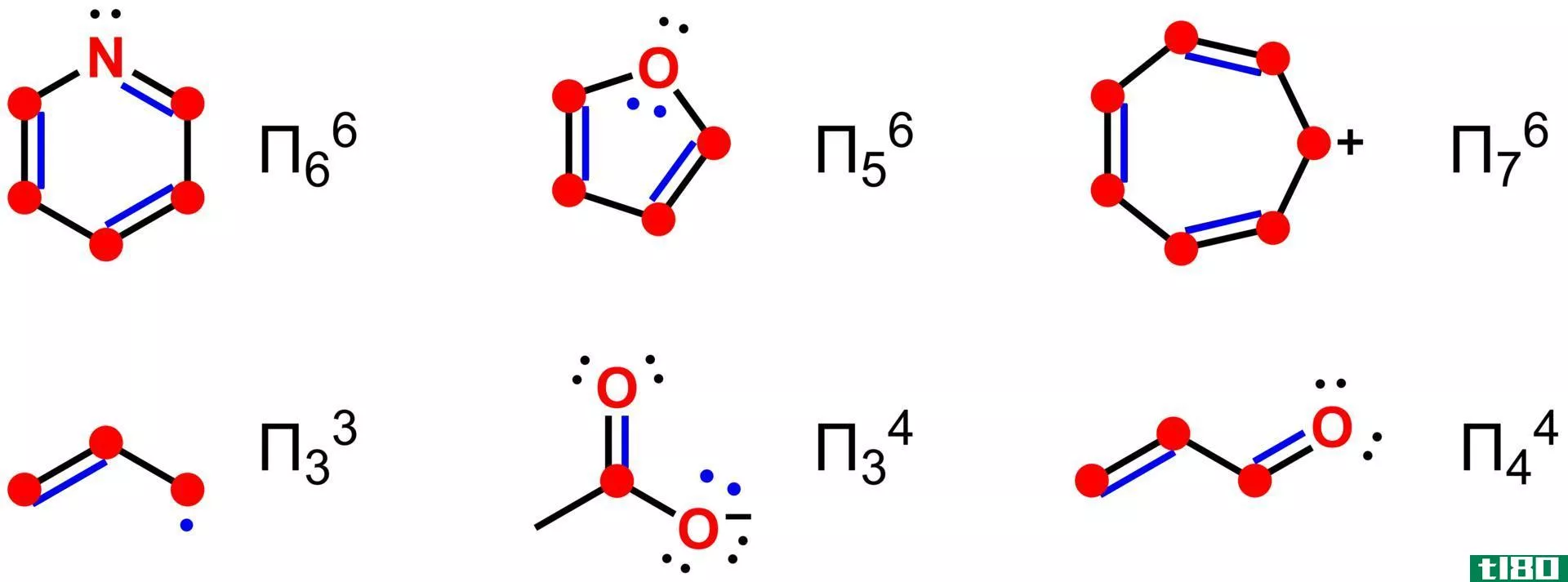
σ-键(通常是C-H或C-C键)中的电子与相邻的空的或部分填充的p-轨道或π-轨道的相互作用会增加系统的稳定性,从而导致扩展的分子轨道。这种稳定作用被称为“超共轭”。根据价键理论,这种相互作用被描述为“双键无键共振”。
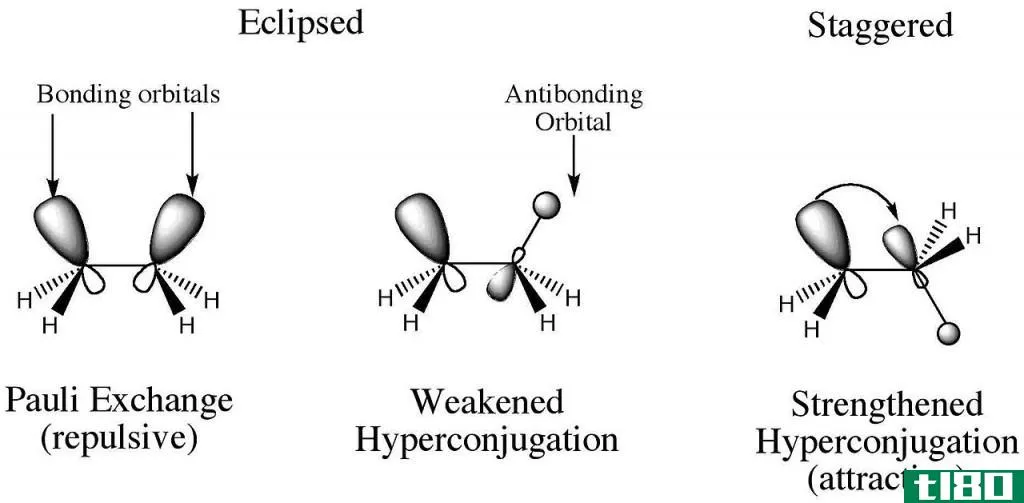
施莱纳超共轭
什么是共振(resonance)?
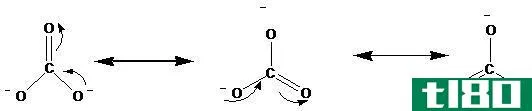
共振是描述分子或多原子离子中离域电子的一种方法,当它可以有一个以上的Lewis结构来表示键合模式时。几种贡献结构可以用来表示分子或离子中的离域电子,这些结构称为共振结构。通过在键中两个原子之间分布电子对,可以用具有可数共价键的Lewis结构来说明所有的贡献结构。因为几种Lewis结构可以用来表示分子结构。实际的分子结构是所有可能的路易斯结构的中间产物。它被称为共振混合体。所有的贡献结构都有相同的原子核位置,但电子的分布可能不同。

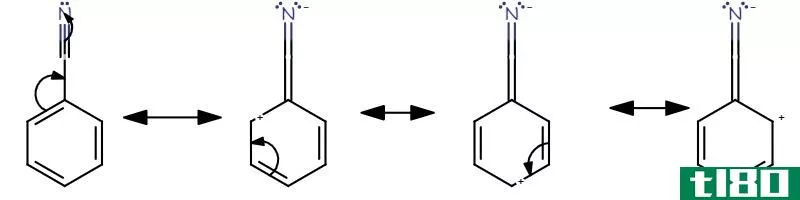
苯酚共振
超共轭(hyperconjugation)和共振(resonance)的区别
超共轭与共振特性
超共轭
- 超共轭影响键长,导致σ键(σ键)缩短。
| 分子 | 碳碳键长度 | 原因 |
| 1,3-丁二烯 | 1.46安 | 两个烯基部分之间的正常共轭。 |
| 甲基乙炔 | 1.46安 | 烷基和炔基部分之间的超共轭作用 |
| 甲烷 | 1.54安培 | 它是一种饱和烃,没有超共轭作用 |
- 与键能之和相比,超共轭分子的生成热值更高。但是,每个双键的加氢热小于在乙烯中的加氢热。
- 碳阳离子的稳定性取决于附着在带正电荷的碳原子上的C-H键的数目。当多个C-H键连接时,超共轭稳定性更强。
(CH3)3C+>;(CH3)2CH+>;(CH3)CH2+>;CH3+
- 相对超结合强度取决于氢的同位素类型。与氘(D)和氚(T)相比,氢的强度更大。氚在它们之间表现出超结合的能力最小。破坏C-T键>C-D键>C-H键所需的能量,这使得H更容易发生超共轭。
共振
- 几种Lewis结构可以用来表示结构,但实际结构是这些贡献结构的中间产物,它由共振混合体表示。
- 共振结构不是同分异构体。这些共振结构只在电子的位置不同,而在原子核的位置上没有差别。
- 每一个Lewis结构都有相同数量的价电子和未配对电子,这就导致每个结构中都有相同的电荷。
- 与贡献结构的估计值相比,实际结构具有较低的总势能。因此,具有共振杂化的分子/离子为各自的分子/离子提供额外的稳定性。