氧化状态与氧化数
氧化态
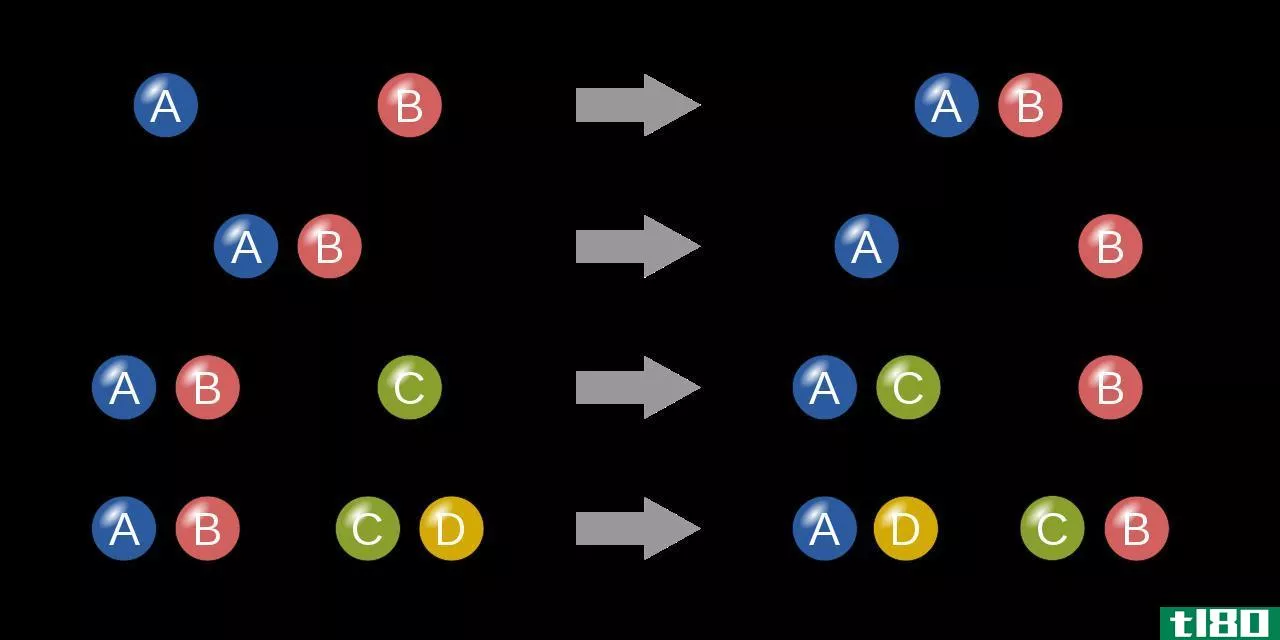
根据IUPAC的定义,氧化状态是“物质中原子氧化程度的量度。氧化态是一个整数值,可以是正、负或零。化学反应使原子的氧化状态发生变化。如果原子被氧化,那么这个状态就是氧化。如果它在减少,那么原子就经历了还原。在氧化还原反应中,电子在转移。在纯元素中,氧化态为零。我们可以用很少的规则来确定分子中原子的氧化状态。
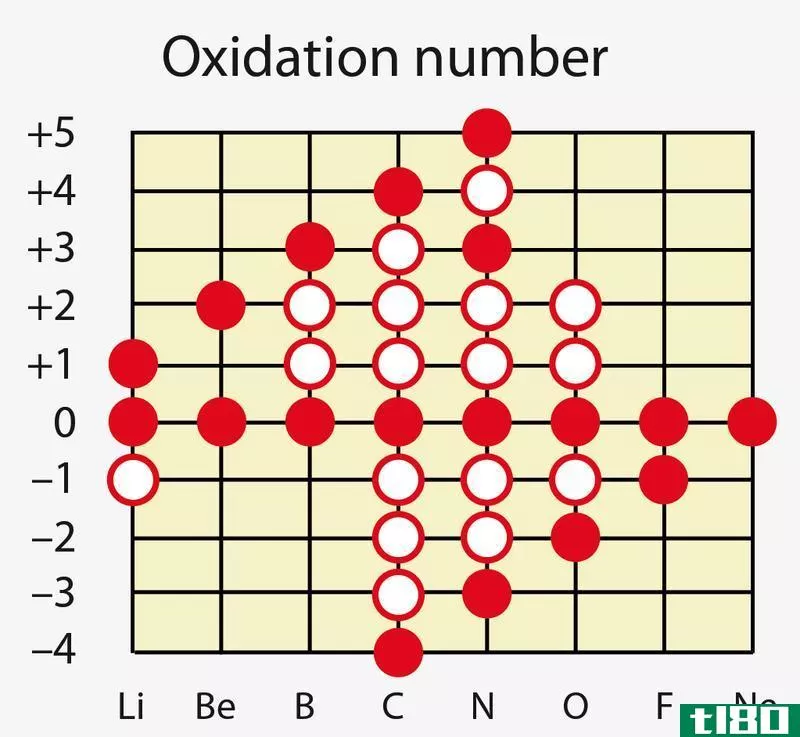
•纯元素为零氧化状态。
•对于单原子离子,氧化状态与其电荷相同。
•在多原子离子中,电荷等于所有原子的氧化态之和。因此,如果已知其他原子的氧化态,就可以找到未知原子的氧化态。
•对于中性分子,所有原子氧化态之和为零。
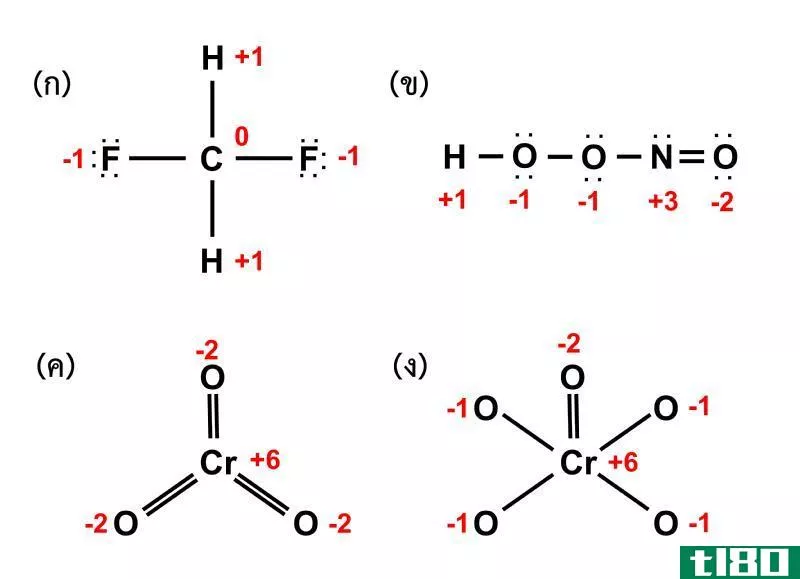
除上述方法外,还可以利用分子的Lewis结构计算氧化态。如果原子是中性的,原子的价电子数与Lewis结构中属于原子的电子数之差,可以算出原子的氧化态。例如,醋酸中的甲基碳具有-3氧化状态。在刘易斯结构中,碳与三个氢原子结合。由于碳的电负性更强,所以键中的六个电子属于碳。碳使另一个碳与另一个碳结合;因此,它们平均地分裂两个键电子。所以,在路易斯结构中,碳有七个电子。当碳处于中性状态时,它有四个价电子。因此,它们之间的差异使得碳的氧化数为-3。
氧化值
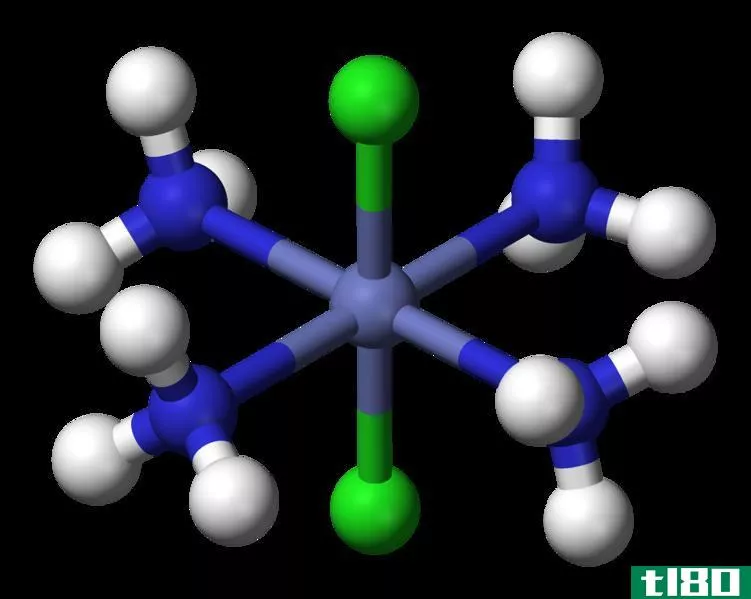
氧化数是配位化合物中心原子的特征。有时电荷和氧化数相似,但有时不同。例如,s块和p块元素的氧化数与其电荷相同。多原子离子的氧化数也与电荷相同。同一种元素可以有不同的氧化数,这取决于它所连接的其他原子。在自由元素中,氧化数总是零。过渡金属离子(d块),元素具有不同的氧化数。
| 氧化状态和氧化数的区别是什么?•氧化数一词主要用于配位化学。它的意义与氧化态稍有不同。•计算氧化数的方法与计算氧化态的方法稍有不同。•在确定氧化态时,考虑了键中原子的电负性。但在测定氧化数时,不考虑电负性。键中的所有电子都属于配体。•通常氧化数用罗马数字表示,而氧化态用印度阿拉伯数字表示。 |