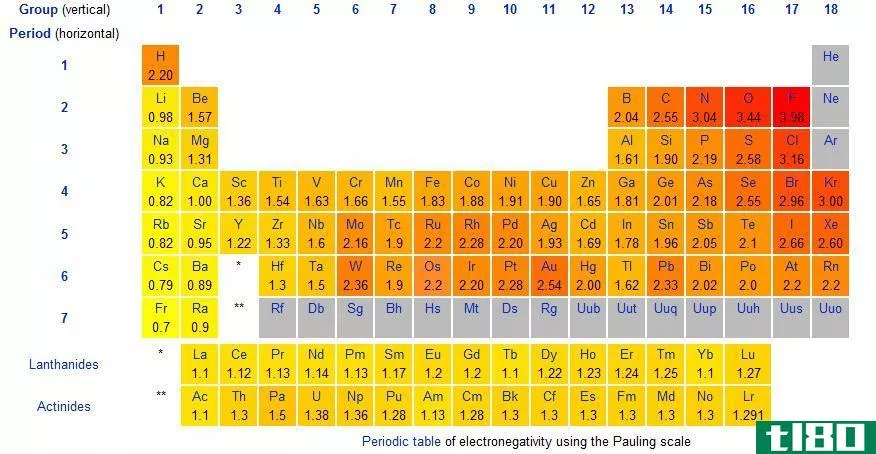
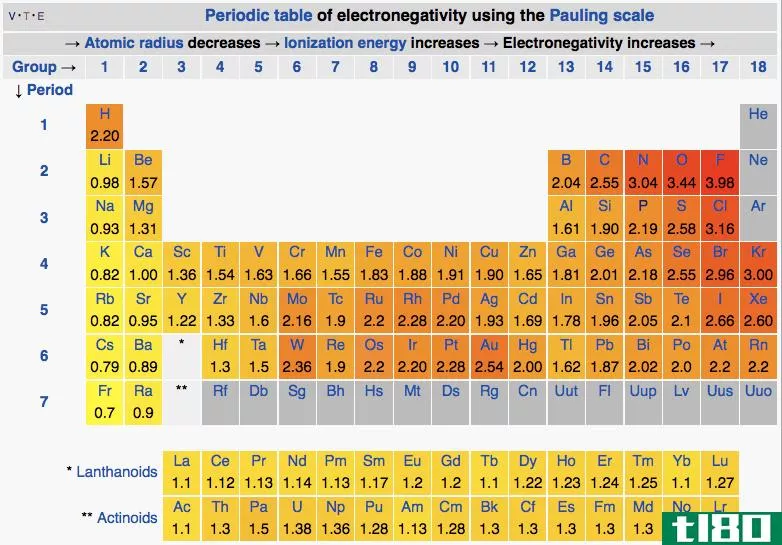
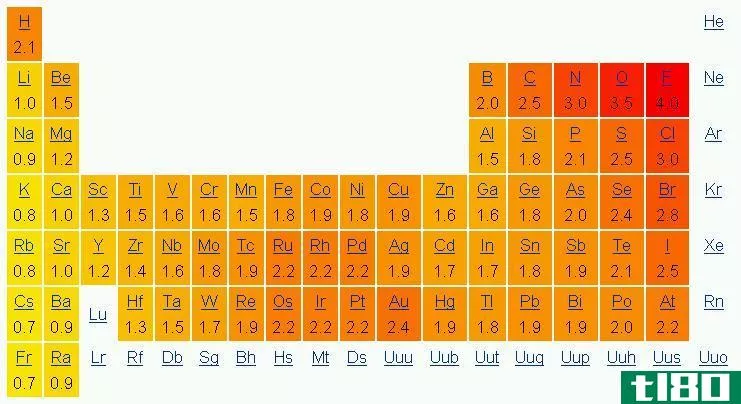
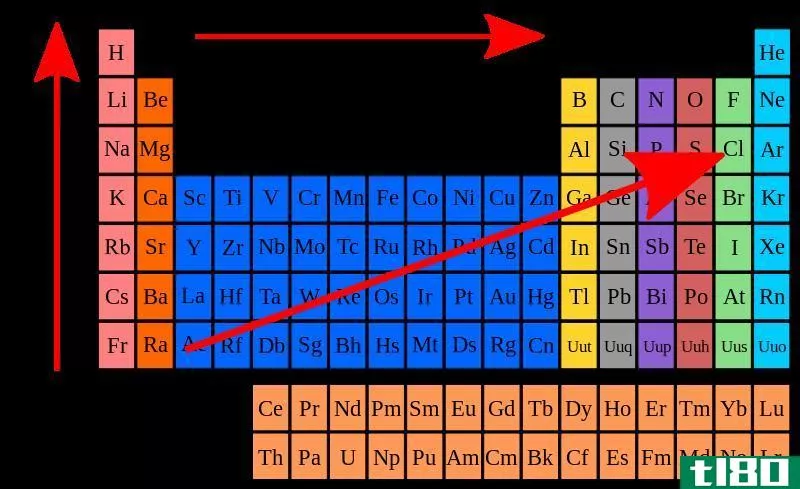
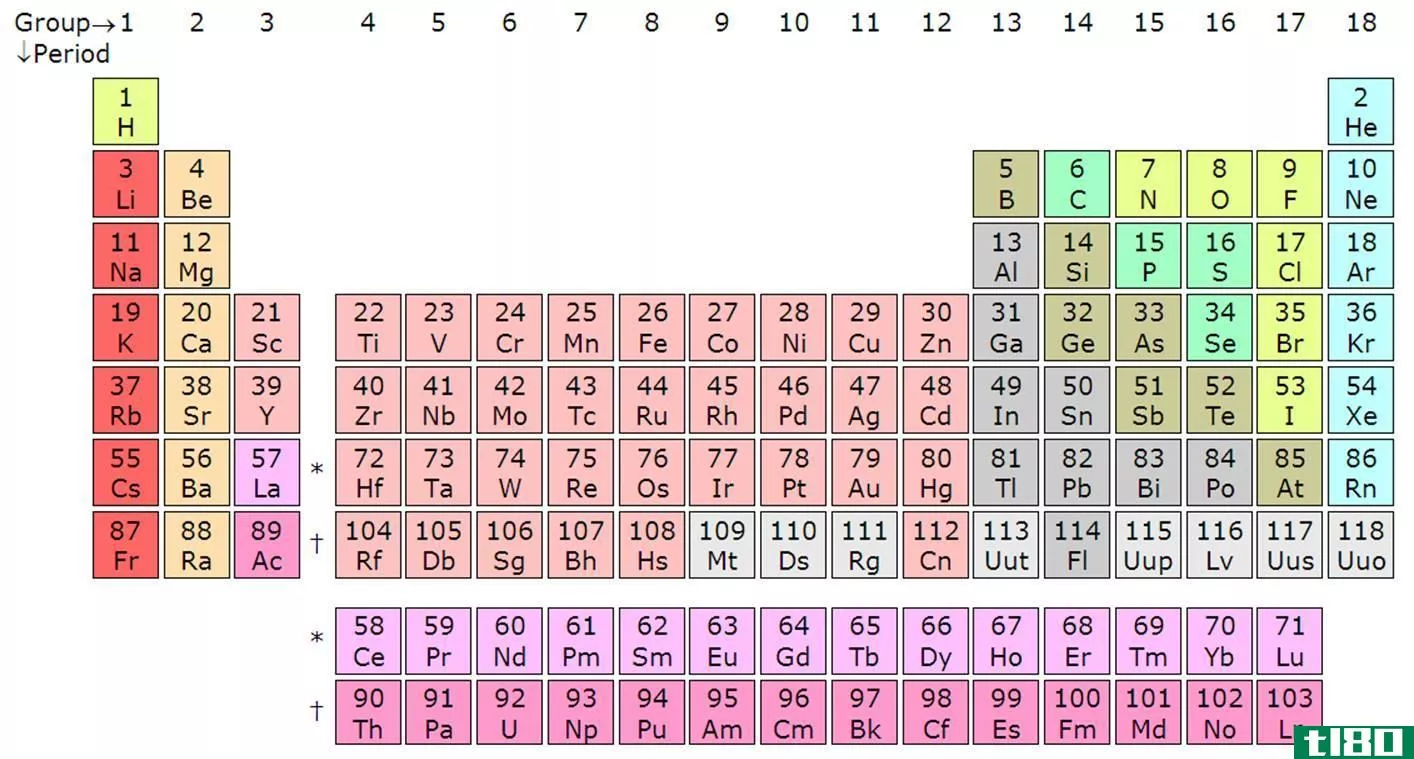
电负性与电子亲和力
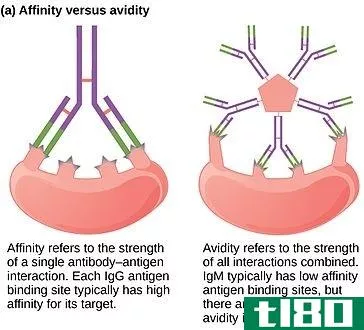
电负性和电子亲和性是学生在理解两个原子的键合形成分子时经常遇到的两个概念。虽然非常相似,但这两个术语有不同之处,需要强调。电负性是一个原子与另一个原子结合的性质,而电子亲和力是一个原子在分子中吸引键对的能力。一般来说,具有高电子亲和力的原子往往更具电负性。
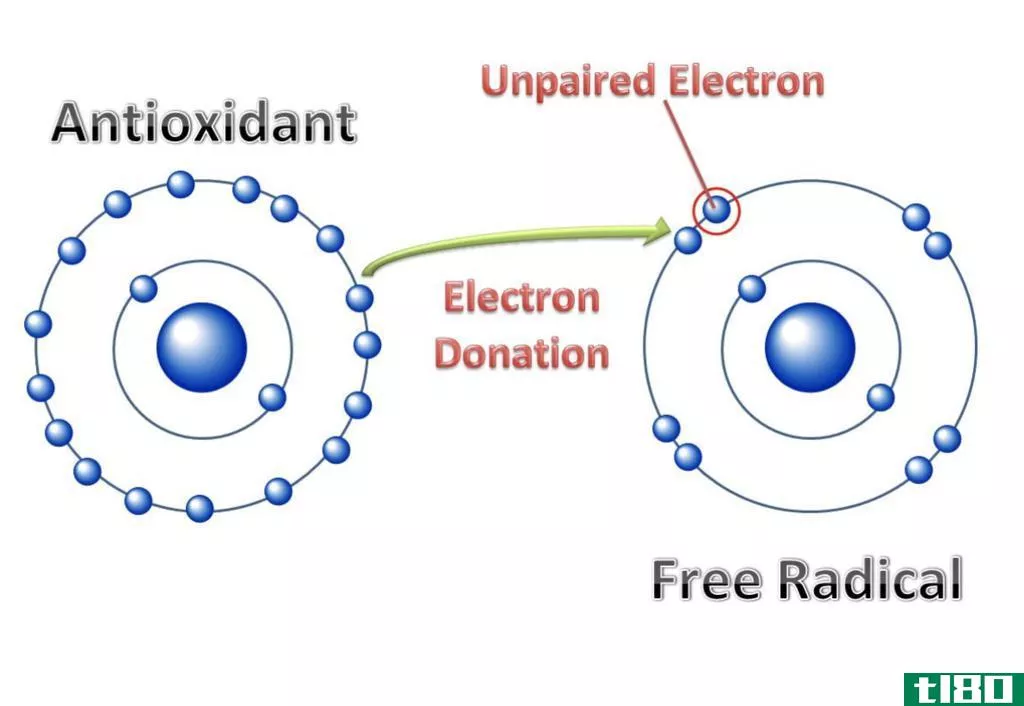
电子亲和力是原子获得电子时释放的能量。能量释放得越多,原子就越容易变成离子。因此,这就是原子吸引额外电子的能力。分子中一个原子的电子亲和力或Eea用以下化学方程式表示。
X-→X+e−
在某些情况下,电子不需要从一个分子上分离出来就可以和另一个分子形成键。在这里,电子被共享并形成共价键。因此,电负性是分子吸引电子并形成共价键的能力的量度。更高的电负性意味着一个分子施加了更大的拉力来吸引电子。
电负性与电子亲和性的区别