阳极(anode)和阴极(cathode)的区别
主要区别-阳极与阴极
阴极和阳极这两个术语用来指极化电气设备的端子。阳极和阴极的主要区别在于,一般来说,阳极是(常规)电流从外部流入设备的终端,而阴极是(常规)电流从设备流出的终端。然而,在某些情况下并没有严格遵循这种用法,因为当一个设备能够经历可逆过程时,被称为“阳极”的同一终端现在可以被称为“阴极”。毫无疑问,这可能会导致混淆,因此建议适应特定领域的一般用法。在本文中,我们将研究使用这些术语的几个场景,并根据这些设备中发生的进程来探讨它们的用法。
什么是阳极(an anode)?
阳极是(常规)电流从外部流入设备的终端。这意味着电子从阳极流出。
什么是阴极(a cathode)?
阴极是(常规)电流从器件中流出的终端。这意味着电子从外部流入这个终端。
原电池
原电池的设置如下所示:
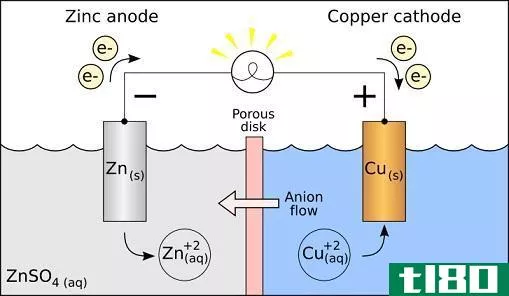
A Galvanic cell
在原电池中,一个电极的还原电位比另一个高。还原电位越高的电极获得电子的能力越强,因此电子从另一个电极流入。在上面画的电池中,铜比锌有更高的还原电位,所以它从锌电极上吸收电子。这伴随着两种反应。在锌电极上,锌分解成Zn2+离子和电子。换句话说,锌被氧化(失去电子)。
锌失去的电子通过导线流到铜电极上。在这里,进入的电子与Cu2+离子结合形成铜原子。铜正在被还原(它获得电子):
在这里,电子从锌端子“流出”器件,所以传统的电流在这里流入器件。这使得锌终端成为阳极。传统的电流从器件的铜端流出,使铜成为阴极。当一个设备使用氧化还原反应时,发生氧化的终端是阳极,发生还原的电极是阴极。这与上面的描述一致:锌(阳极)被氧化,铜(阴极)被还原。
电解槽
在电解槽中,电源用来在含有离子的液体中产生电流。例如,我们将研究当两个电极被放入熔融氯化钠(NaCl,或普通盐)样品中时会发生什么。
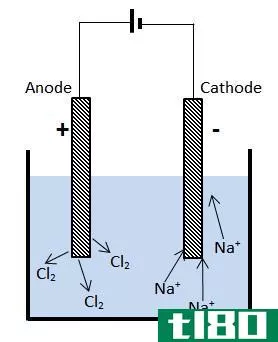
Electrolysis of molten sodium chloride
The electrode connected to the positive terminal of the battery attracts the ani***. Here, these i*** give off their electr***, forming chlorine gas.
在连接到负极的电极上,正钠离子获得电子,形成钠原子:
Here, the terminal that draws current into the device is the electrode connected to the positive terminal of the battery. Therefore, this is the anode. i*** lose their electr*** here, so this is c***istent with the idea that oxidation happens at the anode. Sodium forms at the other electrode where i*** are reduced. Current flows out of the device from this terminal. Therefore, this terminal forms the cathode.
以上两个例子应该说明,术语阳极和阴极不是指特定的电位,而是指电流如何在装置中流动。例如,原电池中的“正”电极是它的“阴极”,而电解时的“正”电极是它的“阳极”。
阳极(anode)和阴极(cathode)的区别
根据电流是从外部流入端子,还是从端子流出到外部,可以给端子命名“阳极”和“阴极”。然而,由于电流在不同情况下的流动方式可能完全不同,将这些术语的用法从一种情况转换到另一种情况可能会令人困惑。因此,可能有必要首先检查情况,以便正确使用术语。如果可能的话,应该使用替代的,不那么模棱两可的术语(视情况而定)。我们讨论了电化学中的两个特殊例子,但术语“阳极”和“阴极”也用于许多其他领域。下面的摘要部分还提到了一些例子。
电流方向:
通常,电流从外部流入阳极。
阴极使电流从装置中流出。这意味着在器件外部,电子从阳极流向阴极。
氧化还原反应:
在依赖氧化还原反应的器件中,氧化发生在阳极上。
而还原发生在阴极。
在原电池和电解电池中:
在原电池和电解电池中,阴极吸引阳离子并将其氧化。
阳极吸引负离子并将其还原。
在电解中:
阳极在电解中形成正极
阴极在原电池中形成负极。
在电子枪和x射线管中:
在电子枪和X射线管中,向器件发射电子的部分形成阴极。
在装置内部,阳极收集电子。
当正常的二极管以正向偏压连接时,正极是p侧,p侧是连接到电池正极的一侧(它从电池吸取电流)。类似地,阴极形成n侧。
尽管在齐纳二极管中,当电流反向偏压时,端子的名称应该是反向的,但是p侧仍然被称为“阳极”,即使从技术上讲,它向外部提供电流。这是一个值得注意的例外,并强调了为什么在可能的情况下应避免使用术语“阳极”和“阴极”(在这种情况下,最好将侧称为p侧和n侧)。
当电池**商将可充电电池的负极端子标记为“阳极”时,另一个混淆的来源就出现了。当电池放电时,术语起作用。然而,从技术上讲,当电池充电时,术语也应该颠倒过来。
参考文献:
丹克,J(2004). 如何定义阳极和阴极。2015年10月1日检索自Welcome to Av8n.com
Image Courtesy:
“Galvanic cell diagram” by Ohio standard (Transferred from en.*********; transferred to Comm*** by User:Burpelson AFB using Comm***Helper) [CC BY-SA 3.0], via Wikimedia Comm***
- 发表于 2021-06-27 07:33
- 阅读 ( 825 )
- 分类:科学
你可能感兴趣的文章
阳极的(anodic)和阴极极化(cathodic polarization)的区别
阳极极化和阴极极化的关键区别在于,阳极极化是指电极电位在正方向上的变化,而阴极极化是指电极电位在负方向的变化。 阳极极化和阴极极化是降低金属表面腐蚀速率的两种电化学技术。阳极极化与阴极极化相反。 目录...
- 发布于 2020-09-16 22:10
- 阅读 ( 639 )
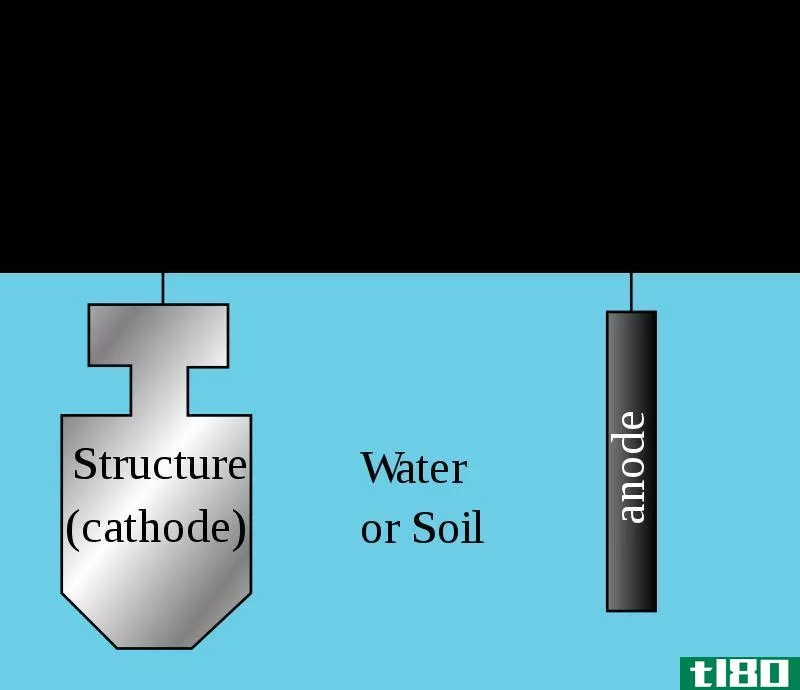
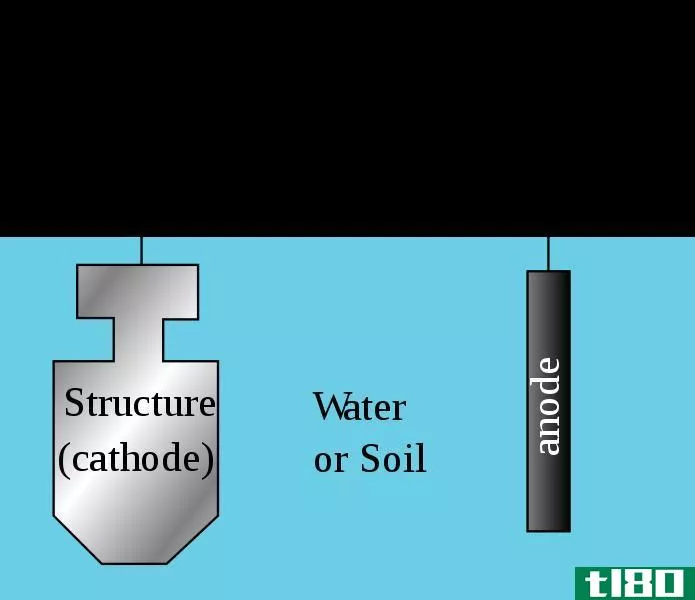
阴极保护(cathodic protection)和牺牲保护(sacrificial protection)的区别
...的阴极来保护金属表面的过程,而牺牲保护则是通过牺牲阳极保护所需的金属表面。 阴极保护和牺牲保护是两种相关的电化学过程。阴极保护包括通过使金属表面成为阴极来保护金属表面。牺牲保护涉及相同的过程,但它描述...
- 发布于 2020-09-17 13:01
- 阅读 ( 510 )
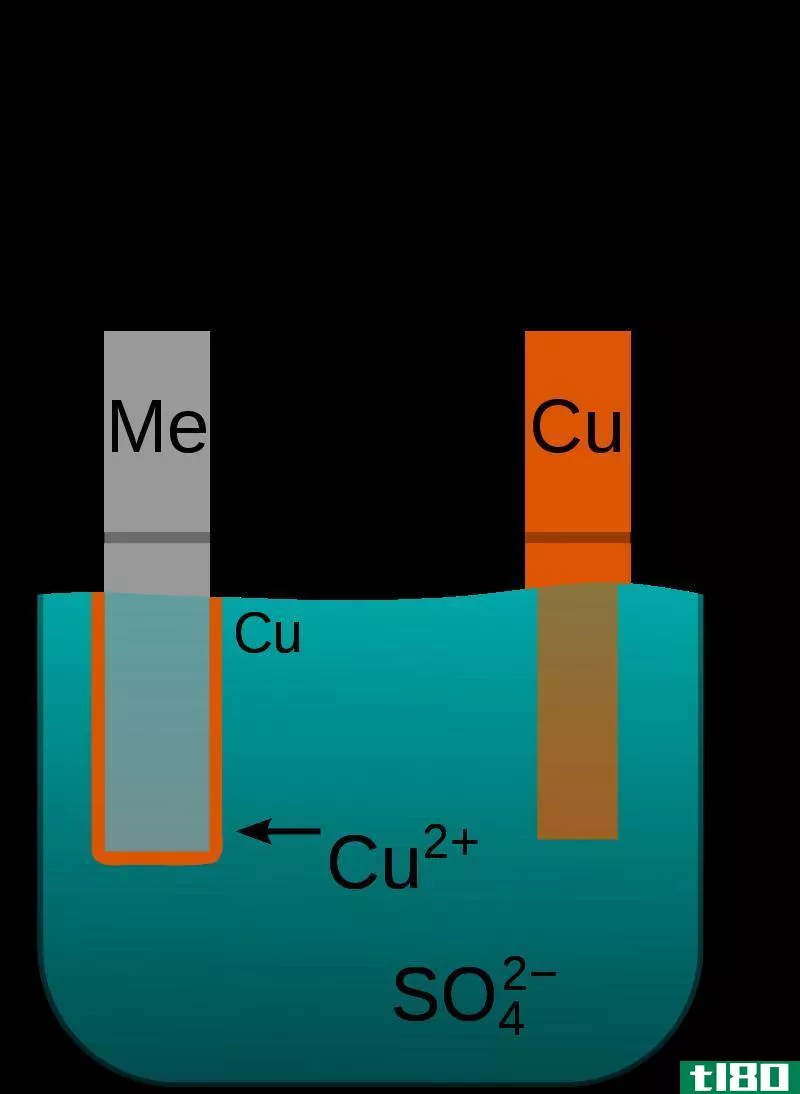
牺牲阳极(sacrificial anode)和外加电流(impressed current)的区别
牺牲阳极和外加电流的主要区别在于,在牺牲阳极中,放置一种金属或合金作为阳极而不是被保护的金属,而在外加电流法中,为被保护金属提供直流电流,使其成为阴极。 牺牲保护和外加电流系统是阴极保护的两种类型。...
- 发布于 2020-10-17 04:00
- 阅读 ( 354 )
阳极的(anodic)和阴极保护(cathodic protection)的区别
阳极保护和阴极保护的主要区别在于,在阳极保护中,被保护表面充当阳极,而在阴极保护中,被保护表面充当阴极。 阳极保护和阴极保护是我们用来防止表面腐蚀或生锈的两种电化学过程。在电化学过程中,我们使用一个...
- 发布于 2020-10-17 05:43
- 阅读 ( 363 )
电镀(electroplating)和阳极氧化(anodizing)的区别
电镀和阳极氧化的关键区别在于,电镀是将一种金属涂覆在另一种金属表面的过程,而阳极氧化是增加金属表面自然氧化层厚度的过程。 在电镀过程中,物体被用作电化学电池的阴极,而在阳极氧化过程中,物体被用作阳极...
- 发布于 2021-03-04 18:13
- 阅读 ( 936 )
阳极(anode)和阴极(cathode)的区别
主要区别-阳极与阴极 阴极和阳极这两个术语用来指极化电气设备的端子。阳极和阴极的主要区别在于,一般来说,阳极是(常规)电流从外部流入设备的终端,而阴极是(常规)电流从设备流出的终端。然而,在某些情...
- 发布于 2021-06-27 07:33
- 阅读 ( 825 )
初级的(primary)和次级细胞(secondary cells)的区别
...学物质都被使用时,发电就终止了。 原电池或原电池由阳极(正电荷端)和阴极(负电荷端)组成。石墨通常用作阴极,锌用作阳极。氧化反应发生在阳极,电子被提供给电路,还原反应发生在阴极,电子从外部被接受。还有...
- 发布于 2021-06-28 18:50
- 阅读 ( 539 )
电化学电池(electrochemical cell)和电解槽(electrolytic cell)的区别
...电路从一个半电池流到另一个半电池。这两个电极被称为阳极和阴极。 氧化和还原反应分别发生在两个电极上。阳极发生氧化反应,阴极发生还原反应。因此,电子在阳极中产生,它们通过外部电路从阳极移动到阴极。盐桥有...
- 发布于 2021-06-29 09:10
- 阅读 ( 618 )
电解(electrolysis)和电镀(electroplating)的区别
...解质。电解液发生的反应应通过电诱导。 在电解槽中,阳极带正电荷,阳极上发生氧化反应;由于阴极上的还原反应,阴极带负电。由于反应是非自发的,它会吸收外界的能量。 调节电解槽的一个重要因素是过电位。为了进行...
- 发布于 2021-06-29 14:20
- 阅读 ( 938 )
阴极(cathode)和阳极(anode)的区别
阴极和阳极是电池中的两种电极,表示电流进入电池和离开电池的位置。阴极(cathode) vs. 阳极(anode)阳极和阴极的区别在于电子会离开阳极,而进入电池的阴极。阴极和阳极的位置并不是固定在一个电池内,并且可以根据在任何给...
- 发布于 2021-07-09 10:46
- 阅读 ( 611 )