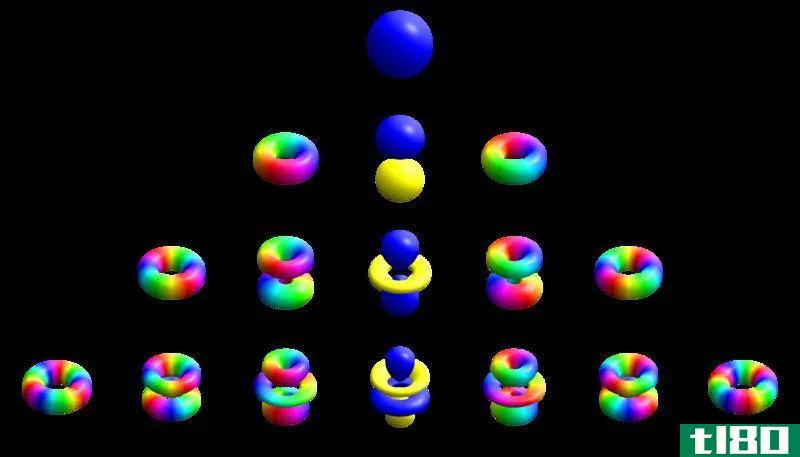子壳定义(电子)
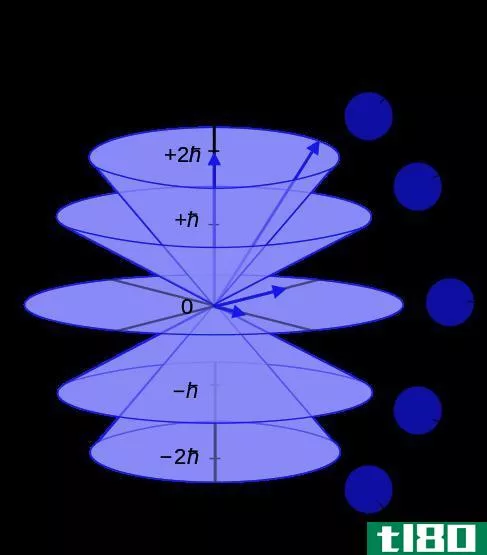
子壳层是由电子轨道分开的电子壳层的一个子部分。子壳层以电子构型标记为s、p、d和f。

子shell示例
下面是一张子壳层的图表,它们的名称以及它们能容纳的电子数:
| 子壳 | ℓ | 最大电子数 | 包含它的贝壳 | 名称 |
| s | 0 | 2. | 每一个贝壳 | 锋利的 |
| P | 1. | 6. | 二等及以上 | 主要的 |
| D | 2. | 10 | 三等及以上 | 弥漫的 |
| F | 3. | 14 | 第四名及以上 | 基本的 |
例如,第一个电子壳层是1s子壳层。第二层电子包含2s和2p子层。
与壳层、次壳层和轨道有关的
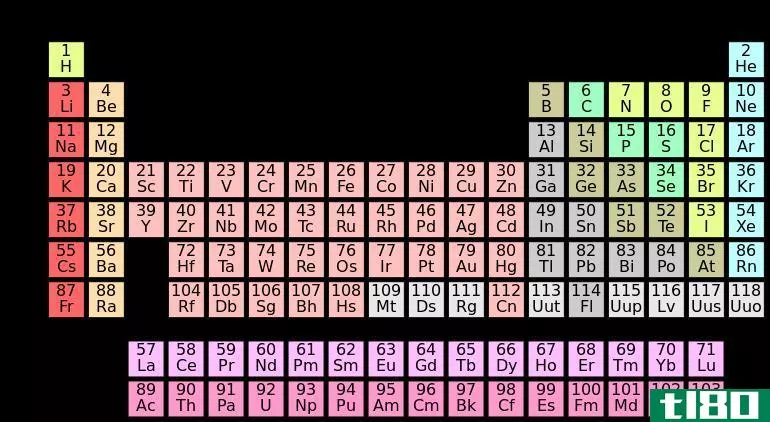
每个原子都有一个电子壳层,标记为K、L、M、N、O、P、Q或1、2、3、4、5、6、7,从离原子核最近的壳层向外移动。外层电子的平均能量高于内层电子的平均能量。
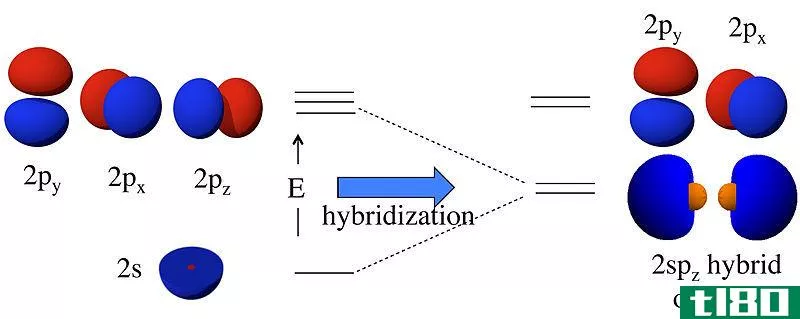
每个外壳由一个或多个子外壳组成。每个子壳由原子轨道组成。
来源
- 生物物理方法的量子力学基础〉,《生物物理的基本概念》。Humana出版社,2009年,纽约。
- 发表于 2021-09-15 16:15
- 阅读 ( 177 )
- 分类:化学
你可能感兴趣的文章
方位角(azimuthal)和主量子数(principal quantum number)的区别
...的次壳层。这些亚壳的形状和方向各不相同。一个能级的子壳层被命名为-I,0和+l。 方位角数 表示 轨道数 最大电子数 0 s 1 2 1 p 3(=-1,0,+1) 6 2 d 5(=-2,-1,0,+1,+2) 10 三 f 7(=-3,-2,-1,0,+1,+2,+3) 14 ...
- 发布于 2020-10-07 18:13
- 阅读 ( 694 )
磁量子数(magnetic quantum number)和自旋量子数(spin quantum number)的区别
...性量子数和自旋量子数的关键区别在于,磁量子数在区分子壳层内可用的轨道时很有用,而自旋量子数则描述了轨道的能量、形状和方向。 量子数是描述原子中电子的唯一量子态的一组值。具体的量子数有四种:主量子数、角...
- 发布于 2020-10-15 03:08
- 阅读 ( 1300 )
混合的(hybrid)和简并轨道(degenerate orbitals)的区别
...能量的原子轨道。例如,sp,sp2和sp3轨道是混合轨道,而p子壳层中有三个p轨道。 总结 - 混合的(hybrid) vs. 简并轨道(degenerate orbitals) 杂化轨道是分子轨道,而简并轨道是原子轨道。杂化轨道和简并轨道的关键区别在于,杂化轨道...
- 发布于 2020-10-16 17:47
- 阅读 ( 908 )
s(s)和p块元素(p block elements)的区别
...置得到最好的解释。在s块元素中,最后一个电子填充到s子壳层,在p块元素中,最后一个电子填充到p子壳层。当它们形成离子时,s阻挡元素很容易将电子从最外层的s亚壳层移除,而p阻挡元素接受电子进入p子壳层或从p子壳层移...
- 发布于 2020-10-27 13:40
- 阅读 ( 351 )
晶场理论(crystal field theory)和配位场理论(ligand field theory)的区别
...相互作用/键 (c) 在自由金属离子中,特定d轨道的所有子壳层的能量相等。 金属离子与其配体之间的相互作用本质上是静电作用。在这个理论中,没有考虑原子和过渡金属之间的键。由于这一局限性,晶体场理论被修改并提出...
- 发布于 2021-06-28 14:30
- 阅读 ( 669 )
氟(fluorine)和氟化物(fluoride)的区别
...元素的原子序数是9。电子构型可以表示为1s22s22p5。由于p子壳层中有5个电子,所以在一个p轨道中有一个未配对的电子。因此,氟可以很容易地通过获得一个电子使其阴离子变得稳定,从而获得惰性气体电子构型(氖)。此外,...
- 发布于 2021-06-29 09:31
- 阅读 ( 510 )
vsepr公司(vsepr)和价键理论(valence bond theory)的区别
...电子配对。 原子的壳层中有电子。这些壳层由s、p、d等子壳层组成,除s子壳层外,其它子壳层由轨道组成。每个子壳中的轨道数如下所示。 子壳 轨道数 轨道名称 s 0 – p 三 像素,像素,像素 d 5 dxz、dxy、dyz、dx2y2、dz2 ...
- 发布于 2021-06-29 09:45
- 阅读 ( 703 )
s(s)和p块元素(p block elements)的区别
...中)而变得稳定。 由于在每个周期后加入了一个新的电子壳层,s块元素的原子半径随周期的增加而减小。随着原子半径的增大,离子化能随原子团的减小而减小。这是因为最外层轨道上的电子被原子核弱吸引 熔点和沸点都随温...
- 发布于 2021-06-29 09:51
- 阅读 ( 557 )
aufbau原理(aufbau principle)和洪德法则(hund’s rule)的区别
...以进一步划分为亚原子粒子。目前公认的原子结构包括电子壳层、子壳层和轨道的细节。电子填充到这些壳层和轨道的方式可以用Aufbau原理和Hund法则来描述。Aufbau原理与Hund法则的主要区别在于Aufbau原理表示电子填充子壳层的顺...
- 发布于 2021-06-29 09:52
- 阅读 ( 845 )
壳次壳(shell subshell)和轨道(orbital)的区别
主要区别壳(main difference shell) vs. 子壳(subshell) 原子是构成物质的基本单位。过去,科学家们认为原子不能进一步分裂。但后来的发现揭示了有关亚原子粒子的信息,这表明原子可以进一步分为亚原子粒子。三种主要的亚...
- 发布于 2021-06-29 12:03
- 阅读 ( 1255 )