弱酸常用ka值表
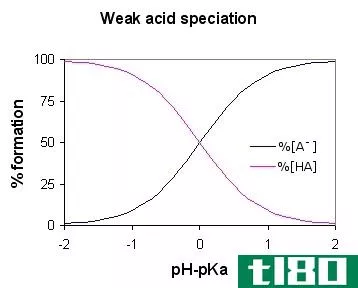
Ka是弱酸离解反应的平衡常数。弱酸是指在水或水溶液中仅部分解离的酸。Ka值用于计算弱酸的pH值。pKa值用于在需要时选择缓冲区。选择pKa接近所需pH值的酸或碱可获得最佳结果。

与ph、ka和pka相关
pH、Ka和pKa都是相互关联的。对于酸性HA:
Ka=[H+][A-]/[HA]pKa=-log KapH=-log([H+])
在当量曲线的中点,pH=pKa。
弱酸钾
| 弱酸钾 | |||
|---|---|---|---|
| 名称 | 公式 | 灵魂 | pKa |
| 醋酸 | HC2H3O2 | 1.8 x 10-5 | 4.7 |
| 抗坏血酸(I) | H2C6H6O6 | 7.9 x 10-5 | 4.1 |
| 抗坏血酸(II) | HC6H6O6- | 1.6 x 10-12 | 11.8 |
| 苯甲酸 | HC7H5O2 | 6.4 x 10-5 | 4.2 |
| 硼酸(I) | H3BO3 | 5.4 x 10-10 | 9.3 |
| 硼酸(二) | H2BO3- | 1.8 x 10-13 | 12.7 |
| 硼酸(III) | HBO32- | 1.6 x 10-14 | 13.8 |
| 碳酸(I) | H2CO3 | 4.5 x 10-7 | 6.3 |
| 碳酸(二) | HCO3- | 4.7 x 10-11 | 10.3 |
| 柠檬酸(一) | H3C6H5O7 | 3.2 x 10-7 | 6.5 |
| 柠檬酸(二) | H2C6H5O7- | 1.7 x 105 | 4.8 |
| 柠檬酸(三) | HC6H5O72- | 4.1 x 10-7 | 6.4 |
| 甲酸 | HCHO2 | 1.8 x 10-4 | 3.7 |
| 肼 | HN3 | 1.9 x 10-5 | 4.7 |
| 氢氰酸 | HCN | 6.2 x 10-10 | 9.2 |
| 氢氟酸 | 高频 | 6.3 x 10-4 | 3.2 |
| 双氧水 | 过氧化氢 | 2.4 x 10-12 | 11.6 |
| 硫酸氢离子 | HSO4- | 1.2x10-2 | 1.9 |
| 次氯 | 次氯酸 | 3.5 x 10-8 | 7.5 |
| 乳的 | HC3H5O3 | 8.3 x 10-4 | 3.1 |
| 亚硝基 | HNO2 | 4.0 x 10-4 | 3.4 |
| 草酸(I) | H2C2O4 | 5.8 x 10-2 | 1.2 |
| 草酸(II) | HC2O4- | 6.5 x 10-5 | 4.2 |
| 苯酚 | HOC6H5 | 1.6 x 10-10 | 9.8 |
| 丙酸的 | HC3H5O2 | 1.3 x 10-5 | 4.9 |
| 含硫(I) | 硫酸 | 1.4 x 10-2 | 1.85 |
| 含硫(二) | HSO3- | 6.3 x 10-8 | 7.2 |
| 尿的 | HC5H3N4O3 | 1.3 x 10-4 | 3.9 |
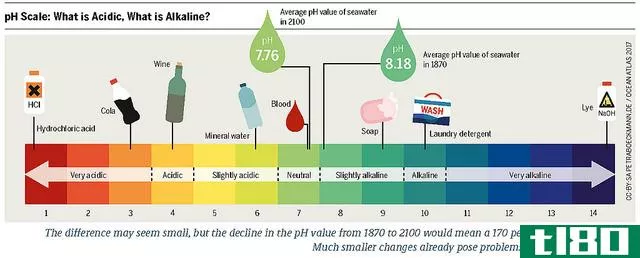
现在看:什么是酸与碱的区别(the differences between acids and bases)?
- 发表于 2021-09-28 09:15
- 阅读 ( 631 )
- 分类:数学
你可能感兴趣的文章
氢氟酸(hydrofluoric acid)和盐酸(hydrochloric acid)的区别
氢氟酸和盐酸的关键区别在于氢氟酸是弱酸,而盐酸是强酸。此外,氢氟酸能够形成氢键,而盐酸不能形成氢键。 此外,氢氟酸和盐酸的另一个重要区别在于它们的分子结构。氢氟酸分子有氟离子,而盐酸分子有氯离子。此...
- 发布于 2020-10-18 08:39
- 阅读 ( 562 )
酸电离常数(acid ionization constant)和碱基电离常数(base ionization constant)的区别
...给出如下公式, 透明质酸+水↔ A–+H3O+ 在这里,HA是一种弱酸,部分分解成离子;阴离子被称为该特定酸的共轭碱。酸分解释放出一个质子(氢离子;H+)。这个质子与水分子结合形成氢离子(H3O+)。这种HA酸的酸离子化常数如...
- 发布于 2020-10-19 03:06
- 阅读 ( 454 )
酸度(acidity)和碱度(basicity)的区别
...越低。pH值越低,酸度越高。 根据物质的酸性,有强酸和弱酸两种类型。在水介质中,强酸会导致较高的酸度,而弱酸则会导致低酸度。强酸可以完全分解成离子,释放出所有可能的氢离子(H+)。相反,弱酸部分分解,只释放...
- 发布于 2020-10-19 11:23
- 阅读 ( 400 )
浓酸(concentrated acid)和强酸(strong acid)的区别
...)释放到其所在的介质中。酸有两种主要类型,即强酸和弱酸。强酸是在水溶液中完全离解,释放H+离子的酸。强碱是在水溶液中完全离解形成OH-离子的化合物。根据水溶液中酸分子的浓度,这些酸可以有浓酸和稀酸两种形式。...
- 发布于 2020-10-19 14:49
- 阅读 ( 402 )
虚弱的(weak)和强酸(strong acid)的区别
弱酸和强酸的关键区别在于弱酸在水中部分电离,而强酸则完全电离。 酸的强度是它在水溶液中与水发生反应时电离或提供氢离子的能力。酸离子化得越多,它就越强,氢离子的生成越少,说明酸是弱酸。这就是强酸和弱酸...
- 发布于 2020-10-23 09:57
- 阅读 ( 378 )
酸的(acid)和酸的(acidic)的区别
...,而且有酸味。此外,还有三大类酸。即强酸、中强酸和弱酸。强酸完全电离,将所有可能的氢离子释放到水溶液中,而弱酸则部分电离。 此外,酸有两大类。也就是说,它们是Brønsted和Lewis酸。Brønsted酸是质子供体。在水溶液...
- 发布于 2020-11-05 21:23
- 阅读 ( 334 )
坚强的(strong)和弱酸(weak acids)的区别
主要区别强(main difference strong) vs. 弱酸(weak acids) 酸是一种能在反应中提供质子或接受电子对的分子或其他物质。酸分为强酸和弱酸两类。强酸和弱酸的主要区别在于强酸在水溶液中完全解离,而弱酸在水溶液中部分解离...
- 发布于 2021-06-28 19:21
- 阅读 ( 1059 )
巴基斯坦航空公司(pka)和酸碱度(ph)的区别
...–log10[Ka]通过观察pKa值,我们可以确定一种酸是强酸还是弱酸。如果pKa值高,酸就弱。这是因为较高的pKa值表明Ka较低。为了使Ka的值较低,[A–][H+]值应低于[HA]值。这意味着酸被部分解离。但如果[A–][H+]的值高于[HA],则Ka值较...
- 发布于 2021-06-28 20:09
- 阅读 ( 343 )
酸碱度(ph)和酸度(acidity)的区别
...子。这些离子引起溶液的酸性。根据电离过程,有强酸和弱酸。强酸能被完全电离并释放出所有可能的质子到溶液中。弱酸部分电离并释放一些质子,从而达到平衡。 酸离解常数给出了溶液酸度的概念。例如,让我们考虑酸“HA...
- 发布于 2021-06-29 08:16
- 阅读 ( 499 )
一元二元酸(monobasic dibasic)和三元酸(tribasic acids)的区别
...应形成盐和水的化学物质。酸有两种主要类型,即强酸和弱酸。酸也可分为三类:一元酸、二元酸和三元酸。酸是按照质子的数量来分组的,以便与碱反应。二元酸和三元酸统称为多元酸。这些一元酸和多元酸可以是强酸,也可...
- 发布于 2021-06-29 12:53
- 阅读 ( 624 )