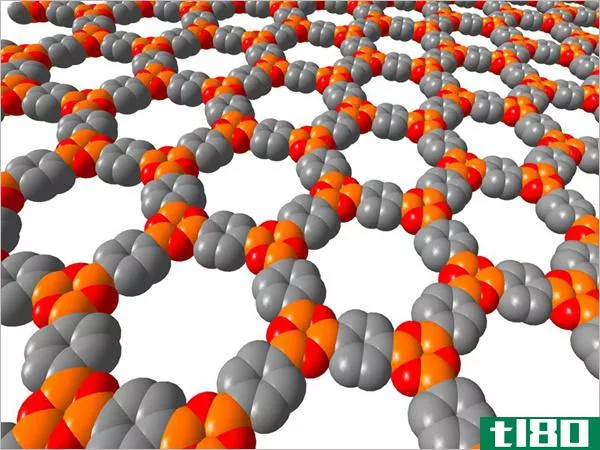
氮化硼和石墨的主要区别在于,氮化硼是由硼和氮原子组成的,而石墨是由碳原子组成的。
氮化硼和石墨是重要的晶体材料。它们有不同的原子组成,这导致了不同的化学和物理性质。
目录
1. 概述和主要区别
2. 什么是氮化硼
3. 什么是石墨
4. 并列比较-氮化硼与石墨表格形式
5. 摘要
什么是氮化硼(boron nitride)?
氮化硼是一种双原子化合物,化学式为BN。它是一种耐热、耐化学腐蚀的耐火材料。氮化硼有几种不同的结构,它们与碳晶格等电子。其中,最常见和稳定的形式是与石墨结构相对应的六边形。而且,这种形式在**润滑油和化妆品时非常有用。
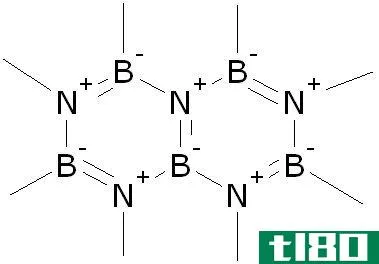
图01:BN的结构
氮化硼最软的多晶型是六角形。立方形状类似于钻石的结构,但比钻石更柔软。然而,这种形式的稳定性优于金刚石。由于所有氮化硼结构具有优异的热稳定性和化学稳定性,该材料主要用作高温设备中的陶瓷。氮化硼通常以无色晶体的形式出现,这种材料不溶于水。加热后可以升华。
什么是石墨(graphite)?
石墨是碳的同素异形体,具有稳定的晶体结构。它是煤的一种形式。此外,它是一种天然矿物(天然矿物是含有一种化学元素的物质,在自然界中不与任何其他元素结合)。此外,石墨是在标准温度和压力下出现的最稳定的碳形式。石墨同素异形体的重复单元是碳(C)。当考虑石墨的晶体结构时,它有一个六角晶系。这种材料的外观可以定义为铁黑色到钢灰色,而且它还具有金属光泽。石墨的条纹颜色是黑色的(细粉矿物的颜色)。

图02:石墨外观
石墨有蜂窝状的晶格。在0.335nm的距离处有石墨烯片。在石墨的晶格结构中,碳原子之间的距离为0.142nm。这些碳原子通过共价键相互结合,一个碳原子周围有三个共价键。一个碳原子的价态是4;因此,这种结构的每个碳原子中都有第四个未被占据的电子。因此,这个电子可以自由迁移,使石墨导电。天然石墨可用于耐火材料、电池、炼钢、膨胀石墨、刹车片、铸造表面和润滑剂。
氮化硼(boron nitride)和石墨(graphite)的区别
氮化硼和石墨的主要区别在于,氮化硼由硼和氮原子组成,而石墨含有碳原子。此外,氮化硼是一种优良的耐热和耐化学腐蚀的耐火材料,而石墨具有优良的导电性。
下表总结了氮化硼和石墨之间的区别。
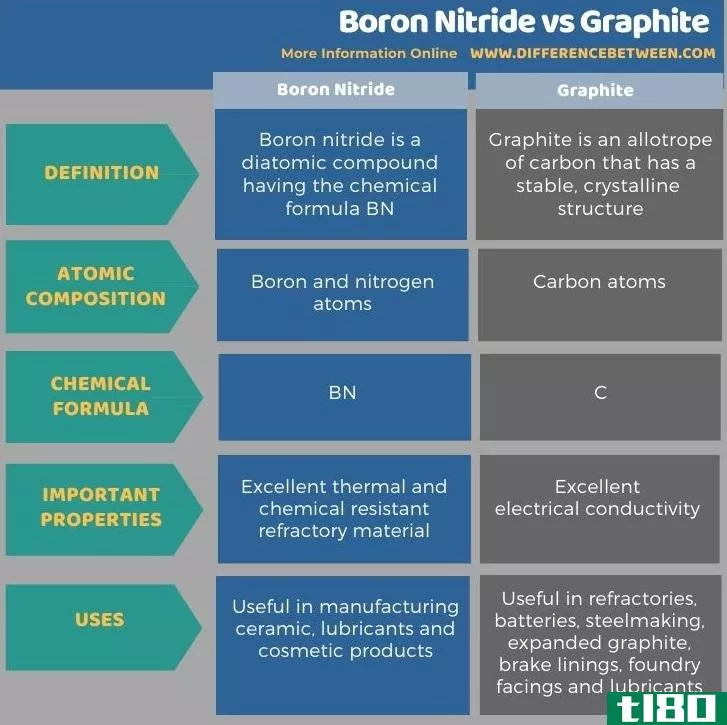
总结 - 氮化硼(boron nitride) vs. 石墨(graphite)
氮化硼和石墨是重要的晶体材料。它们有不同的原子组成,因而具有不同的化学和物理性质。氮化硼和石墨的主要区别在于,氮化硼由硼和氮原子组成,而石墨含有碳原子。
引用
1“氮化硼”,《大英百科全书》,大英百科全书,2013年7月15日,可在此处查阅。“氮化硼”,维基百科,维基媒体基金会,2020年4月15日,可在这里查阅。
2“氮化硼”,维基百科,维基媒体基金会,2020年4月15日,