什么是焓?(enthalpy?)

焓是在化学反应中发生的热能交换。它的符号是H,单位是kJ/mol,即每摩尔千焦耳。在恒定压力下与周围环境交换的能量被称为反应的焓变。为了测量这一变化,使用了标准条件,包括1个大气压和298开尔文的温度(77℉或25℃)。

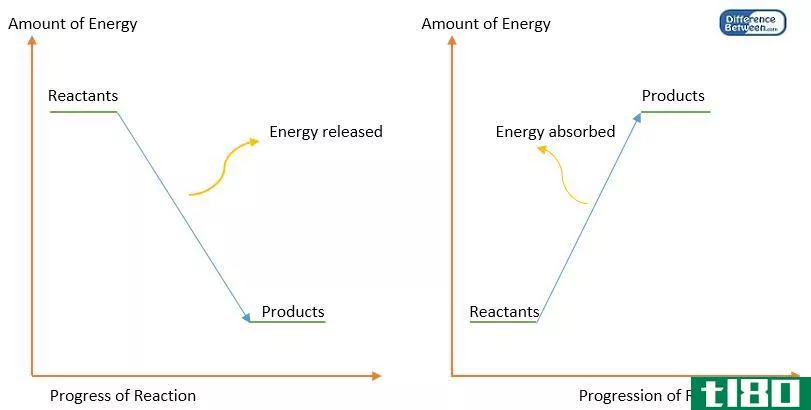
当反应放出热量时,它被称为放热。在这种情况下,焓变是负的,因为反应由于向周围环境损失热能而从高能变为低能。如果能量从周围环境流入一个系统,或者热量被吸收,则被称为内热。在这种情况下,变化是积极的,因为系统正在以热的形式获得能量。
能级图是显示这种热量变化的最常见方式。一般有两种图,一种用于放热反应,另一种用于内热反应。对于一个放热反应,反应物的能量将高于产生的产品的能量。对于内热反应则相反。这种变化在两张图上都有明确的标记。
测量焓值变化的两种方法是简单量热计或简单火焰量热计。简单量热计是由一个装水的容器制成的,热量转移到水中。所记录的水温变化将是由于反应的能量交换造成的。当使用简单量热计时,反应是在量热计本身的水中进行的。
在简单的火焰量热仪中,反应是在装置外进行的。在反应过程中,热量必须转移到量热计内的水中。这种类型的量热仪用于测量燃烧反应的变化。
为了计算焓的变化,必须知道三件事。首先是一个常数,即水的比热容,为4.2J/g/℃。必须测量水的质量和水的温度变化量。计算这种变化的公式是4.2×水的质量×温度变化。
- 发表于 2022-02-09 22:14
- 阅读 ( 96 )
- 分类:科学
你可能感兴趣的文章
键能(bond energy)和键焓(bond enthalpy)的区别
关键区别-键能与键焓 键能和键焓都描述了同一个化学概念:将一摩尔分子分解成其组成原子所需的能量。它测量化学键的强度。所以也叫粘结强度。键能计算为气相化学物质在298K下的键离解能的平均值。键能和键焓这两个...
- 发布于 2020-09-24 09:39
- 阅读 ( 913 )
键焓(bond enthalpy)和晶格焓(lattice enthalpy)的区别
键焓和晶格焓的关键区别在于,键焓是分解化学键所需的能量,而晶格能是从气态的阳离子和阴离子形成一摩尔离子化合物所需的能量。 这两个术语都描述了系统与其周围环境之间的能量交换。键焓与晶格焓相反。键焓解释...
- 发布于 2020-10-15 02:15
- 阅读 ( 472 )
自由能(free energy)和焓(enthalpy)的区别
关键区别-自由能与焓 自由能和焓是两个热力学术语,用来解释热能与热力学系统中发生的化学反应之间的关系。自由能或热力学自由能是一个热力学系统能做的功的量。换言之,自由能是热力学系统中进行热力学功的可用能...
- 发布于 2020-10-19 11:40
- 阅读 ( 643 )
融合(fusion)和汽化(vaporization)的区别
...为“聚变热”和“汽化热”。 目录 1. 概述和主要区别 2. 什么是融合 3. 什么是汽化 4. 并列式与汽化式比较 5. 摘要 什么是融合(fusion)? 熔合是固态转变为液态的熔化过程。因此,这个术语是指相变。它发生在物质的熔点处。这...
- 发布于 2020-10-23 03:09
- 阅读 ( 355 )
焓(enthalpy)和熵(entropy)的区别
焓和熵之间的关键区别在于,焓是在恒定压力下发生的热传递,而熵给出了系统随机性的概念。 为了化学研究的目的,我们把宇宙分成两个系统和一个环境。在任何时候,我们要研究的部分是系统,其余的都是围绕着系统。...
- 发布于 2020-11-04 20:59
- 阅读 ( 1907 )
焓(enthalpy)和热(heat)的区别
焓和热之间的关键区别在于,焓是在恒压下化学反应过程中传递的热量,而热是能量的一种形式。 为了研究化学,我们把宇宙分成两个部分:一个系统和一个周围。系统是我们调查的对象,其余的是周围的。热和焓是描述系...
- 发布于 2020-11-05 19:40
- 阅读 ( 923 )
电子亲和力(electron affinity)和电子增益焓(electron gain enthalpy)的区别
电子亲和力和电子增益焓的关键区别在于,电子亲和力是指孤立原子获得电子的趋势,而电子增益焓是指孤立中性原子获得一个额外电子时释放的能量。 电子亲和力和电子增益焓是两个相关的术语,因为电子增益焓是关于电...
- 发布于 2021-03-04 15:37
- 阅读 ( 679 )
原子化焓(enthalpy of atomisation)和键裂解(bond dissociation)的区别
原子化焓和键离解焓之间的关键区别在于,原子化焓描述了将分子分离成原子所需的能量,而键离解焓描述了分子中化学键的离解。 有时,如果存在简单键,一些简单化合物的原子化焓和键解离焓是相同的。这是因为,在简...
- 发布于 2021-03-04 20:07
- 阅读 ( 982 )
键能(bond energy)和键离解能焓(bond dissociation energy enthalpy)的区别
键能与键离解能(焓) 键能是存在于相同类型原子之间的气相键离解能(通常在298 K的温度下)的平均值。然而,键能和键离解能是不一样的。键离解能是共价键(也称为分子键,是两个非金属原子之间的化学键,涉及这些原子...
- 发布于 2021-06-26 10:13
- 阅读 ( 496 )
熵(entropy)和焓(enthalpy)的区别
主差熵(main difference entropy) vs. 焓(enthalpy) 在化学热力学中,熵和焓都与测量函数有关。而且它们都与反应的热变化有关。熵和焓的主要区别是,熵用来衡量化学过程的无序性或随机性,而焓用来衡量化学反应的热变化或...
- 发布于 2021-06-27 08:16
- 阅读 ( 1299 )