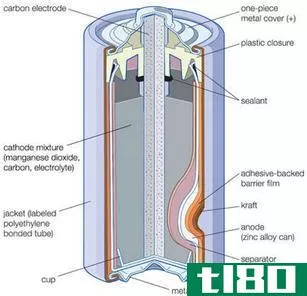
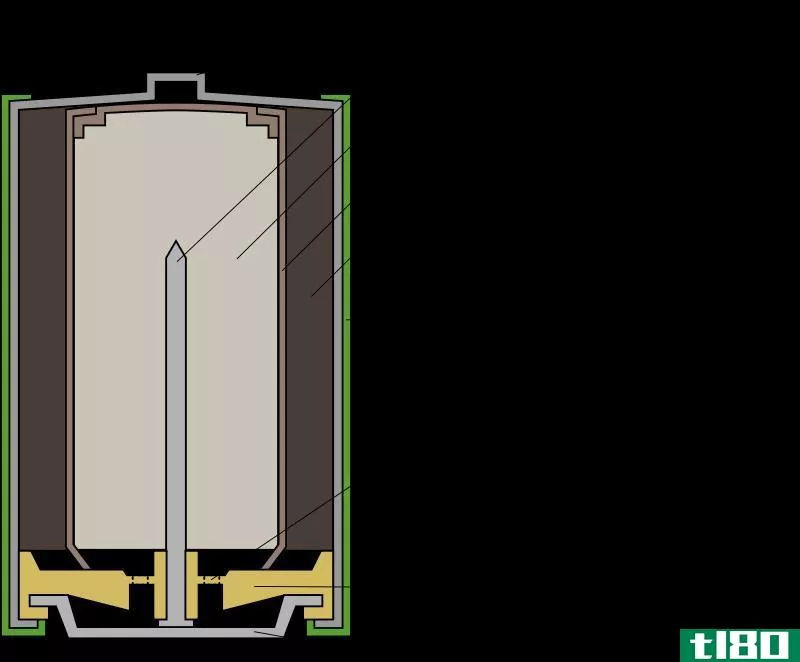
电解槽与电解槽
在电化学氧化中,还原反应起着重要的作用。在氧化还原反应中,电子从一种反应物转移到另一种反应物。接受电子的物质称为还原剂,释放电子的物质称为氧化剂。还原剂负责在氧化过程中还原其他反应物。而对于氧化剂,则相反。这些反应可分为两个半反应,分别显示氧化和还原;因此,它显示了进出电子的数量。
电化学电池
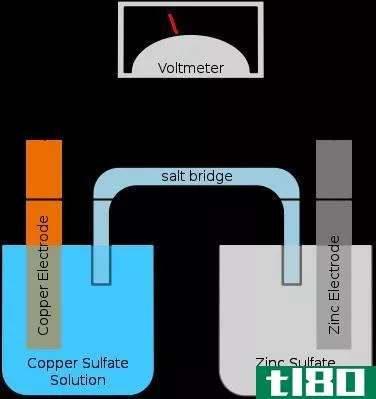
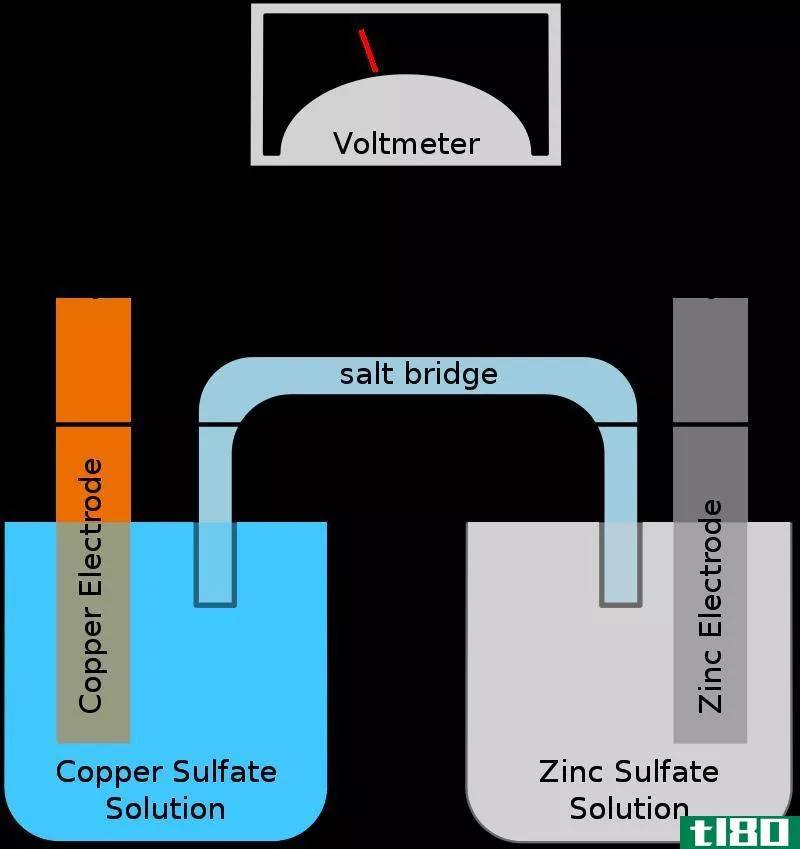
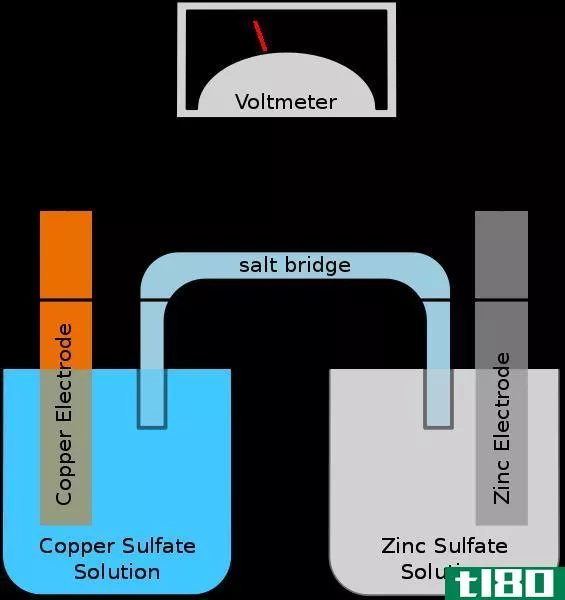
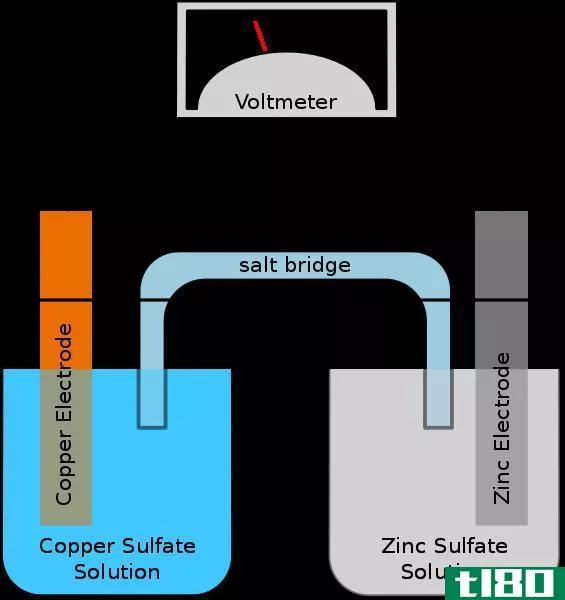
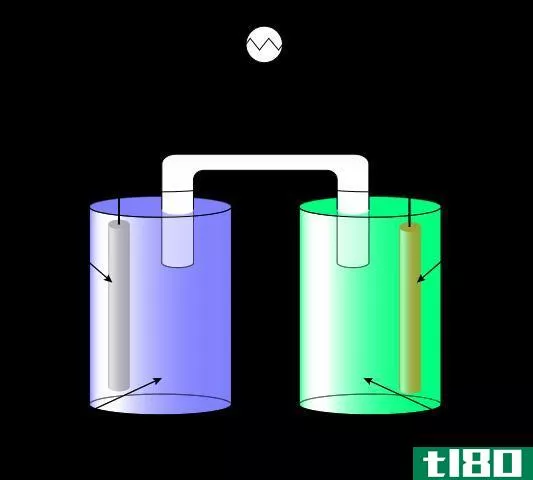
电化学电池是一种还原剂和氧化剂的混合物,它们是物理分离的。通常用盐桥进行分离。虽然它们在物理上是分开的,但两个半细胞都是相互化学接触的。电解电池和原电池是两种类型的电化学电池。在电解槽和原电池中,都会发生氧化还原反应。因此,在电化学电池中,有两个电极叫做阳极和阴极。两个电极外接一个高电阻电压表;因此,电流不会在电极之间传输。这个电压表有助于在发生氧化反应的电极之间保持一定的电压。氧化反应发生在阳极上,还原反应发生在阴极上。电极浸入单独的电解质溶液中。通常,这些溶液是与电极类型有关的离子溶液。例如,铜电极浸入硫酸铜溶液中,银电极浸入氯化银溶液中。这些解决方案是不同的;因此,它们必须分开。最常见的分离方法是盐桥。在电化学电池中,电池的势能被转换成电流,我们可以用它来点亮灯泡,或者做一些其他的电工作。
电解槽
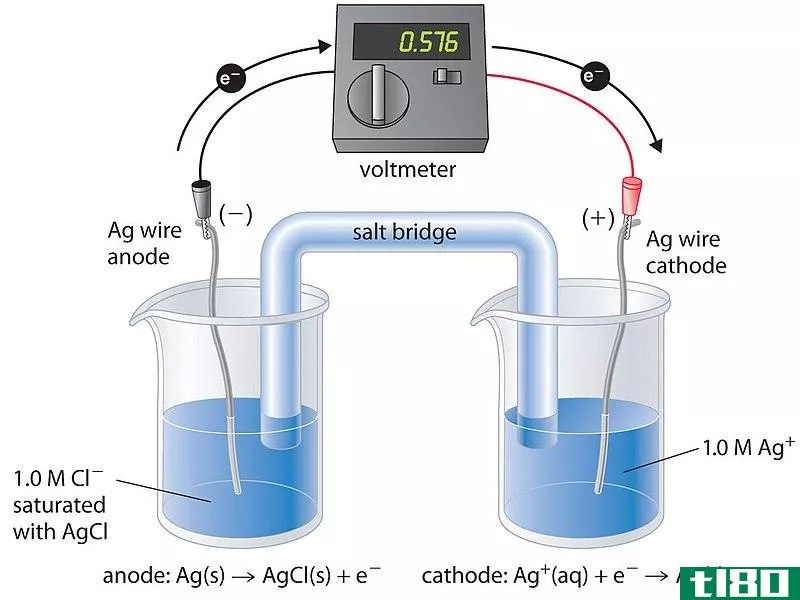
这是一个电池,它利用电流来分解化合物,或者换句话说,进行电解。因此,电解槽的运行需要外部的电能来源。举个例子,如果我们把铜和银作为电池的两个电极,银就连接到外部能源(电池)的正极端子上。铜连接到负极端子。由于负端富含电子,电子从那里流向铜电极。所以铜被还原了。在银电极上,发生氧化反应,释放的电子被送到电池缺电子的正极端子上。以下是电解槽中发生的全部反应,电解槽有铜电极和银电极。
2Ag+Cu2+(aq)⇌2Ag+(aq)+Cu(s)
| 电化学电池和电解电池有什么区别?•电解槽是一种电化学电池。•电解槽需要外部电流才能工作。但是电化学电池,电池的势能被转换成电流。•在电解槽中,阳极是自发的,所以在电解槽中,阳极是负的。在电解槽中,阴极是负的,阳极是正的。 |