分子间力与分子内力
分子间作用力
分子间力是指相邻分子、原子或任何其他粒子之间的作用力。这些力可以是吸引力或排斥力。有吸引力的分子间力把物质结合在一起,因此,这些对**大块材料很重要。所有的分子之间都有分子间的作用力,这些力有的弱,有的强。分子间作用力有多种类型,如下所示。
•氢键
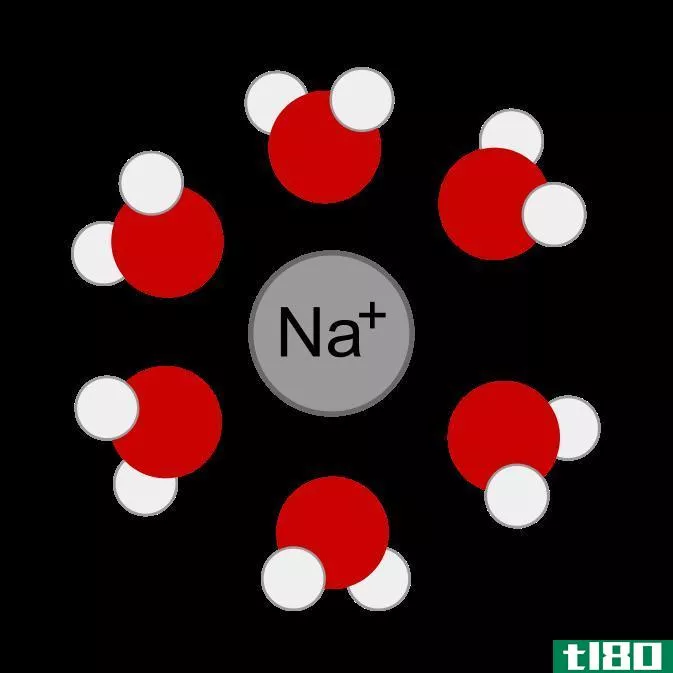
•离子-偶极力
•偶极子-偶极子
•离子诱导偶极子
•偶极感应偶极子
•伦敦/分散部队
当氢附着在像氟、氧或氮等负电原子上时,会产生极性键合。由于电负性,键中的电子比氢原子更容易被负电原子吸引。因此,氢原子会得到部分正电荷,而负电荷越多,则会产生部分负电荷。当两个具有电荷分离的分子接近时,氢和负电荷原子之间会有一个吸引力。这种吸引力被称为氢键。在某些分子中,由于电负性差异,可能会产生电荷分离。因此,这些分子具有偶极子。当离子靠近时,离子和分子的对电荷端之间会形成静电相互作用,即离子偶极力。有时,当一个分子的正端和另一分子的负端接近时,两个分子之间会形成静电相互作用。这就是所谓的偶极偶极相互作用。有些对称分子,如H2,Cl2,在那里没有电荷分离。然而,电子在这些分子中不断地运动。所以,如果电子向分子一端移动,分子内部就可以立即分离电荷。电子的末端会有一个暂时的负电荷,而另一端则会有一个正电荷。这些临时偶极子可以在相邻分子中诱导偶极子,此后,可能发生相对极之间的相互作用。这种相互作用称为瞬时偶极相互作用。这是一种范德瓦尔斯部队,它被单独称为伦敦分散力。
分子内力
这些是分子或化合物原子间的作用力。它们使原子相互结合,保持分子不破裂。分子内作用力有三种类型:共价键、离子键和金属键。
当两个具有相似或极低电负性差的原子发生反应时,它们通过共享电子形成共价键。此外,原子可以获得或失去电子,并分别形成负电荷或正电荷粒子。这些粒子叫做离子。离子间存在静电相互作用。离子键合是这些带相反电荷的离子之间的吸引力。金属在外层释放电子,这些电子分散在金属阳离子之间。因此,它们被称为离域电子的海洋。电子和阳离子之间的静电相互作用称为金属键合。
| 分子间力和分子内力的区别是什么?•分子间作用力在分子之间形成,分子内作用力在分子内形成。•分子内作用力比分子间作用力强得多。•共价键、离子键和金属键合是分子内力的类型。偶极-偶极,偶极诱导偶极,色散力,氢键是分子间作用力的一些例子。 |