原子(atom)和离子(ion)的区别
主差原子(main difference atom) vs. 离子(ion)
原子是物质的组成部分。一切物质都是由原子组成的。早些时候,科学家认为原子不能进一步分裂。但后来的发现发现,原子可以进一步分为亚原子粒子。主要的亚原子粒子是质子、中子和电子。由几个原子组成的基本结构称为分子。离子是特定原子的衍生物。原子和离子的主要区别在于原子没有净电荷,而离子有净电荷。
覆盖的关键领域
1.什么是原子-定义、基本特征和示例2.什么是离子-定义、基本特征和示例3.原子和离子的相似之处是什么-共同特征概述4.原子和离子的区别是什么-主要区别的比较
Key Terms: Anion, Atom, Cation, Electron, Ion, Neutron, Proton
什么是原子(an atom)?
原子是所有物质的基本单位。换句话说,所有物质都是由原子构成的。尽管科学家早先认为原子不能进一步分裂,但这一概念已不再有效。这个概念随着电子、质子和原子核的发现而改变。之后,发展了原子理论,描述了原子的结构。
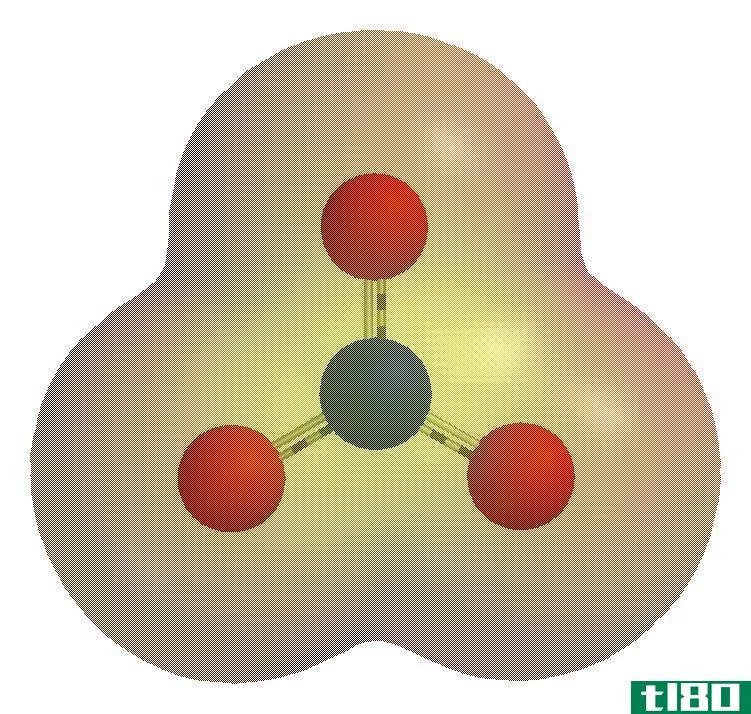
根据现代原子理论,一个原子由两部分组成。它们是原子核和原子轨道。原子核由质子和中子组成,质子是带正电荷的亚原子粒子,中子是带中性电荷的亚原子粒子。质子的电荷是+1。在原子核周围有一个电子云,其中原子的电子沿着假设的轨道运动。电子的电荷为-1。因此,电子是带负电的粒子。
某一元素的原子彼此相同。因此,原子核中质子和中子的数量对于一种元素来说是相等的。对于属于同一元素的原子,原子核周围的电子数是相同的。
质子和中子在原子核中结合在一起是由于这些粒子之间存在强大的作用力。这些力叫做相互作用。这些相互作用是由于被称为介子的微小粒子的交换而发生的。因此,为了将原子核分解成质子和中子,需要非常高的能量。电子绕着原子核运动。因为电子带负电;电子不会被原子核中带正电的质子吸引,也不会落在原子核上,因为电子运动产生的作用力等于原子核的吸引力。由于这两种力相互平衡,电子在运动中与原子核保持一定距离。这些电子移动的路径称为壳层或轨道。

Figure 1: Simplified Atomic Structure
原子的结构可以这样给出,但这是错误的。实际结构比上图复杂得多。
原子能参与化学键。原子结合在一起形成分子或化合物。这些附着物是通过化学键形成的。这些键可以是共价键、离子键、配位键或金属键。在这些键的形成过程中,电子发生交换。但是原子核中的质子和中子不参与化学键合。但在放射性衰变过程中,原子核随着辐射的发射,质子或中子转化为不同的粒子,从而转化为完全不同的原子核。
什么是离子(an ion)?
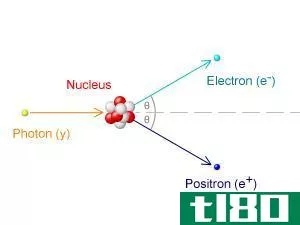
离子是具有净电荷的原子或分子。这个电荷可以是正电荷也可以是负电荷。当原子或分子失去或获得电子时,就形成了离子。例如,如果一个特定的原子失去了一个电子,那么就没有足够的电子来中和原子核的总正电荷。因此,整个原子得到一个净正电荷。但是如果一个原子获得一个电子,那么原子核中就没有足够的质子来中和所有电子的总负电荷。因此,整个原子得到一个净负电荷。由于离子是带电物种,它们可以被电场吸引。负离子被吸引到正极,而带正电荷的离子被吸引到负极。
离子可以形成离子键。离子键是一种化学键,由于两个带相反电荷的离子之间的静电吸引而产生。负离子与一个或多个正离子形成离子键以中和净电荷。

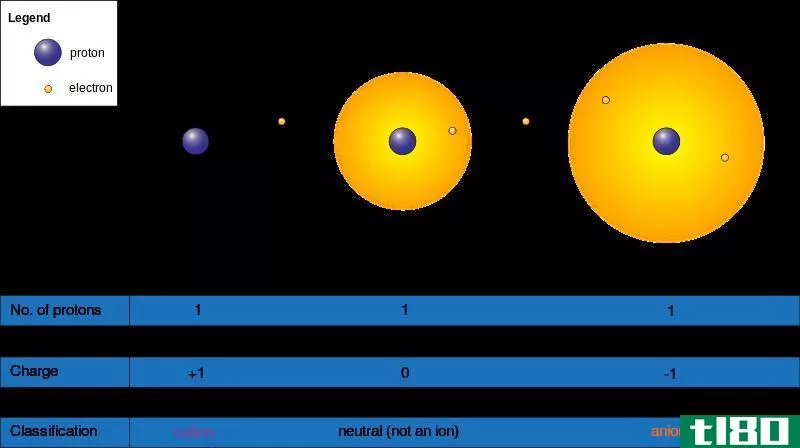
Figure 2: Formation of Cati*** and Ani***
离子有两种类型;阳离子和阴离子。阳离子是具有净正电荷的原子或分子,而阴离子是具有净负电荷的原子或分子。阴离子和阳离子相互吸引,因为它们是带相反电荷的物种。
如果离子是单原子,那么它就是单原子离子。如果离子是分子,那么它就是多原子离子。金属原子通常通过从最外层轨道移除一个或多个电子而形成带正电的离子或阳离子。这是因为金属原子在其最外层轨道上由较少数量的电子组成,并且松散地束缚在原子核上。因此,通过获得大量的电子来填充轨道,形成阳离子比形成阴离子更容易失去这些电子。大多数非金属倾向于共享它们的未配对电子,而不是失去或获得它们。但是,如果它们倾向于变成离子,它们会获得形成阴离子的电子,而不是通过移除大量电子而变成阳离子。
原子和离子的相似性
- 原子可以变成离子。
- 原子和离子都是由可交换的电子组成的。
原子(atom)和离子(ion)的区别
定义
原子:原子是所有物质的基本单位。
离子:离子是具有净电荷的原子或分子。
电荷
原子:原子带中性电荷。
离子:离子要么带正电荷,要么带负电荷。
电场吸引
原子:原子不被电场吸引。
离子:离子根据电荷被电场吸引。
电子数
原子:原子由等量的电子和质子组成。
离子:离子由数目不等的电子和质子组成。
结论
原子是构成所有物质的基本单位。原子可以通过获取或移除电子而成为离子。但并不是所有的离子都是原子,因为有些分子可以通过移除或获得电子而成为离子。原子和离子之间的主要区别在于原子没有净电荷,而离子包含净电荷。
引用
1.赫尔曼斯汀,安妮·玛丽。”什么是原子(解释和例子)。N.p.,N.d.网站。这里有。2017年8月10日。 2.“什么是离子?”BBC。BBC,n.d.网。这里有。2017年8月10日。 2.“什么是离子?”BBC。BBC,n.d.网。
- 发表于 2021-06-29 10:30
- 阅读 ( 537 )
- 分类:科学
你可能感兴趣的文章
多原子离子(polyatomic ions)和化合物(compounds)的区别
多原子离子和化合物之间的关键区别在于,多原子离子具有正电荷或负电荷,而化合物没有净电荷。 多原子离子是一个术语,我们用它来命名含有两个或两个以上带负电荷或正电荷的原子的化学物种。这个离子的电荷是由每...
- 发布于 2020-09-25 07:29
- 阅读 ( 732 )
多价元素(polyvalent element)和多原子离子(polyatomic ion)的区别
多价元素和多原子离子的关键区别在于多价元素有多个价,而多原子离子有多个原子共价键合。 前缀“poly-”表示“许多”。换言之,如果我们用这个前缀来命名某个东西,那就意味着这个东西不止一个。例如,多价意味着...
- 发布于 2020-10-16 01:43
- 阅读 ( 323 )
配位化合物(coordination compound)和复合离子(complex ion)的区别
...ination compound)? 配位化合物是一种化学物质,其中心金属原子被非金属原子或一组称为配体的原子包围,通过化学键与之相连。我们把它们命名为配位化合物是因为金属原子和配体之间存在配位共价键。 图01:一种不带电的配位...
- 发布于 2020-10-16 02:25
- 阅读 ( 702 )
碳离子(carbonium ion)和碳负离子(carbanion)的区别
碳离子和碳负离子的主要区别在于碳离子中的碳原子是五价的,而碳离子中的碳原子是三价的。 碳离子和碳负离子是带有碳原子的有机化合物的离子形式。然而,这两种离子根据电荷、碳原子的价态、化学键等不同而不同。 ...
- 发布于 2020-10-16 18:39
- 阅读 ( 421 )
积极的(positive)和负离子(negative ion)的区别
...质从其化学结构中失去一个电子时形成的。正离子可以是原子或分子的一部分。 这些物种拥有等量的质子和电子来中和电荷。因此,当这个原子或分子失去一个电子时,就会有一个带正电荷的质子。这就给原子或分子带上了一...
- 发布于 2020-10-18 05:23
- 阅读 ( 596 )
离子(ions)和电子(electrons)的区别
...子是带负电的微粒,而离子则是带负电或正电荷的分子或原子。电子的性质可以用“量子力学”来解释,但离子的性质可以用普通化学来解释。电子(符号:β-或℮-)是亚原子粒子,它没有子粒子或子结构。但是,离子可以有...
- 发布于 2020-10-24 02:41
- 阅读 ( 715 )
原子(atom)和离子(ion)的区别
原子和离子的主要区别在于它们的电荷;原子是中性的,而离子则带正电荷或负电荷。 原子是能形成键的最小中性单元,而离子是任何带电分子。离子可以由几个原子或单个原子组成。原子是唯一的,不分为各种类型,而离...
- 发布于 2020-10-26 18:32
- 阅读 ( 1288 )
自由基(free radical)和离子(ion)的区别
...加,离子可以作为带有电荷(正电荷或负电荷)的分子或原子出现。离子由于电子的增加而带负电荷,而由于失去电子而保持正电荷。离子可能以单电荷或多电荷化学物质的形式出现,这取决于获得或丢失的电子数。自由基是至...
- 发布于 2020-10-26 20:15
- 阅读 ( 1662 )
氢原子(hydrogen atom)和氢离子(hydrogen ion)的区别
氢原子和氢离子之间的关键区别在于氢原子是中性的,而氢离子带有电荷。 氢是元素周期表中第一个也是最小的元素,用H来表示。由于氢的电子构型为1s1,它在周期表中被归为第1组和第1周期。氢可以吸收一个电子形成一个...
- 发布于 2020-11-02 21:56
- 阅读 ( 1138 )
离子型(ionic)和共价化合物(covalent compounds)的区别
...分为离子化合物和共价化合物。由于参与**分子/化合物的原子之间的键合类型不同,它们彼此不同。顾名思义,离子化合物是由离子键构成的,共价化合物是由共价键构成的。离子键发生在相互静电吸引的两个物种之间,而共价...
- 发布于 2021-06-27 07:49
- 阅读 ( 480 )