氢原子和氢离子之间的关键区别在于氢原子是中性的,而氢离子带有电荷。
氢是元素周期表中第一个也是最小的元素,用H来表示。由于氢的电子构型为1s1,它在周期表中被归为第1组和第1周期。氢可以吸收一个电子形成一个带负电的离子,也可以很容易地把电子捐赠出来产生一个带正电荷的质子。如果没有,它可以共享电子,形成共价键。
元素周期表中的元素除了惰性气体外是不稳定的。因此,元素试图与其他元素发生反应,以获得稀有气体的电子构型并达到稳定性。同样地,氢也必须获得一个电子才能实现惰性气体氦的电子组态。当达到这种电子构型时,它形成氢离子。
目录
1. 概述和主要区别
2. 什么是氢原子
3. 什么是氢离子
4. 并列比较-氢原子与氢离子的表格形式
5. 摘要
什么是氢原子(a hydrogen atom)?
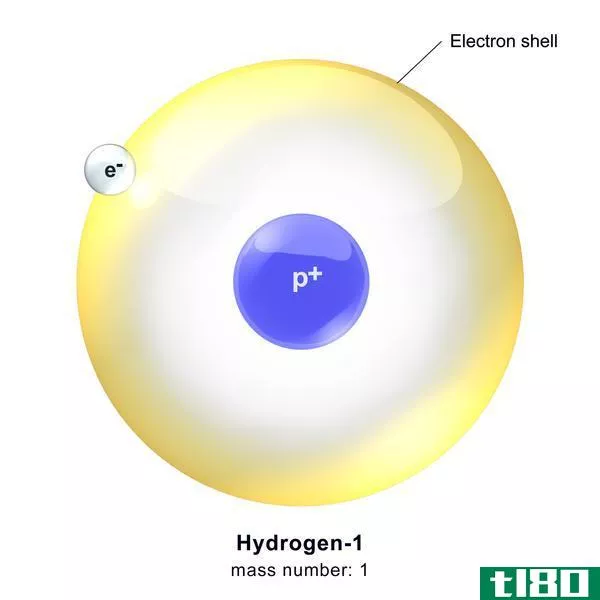
氢原子是周期表中的第一个元素。氢原子有一个电子和一个质子。因此,它的电子构型是1s1。此外,它在s次轨道上只有一个电子,尽管这个轨道可以容纳两个电子。因此,为了获得稳定的电子构型,氢原子是不稳定的和非常活跃的。
图1:氢原子的结构
由于氢原子中质子和电子的数量相似,这个原子不带净电荷。因此,我们说它是中性的。然而,氢有三种同位素:质子-1H(无中子)、氘-2H(一个中子)和氚-3H(两个中子)。这些同位素在原子核中有不同数量的中子。
什么是氢离子(a hydrogen ion)?
氢离子是携带电荷的氢元素的形式。这个离子的电荷可以是正的,也可以是负的,这取决于它的形成方式。它可能是从氢原子中移除一个电子,或是从电子获得过程中形成的。因此,氢离子具有+1或-1电荷(单价)。我们可以把带正电荷的氢离子表示为H+(阳离子),而将负离子表示为H-(阴离子)。
图2:氢原子形成离子
质子的阳离子特别被称为质子,它们是我们在化学反应中主要考虑的氢原子类型,因为与其他同位素相比,质子的自然丰度非常高。此外,它以氢离子(H3O+)的形式存在于水溶液中。
氢离子负责酸度,用氢离子的浓度来计算pH值。当氢原子与其他非金属反应时,就会形成氢离子,当分子溶解时,这些离子会全部或部分释放到水介质中。虽然氢负离子的形成很少见,但它是在氢与诸如1族金属等金属反应时形成的。
氢原子(hydrogen atom)和氢离子(hydrogen ion)的区别
氢是最小的化学元素。它有一个质子和一个电子,所以它是中性的。然而,氢原子的离子是带电的。因此,氢原子和氢离子之间的关键区别在于氢原子是中性的,而氢离子带有电荷。氢原子和氢离子的另一个显著区别是氢原子有一个电子,而氢的阳离子没有电子,氢的阴离子有两个电子。
此外,为了获得稳定的电子构型,氢原子具有高度的反应性。但是,由于氢离子已经达到稳定状态,所以它们的反应性较小/不活泼。阳离子的电荷为+1,阴离子的电荷为-1。所以,我们也可以把这看作是氢原子和氢离子之间的区别。

总结 - 氢原子(hydrogen atom) vs. 氢离子(hydrogen ion)
氢是元素周期表中的第一个元素。因此,它是最小的原子。它可以形成带正电荷或负电荷的离子。氢原子和氢离子的关键区别在于氢原子是中性的,而氢离子是带电荷的。
引用
1约翰·C·莫里森,《现代物理学》,20102。“8.1:氢原子。”物理剧本,剧本,2019年5月2日,可在这里查阅。