氢键和离子键的关键区别在于,永久性阴阳离子之间存在离子键,而部分正电荷和部分负电荷之间存在氢键。
化学键把原子和分子结合在一起。键在决定分子和原子的化学和物理行为方面很重要。正如美国化学家G.N.Lewis提出的那样,当原子的价壳层中含有8个电子时,原子是稳定的。大多数原子的价壳层中的电子少于8个(周期表第18组中的稀有气体除外);因此,它们是不稳定的。这些原子趋向于相互反应以变得稳定。因此,每一个原子都可以实现稀有气体的电子组态。离子键就是这样一种化学键,它连接化合物中的原子。氢键是分子间的相互吸引。
目录
1. 概述和主要区别
2. 什么是氢键
3. 什么是离子键
4. 并列比较-氢键与离子键的表格形式
5. 摘要
什么是氢键(hydrogen bond)?
当氢与氟、氧或氮等负电荷原子相连时,就会形成极性键。由于电负性,键中的电子比氢原子更容易被电负性原子吸引。因此,氢原子将得到部分正电荷,而更负电荷的原子将获得部分负电荷。当两个具有这种电荷分离的分子靠近时,氢和带负电荷的原子之间就会产生引力。我们称之为氢键。
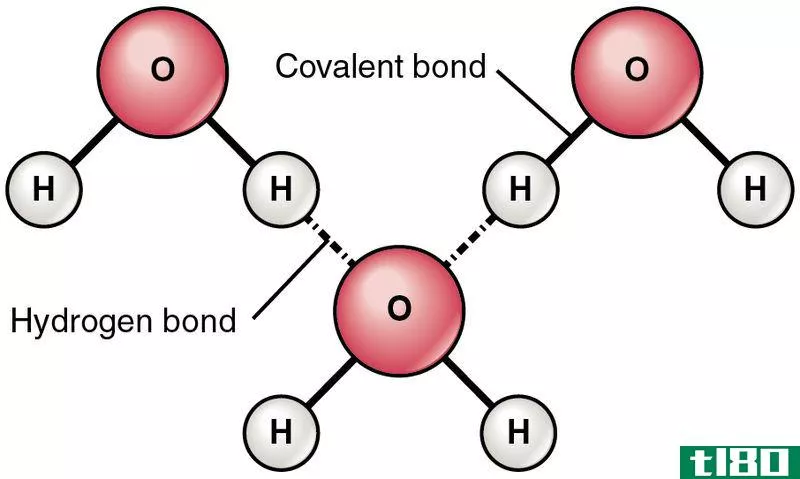
氢键相对比其他偶极相互作用强,它们决定了分子的行为。例如,水分子具有分子间氢键。一个水分子可以与另一个水分子形成四个氢键。由于氧有两个孤对,它可以与带正电荷的氢形成两个氢键。然后,我们可以把这两个水分子称为二聚体。由于氢键的能力,每一个水分子都能与其他四个分子结合。它导致水的沸点更高,即使水分子的分子量很低。因此,当氢键进入气相时,打破氢键所需的能量很高。
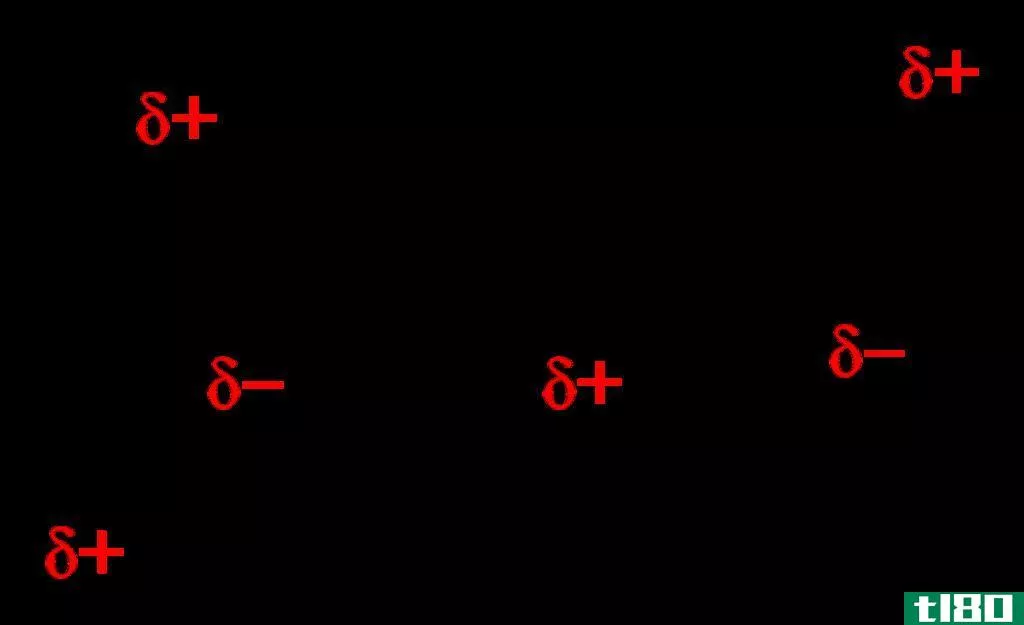
图01:水分子之间的氢键
此外,氢键决定了冰的晶体结构。独特的冰格结构使其能够漂浮在水面上,从而保护了冬季的水生生物。除此之外,氢键在生物系统中起着至关重要的作用。蛋白质和DNA的三维结构完全基于氢键。此外,氢键可以被加热和机械力破坏。
什么是离子键(ionic bond)?
原子可以获得或失去电子,并分别形成负电荷或正电荷粒子。这些粒子叫做离子。离子间存在静电相互作用。离子键合是这些带相反电荷的离子之间的吸引力。静电相互作用的强度很大程度上受离子键中原子的电负性影响。电负性可以测量原子对电子的亲和力。高电负性的原子可以从低电负性原子中吸引电子形成离子键。
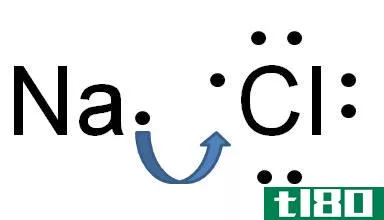
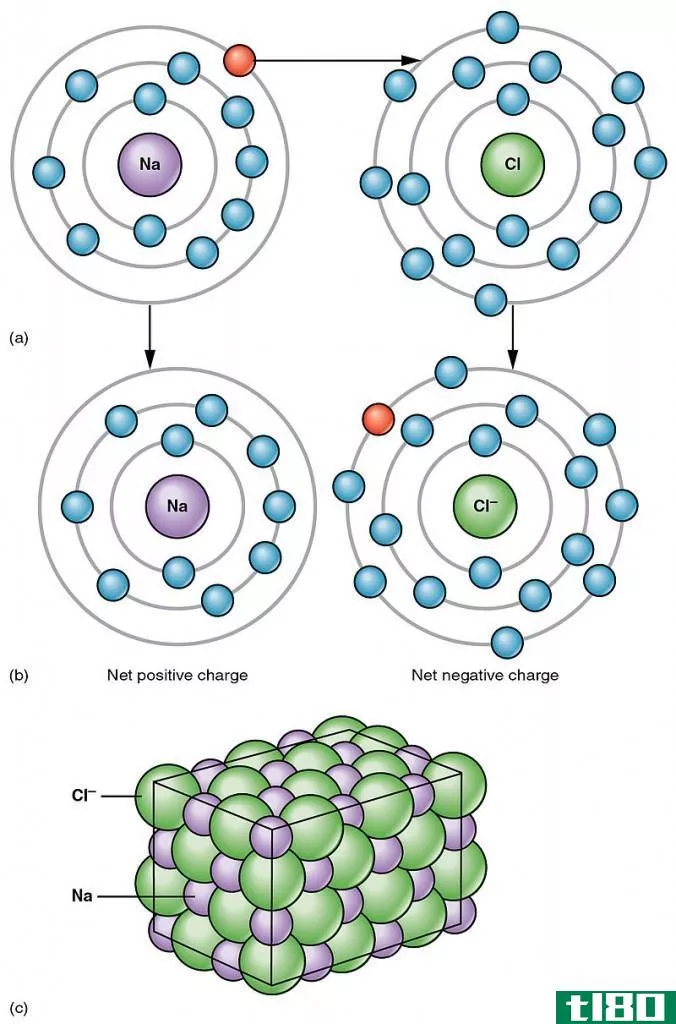
图02:氯化钠中离子键的形成
例如,氯化钠在钠离子和氯离子之间有一个离子键。钠是一种金属,因此它的电负性(0.9)比氯(3.0)低。由于这种电负性的差异,氯可以从钠中吸引一个电子,形成氯离子和钠离子。因此,两个原子都获得了稳定的惰性气体电子组态。Cl-和Na+被很强的吸引静电力结合在一起,从而形成离子键。
氢键(hydrogen bond)和离子键(ionic bond)的区别
氢键是分子间的吸引力,而离子键是有吸引力的静电力。氢键和离子键的关键区别在于,永久性阴阳离子之间存在离子键,而部分正电荷和部分负电荷之间存在氢键。另外,离子键比氢键强。
此外,当存在一个氢原子和一个电负性原子时,氢键就产生了,而离子键则发生在任何金属和非金属原子之间。所以,这是氢键和离子键的显著区别。此外,氢键和离子键的另一个区别是氢键很容易断裂,因为它们要么是分子间的吸引力,要么是分子内的引力,而离子键是很强的化学键,很难被打破。
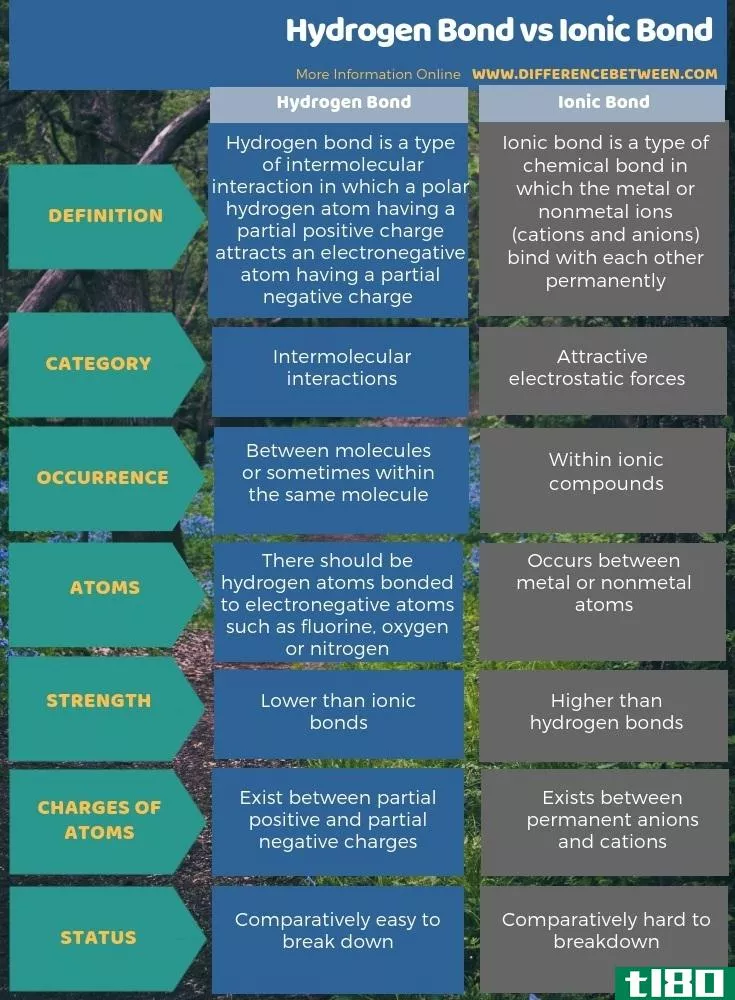
总结 - 氢键(hydrogen bond) vs. 离子键(ionic bond)
离子键发生在离子化合物中。氢键是分子间的键。氢键和离子键的关键区别在于,永久性阴阳离子之间存在离子键,而部分正电荷和部分负电荷之间存在氢键。
引用
1赫尔曼斯汀,安妮·玛丽。“氢键的定义和例子”,ThoughtCo,May。2019年6月6日,可在这里购买。赫尔曼斯汀,安妮·玛丽。“离子键定义”,ThoughtCo,2019年1月26日,可在这里查阅。
2赫尔曼斯汀,安妮·玛丽。“离子键定义”,ThoughtCo,2019年1月26日,