离子键和共价键之间的关键区别在于,离子键发生在电负性非常不同的原子之间,而共价键发生在电负性差异相似或极低的原子之间。
正如美国化学家G.N.Lewis提出的那样,当原子的价壳层中含有8个电子时,原子是稳定的。大多数原子的价壳层中的电子少于8个(周期表第18组中的稀有气体除外);因此,它们是不稳定的。这些原子趋向于相互反应以变得稳定。因此,每一个原子都可以实现稀有气体的电子组态。离子键和共价键是连接化合物中原子的两种主要化学键。

目录
1. 概述和主要区别
2. 什么是离子键
3. 什么是共价键
4. 并列比较-表格式的离子键与共价键
5. 摘要
什么是离子键(ionic bonds)?
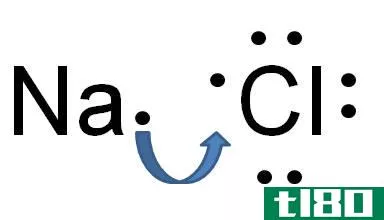
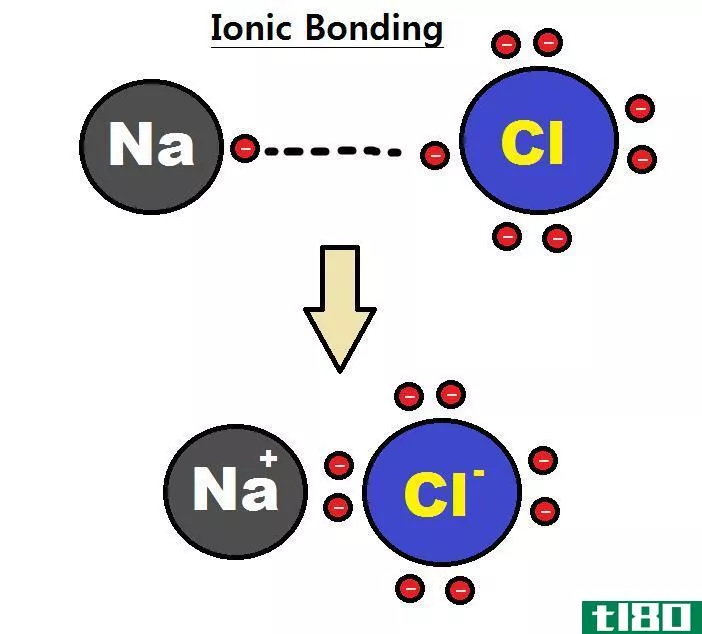
原子可以获得或失去电子,形成负电荷或正电荷的粒子;我们称之为离子。离子间存在静电相互作用。离子键是这些带相反电荷的离子之间的吸引力。离子间的相互作用很大程度上影响了离子间的电性。
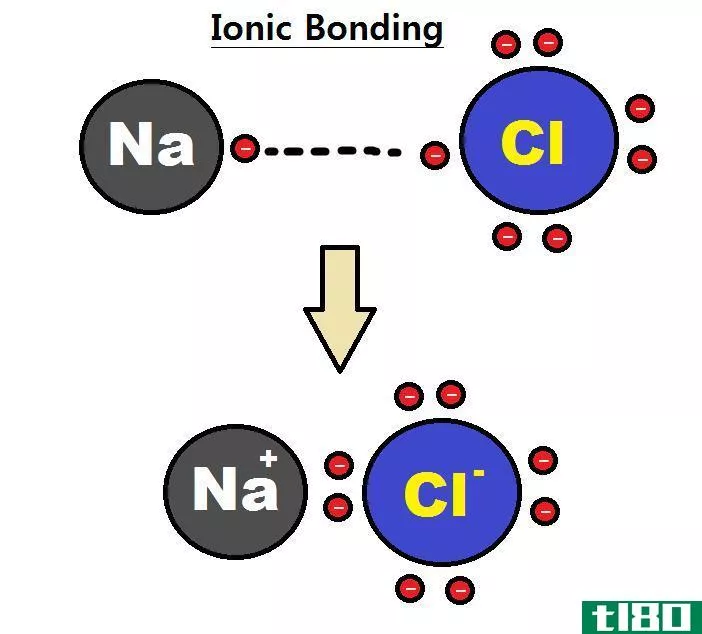
图01:钠和氯原子之间离子键的形成
电负性是原子对电子亲和力的测量。具有高电负性的原子可以从低电负性的原子中吸引电子形成离子键。例如,氯化钠在钠离子和氯离子之间有一个离子键。钠是金属,氯是非金属;因此,与氯(3.0)相比,它的电负性(0.9)非常低。由于这种电负性的差异,氯可以从钠中吸引一个电子并形成Cl-。同时,钠形成钠离子。由于这两个稀有原子的电子构型稳定。Cl-和Na+被吸引的静电力结合在一起,从而形成离子键;Na-Cl键。
什么是共价键(covalent bonds)?
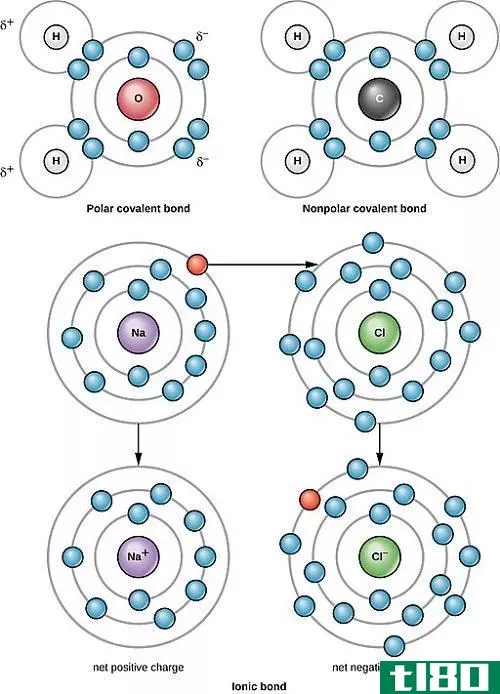
当两个具有相似或极低电负性差的原子发生反应时,它们通过共享电子形成共价键。这样,两个原子都可以通过共享电子而获得稀有气体的电子组态。分子是原子间共价键形成的产物。例如,同一元素的原子结合形成Cl2、H2或P4等分子,每个原子通过共价键与另一个原子结合。
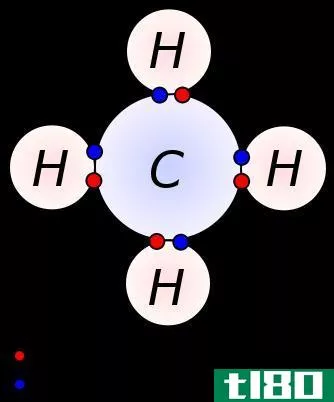
图02:甲烷分子中碳原子和氢原子之间的共价键
甲烷分子(CH4)在碳原子和氢原子之间也有共价键;在一个中心碳原子和四个氢原子之间有四个共价键(四个C-H键)。甲烷是一个分子的例子,原子间具有极低的电负性差的共价键。
离子型(ionic)和共价键(covalent bonds)的区别
| 离子键与共价键 | |
| 由离子化合物中相反带电离子间的静电作用引起的两个原子之间的化学联系。 | 两个原子或离子之间的化学连接,其中电子对在它们之间共享。 |
| 原子数 | |
| 发生在金属和非金属之间。 | 最常见于两种非金属之间。 |
| 电子数 | |
| 电子发生完全转移。 | 当两个(或更多)元素共享电子时发生。 |
| 化合物 | |
| 通常被视为晶体,其中很少有带正电的离子围绕着带负电的离子。 | 共价键结合的原子以分子形式存在,在室温下,主要以气体或液体的形式存在。 |
| 极性 | |
| 离子键有很高的极性。 | 共价键的极性很低。 |
| 物理性质 | |
| 与共价分子相比,离子化合物具有极高的熔点和沸点。 | 共价分子的熔点和沸点比离子化合物低。 |
| 水溶性 | |
| 在极性溶剂(如水)中,离子化合物溶解释放出的离子;这种溶液能够导电。 | 在极性溶剂中,共价分子不会大量溶解,因此这些溶液不能导电。 |
总结 - 离子型(ionic) vs. 共价键(covalent bonds)
离子键和共价键是化合物中存在的两种主要化学键。离子键和共价键的区别在于,在具有极不同电负性的原子之间发生离子键,而共价键发生在具有相似或极低电负性差异的原子之间。
引用
1Helmenstine,Anne Marie博士,“离子键定义”,ThoughtCo,2017年2月10日。在这里可以买到2。Helmenstine,Anne Marie博士,“共价键定义”,ThoughtCo,2018年2月7日。此处提供
2Helmenstine,Anne Marie博士,“共价键定义”,ThoughtCo,2018年2月7日。