共价键和与格键的关键区别在于,当两个原子的未成对电子相互结合时,共价键就形成了;而与格键则是当一个原子将它的一对电子捐赠给另一个原子时形成的。
虽然与格键看起来像共价键,但当我们考虑键的形成时,它们是不同的。但共价键和与格键形成后没有区别。因此,我们通常称与格键为共价键,这是正确的。
目录
1.概述和主要区别
2. 什么是共价键
3. 什么是与格键
4. 并列比较-共价键与与格键的表格形式
5. 摘要
什么是共价键(covalent bond)?
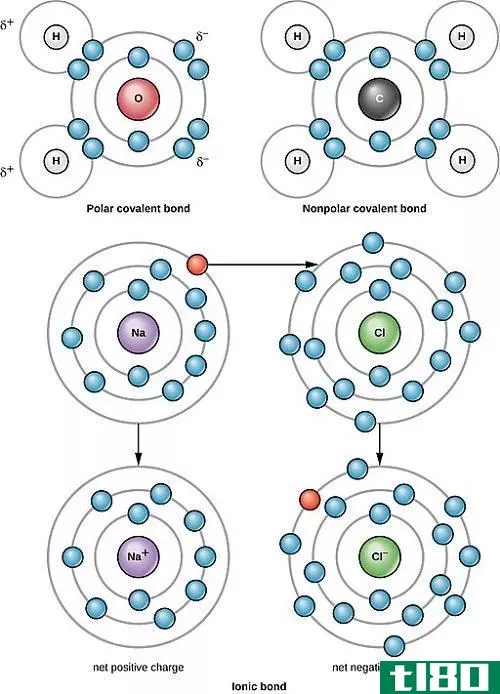
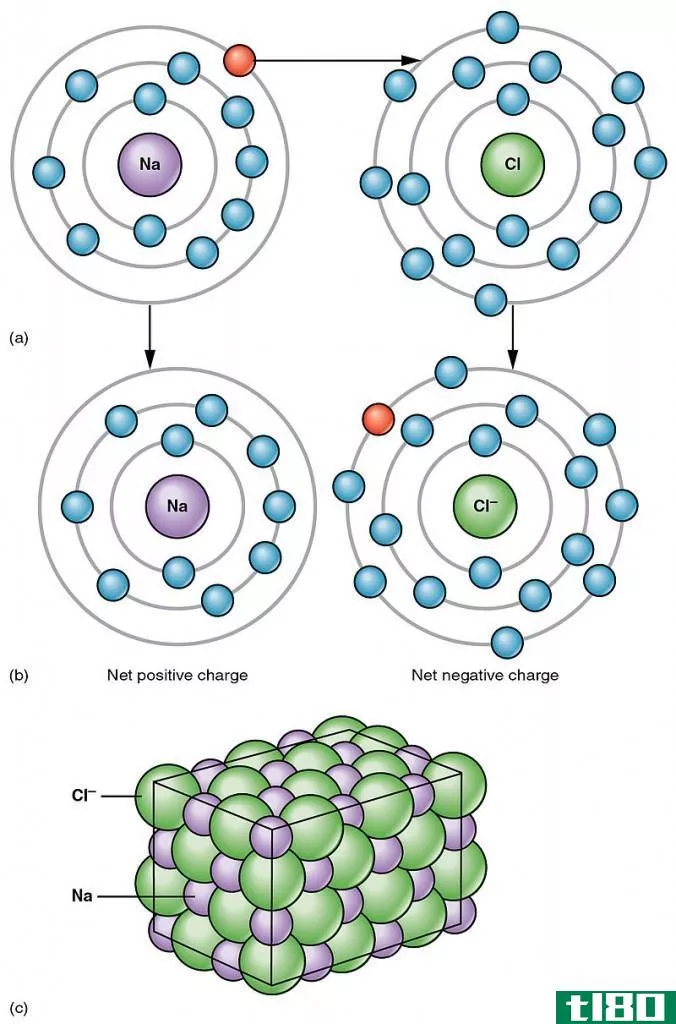
共价键是两个原子共用一对电子时形成的化学键。我们称之为“分子键”。共享的电子是“共享对”或“键对”。当原子共享电子时,由于原子间吸引力和排斥力的稳定平衡而形成的共价键。这种电子共享使得每个原子都有相当于一个完整的外壳。这种键形成于两个电负性值相近的非金属原子之间,或电子与带正电的金属离子之间。

图01:两个氢原子之间共价键的形成
共价键主要有两种类型:极性键和非极性键。两个原子之间存在极性键,它们的电负性值相差在0.4到1.7之间。如果这个差值小于0.4,就会形成非极性键。这是因为,电负性值之间的高差异意味着,一个原子(具有较高的电负性值)比另一个原子更能吸引电子,使键成为极性的。
根据两个原子之间共享的电子对的数量,共价键有三种主要类型。它们是包含一个电子对的单键,包含两个电子对的双键,以及包含三个电子对的三键。
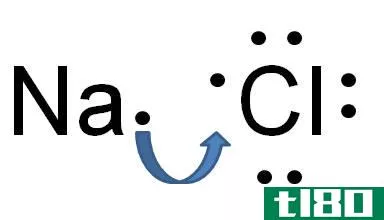
什么是与格键(dative bond)?
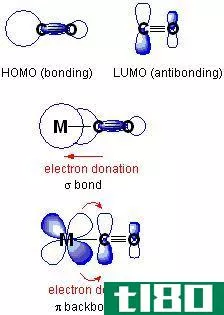
与格键是一种共价键,当一个原子把它的电子对捐给另一个原子时形成。在键形成后,它看起来就像一个共价键。这是因为两个原子共享同一电子对和键对。

图02:与格键的形成
这种键的同义词是“偶极键”和“坐标键”。最常见的例子是配位络合物中的键。在那里,金属离子通过这些配位键与配体结合。
共价键(covalent bond)和与格键(dative bond)的区别
共价键是两个原子共用一对电子时形成的化学键。与格键是一种共价键,当一个原子把它的电子对捐给另一个原子时形成。根据它们的形成方式不同。因此,共价键和与格键的关键区别在于,当两个原子的未成对电子相互结合时,共价键就形成了;而原子将其电子对中的一对捐赠给另一个原子时,共价键就形成了。
下面的信息图以表格形式展示了共价键和与格键之间的区别。
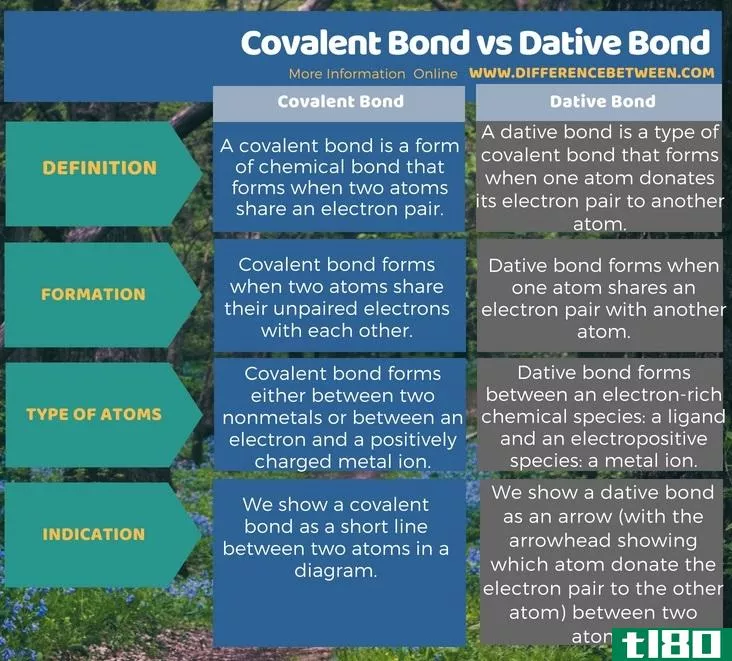
总结 - 共价键(covalent bond) vs. 与格键(dative bond)
键形成后,共价键和与格键似乎都很相似。然而,根据它们形成的方式不同,它们又各不相同。共价键和与格键的区别在于,当两个原子的未成对电子相互结合时,共价键就形成了;而当一个原子将它的一对电子捐赠给另一个原子时,共价键就形成了。
引用
1Helmenstine,Anne Marie博士,“共价键定义”,ThoughtCo,2018年6月22日。这里有2个。Helmenstine,Anne Marie博士,“与格键定义(坐标键)。”ThoughtCo,2018年6月22日。此处提供
2Helmenstine,Anne Marie博士,“与格键定义(坐标键)。”ThoughtCo,2018年6月22日。