离子共价和金属氢化物之间的关键区别在于它们的形成。当氢与高电正性s-块元素反应时形成离子氢化物;当具有可比电负性值的化学元素的原子与氢反应时形成共价氢化物,而当过渡金属与氢反应时形成金属氢化物。
氢化物是一种含有氢阴离子H-的化合物。氢化物主要有离子氢化物、共价氢化物和金属氢化物三种。
目录
1. 概述和主要区别
2. 什么是离子氢化物
3. 什么是共价氢化物
4. 什么是金属氢化物
5. 并列比较-离子与共价与金属氢化物的表格形式
6. 摘要
什么是离子氢化物(ionic hydrides)?
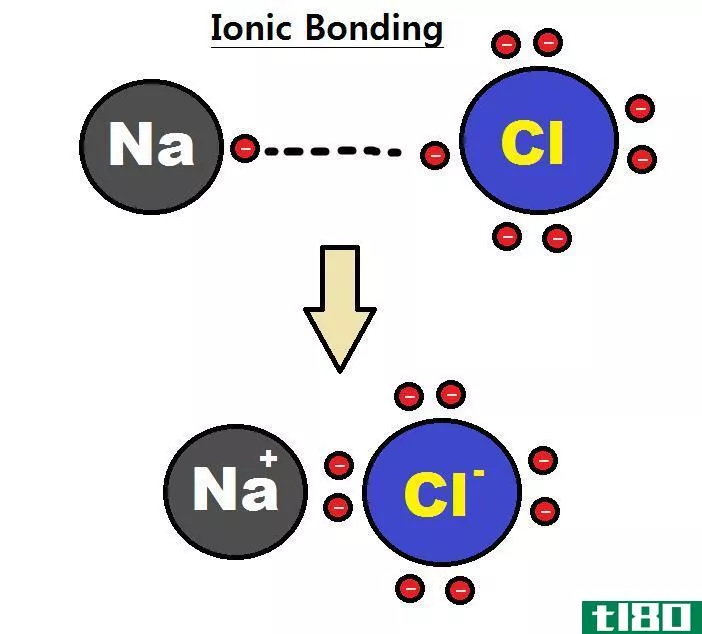
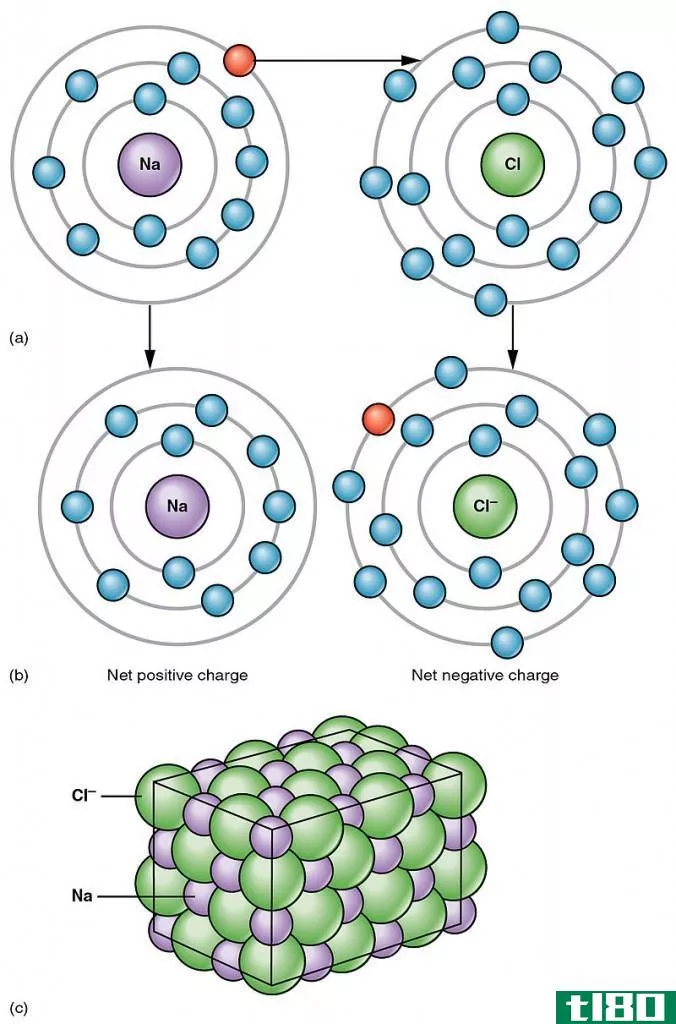
离子氢化物是一种氢化物化合物,它含有一个与高电正性s-嵌段阳离子结合的氢阴离子。这些化合物也被称为盐水氢化物或假卤化物。氢与碱金属和碱土金属群中最活跃的金属结合形成这种氢化物化合物。在这些化合物中,氢处于负氧化状态,氧化数为-1。通常,离子氢化物是一个分子中只有两种化学元素的二元化合物。此外,这些化合物通常不溶于溶液。
什么是共价氢化物(covalent hydrides)?
共价氢化物是一种氢化物化合物,它含有一个与电负性相当的化学元素结合的氢阴离子。在这些化合物中,有一个氢原子和一个或多个非金属原子形成化合物。
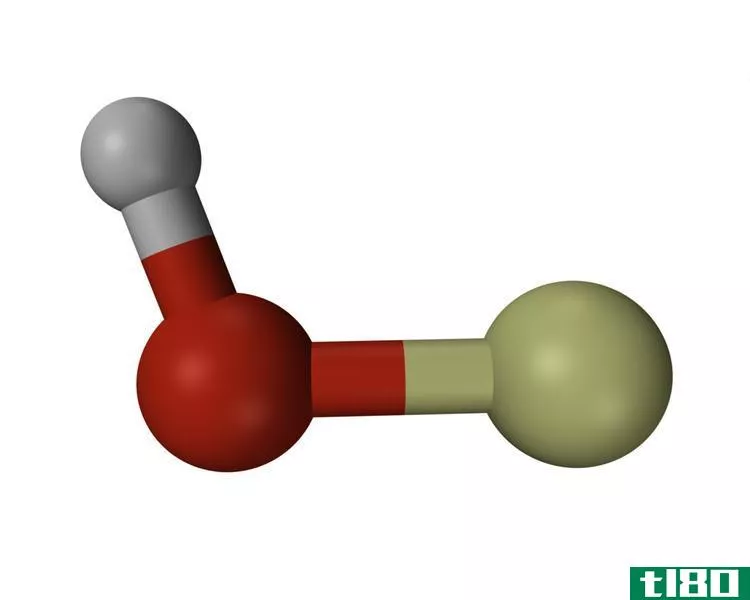
图01:水分子是共价氢化物化合物
氢原子和电正性更强的化学元素之间存在共价化学键。当两个原子共用价电子时,这种化学键就形成了。这些化合物可以是挥发性的,也可以是非挥发性的。
什么是氢化物(metallic hydrides)?
金属氢化物是含与过渡金属元素结合的氢阴离子的氢化物化合物。这些化合物也被称为间隙氢化物。作为这些化合物的一个特征,我们可以观察到它们是非化学计量的化合物。也就是说,化合物中氢原子与金属原子的比例不是一个固定值。换句话说,这些化合物的原子组成是可变的。
离子共价(ionic covalent)和氢化物(metallic hydrides)的区别
氢化物是一种含有氢阴离子H-的化合物。根据与氢负离子结合的化学元素的类型,我们可以将氢化物分为三大类:离子氢化物、共价氢化物和金属氢化物。因此,离子共价键和金属氢化物之间的关键区别在于与氢阴离子结合的化学元素的类型。当氢与高电正性s-块元素反应时形成离子氢化物,当具有可比电负性值的化学元素的原子与氢反应时形成共价氢化物。同时,过渡金属与氢反应形成金属氢化物。
此外,离子氢化物是氢与碱土或碱土族中的高电正性原子的组合,而共价氢化物是氢与具有相对电负性的非金属的组合。但是,金属氢化物是氢和过渡金属的混合物。
下面的信息图表以表格形式总结了离子共价和金属氢化物之间的区别。

总结 - 离子型(ionic) vs. 共价的(covalent)
氢化物主要有三种:离子氢化物、共价氢化物和金属氢化物。离子氢化物、共价氢化物和金属氢化物之间的关键区别在于,当氢与高电正性s-块元素反应时形成离子氢化物,当具有可比电负性值的化学元素的原子与氢反应时形成共价氢化物,而过渡金属与氢反应形成金属氢化物。
引用
1“氢化物”,化学剧本,剧本,2020年8月15日,可在这里获得。